Металл PbO2, или двуокись свинца, является важным веществом в химической промышленности. Получение этого соединения возможно через химическую реакцию между свинцом и углекислым газом (CO2). Реакция эта происходит при определенных условиях и имеет свои химические уравнения.
Уравнение химической реакции между свинцом и углекислым газом может быть записано следующим образом:
Pb + CO2 → PbO2 + C
Это уравнение показывает, что свинец вступает в реакцию с углекислым газом, что приводит к образованию оксида свинца (PbO2) и углерода (C).
Получение металла PbO2 с помощью реакции с углекислым газом имеет свои преимущества и недостатки. С одной стороны, это процесс, который можно осуществить при относительно низкой температуре и обычном давлении. С другой стороны, реакция требует специального оборудования и контроля, чтобы обеспечить правильные условия и получить высокую степень чистоты металла.
Что такое металл PbO2?

PbO2 - это химическое соединение, представляющее собой оксид свинца (IV), который является одним из основных оксидов свинца. Свойства металла PbO2 обусловлены его структурой и составом.
Металл PbO2 обладает темно-коричневым цветом и часто используется в качестве электродного материала, особенно в аккумуляторах и электролитических процессах. Он имеет высокую степень оксидации, что делает его эффективным катализатором для различных химических реакций.
Кроме того, PbO2 является нелистобылевым материалом, который может выделять кислород во время разложения. Это свойство делает его полезным в самовоспламеняющихся и самогорящихся системах, таких как взрывчатые вещества.
Однако следует отметить, что PbO2 является токсичным и может представлять опасность для здоровья человека и окружающей среды. Поэтому при работе с этим металлом необходимо соблюдать все соответствующие меры безопасности.
Как получают металл PbO2?

Металл PbO2, более известный как диоксид свинца, можно получить различными методами.
Одним из способов получения металла PbO2 является термическое разложение свинцового гидроксида. Для этого необходимо подвергнуть нагреву гидроксид свинца при температуре около 350 градусов Цельсия. В результате разложения образуется металл PbO2.
Кроме того, металл PbO2 можно получить с помощью электрохимических методов. Один из таких методов называется электролизом. Для этого необходимо взять свинцовое соединение, например, свинцовую соль, и поместить его в электролит, обычно это раствор кислоты. Затем в электролите заключается электроды - анод и катод. При включении электрического тока происходит процесс электролиза, в результате которого на катоде образуется металл PbO2.
Также металл PbO2 можно получить с помощью химической реакции между свинцовым карбонатом и кислородом. Для этого два компонента смешиваются и подвергаются нагреву. В результате реакции образуется металл PbO2 и выделяется углекислый газ (CO2).
Реакция получения металла PbO2 из Pb и CO2
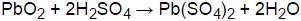
Для получения металла PbO2 из Pb и CO2 необходимо провести химическую реакцию, в результате которой происходит окисление свинца и образование двухокиси свинца.
Вначале свинец (Pb) реагирует с углекислым газом (CO2), образуя оксид свинца (PbO) и выделяя углекислый газ (CO2). Эта реакция может быть представлена уравнением:
Pb + CO2 → PbO + CO2
Полученный оксид свинца (PbO) затем подвергается дополнительному окислению, чтобы получить двуокись свинца (PbO2). Для этого необходимо использовать кислород (O2) в качестве окислителя:
PbO + O2 → PbO2
Таким образом, реакция получения металла PbO2 из Pb и CO2 состоит из двух этапов: сначала образуется оксид свинца (PbO), а затем он окисляется до двуокиси свинца (PbO2).
Уравнение химической реакции для получения металла PbO2 из Pb и CO2
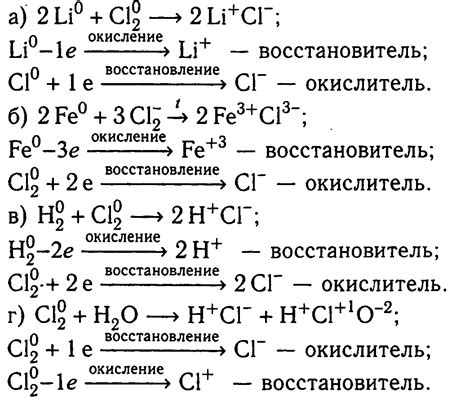
Детальное уравнение химической реакции для получения металла PbO2 из Pb и CO2 выглядит следующим образом:
- В исходной реакции свинец (Pb) реагирует с углекислым газом (CO2), образующимся, например, в результате сгорания горючих материалов.
- Уравнение реакции можно записать следующим образом: Pb + CO2 → PbO2 + CO.
- В этой реакции атом свинца (Pb) окисляется и образует оксид свинца(IV) (PbO2), в то время как углекислый газ (CO2) восстанавливается и образует угарный оксид (CO).
- В результате этой реакции свинец превращается в оксид свинца(IV), который используется, например, для производства кислородных электродов в батареях.
Таким образом, уравнение химической реакции для получения металла PbO2 из свинца (Pb) и углекислого газа (CO2) может быть представлено как Pb + CO2 → PbO2 + CO.
Значение металла PbO2 в промышленности и научных исследованиях

Металл PbO2 (диоксид свинца) имеет значительное значение в промышленности и научных исследованиях. Данный материал обладает свойствами, которые позволяют его использовать в различных сферах деятельности.
В промышленности PbO2 применяется, в первую очередь, благодаря своей химической активности. Металл используется в процессах производства кислот, аккумуляторов и различных электрохимических устройств. Например, PbO2 используется в аккумуляторах автомобилей, поскольку образует высокопроизводительную анодную плату.
Научные исследования в области электрохимии также активно применяют PbO2. Данный металл используется в качестве катода в различных электролитических системах. Это связано с его способностью к эффективному электрохимическому окислению многих органических и неорганических веществ.
Кроме того, PbO2 нашел применение в других научных областях. Например, в аналитической химии данный металл используется в качестве катализатора при различных химических реакциях. Он также находит применение в исследованиях, связанных с электрохимическим окислением и процессами разложения органических соединений.
Таким образом, металл PbO2 является важным материалом в промышленности и научных исследованиях. Его химические и электрохимические свойства позволяют применять его в различных областях и способствуют развитию новых технологий и научных открытий.
Вопрос-ответ

Какой метод используется для получения металла PbO2 с Pb CO2?
Металл PbO2 с Pb CO2 получается с помощью электролиза раствора соли свинца (II) с использованием электрода из свинца. При этом на положительном электроде образуется PbO2, а на отрицательном электроде — металлический свинец.
Какие вещества используются при получении металла PbO2 с Pb CO2?
Для получения металла PbO2 с Pb CO2 используются раствор соли свинца (II) и электроды из свинца. Раствор соли свинца (II) содержит ионы свинца (Pb2+) и карбонатные ионы (CO32-). При прохождении электрического тока через раствор, происходит окисление свинца на положительном электроде и восстановление на отрицательном, что приводит к образованию металла PbO2 и выделению CO2.
