Металлы и неметаллы - две основные группы элементов, составляющих химическую таблицу. Каждая из этих групп имеет свою уникальную структуру атомов, которая влияет на их физические и химические свойства. Изучение различий в атомах металлов и неметаллов является важным шагом к пониманию их химического поведения и применения в различных отраслях промышленности и научных исследований.
Одной из основных различий в атомах металлов и неметаллов является их структура. Атомы металлов обычно имеют относительно небольшое количество электронов во внешней электронной оболочке. Это делает атомы металлов склонными к отдельному или общему использованию электронов с другими атомами, образуя положительно заряженные ионы. Неметаллы, напротив, имеют больше электронов во внешней электронной оболочке и обычно стремятся принимать или разделять электроны с другими атомами, образуя отрицательно заряженные ионы. Это различие в строении атомов определяет их химическую активность и те свойства, которые мы наблюдаем в повседневной жизни.
Примеры различий в атомах металлов и неметаллов могут быть найдены в их физических свойствах. Металлы характеризуются высокой термической и электрической проводимостью, блеском, пластичностью и хорошей теплопроводностью. Эти свойства связаны с способностью металлических атомов легко образовывать межатомные связи и перемещать свою электронную структуру. Неметаллы, напротив, имеют низкую термическую и электрическую проводимость, часто являются хрупкими и непроводящими тепла материалами. Подобные физические свойства обусловлены большой разницей в электронной структуре атомов неметаллов, что приводит к ограниченным возможностям перемещения электронов и проводимости тепла и электричества.
Атомы металлов и неметаллов: общая информация

Металлы - это элементы, которые обладают характеристиками, отличающимися от элементов неметаллов. Основные черты металлов включают высокую электропроводность, высокую теплоемкость, блеск и малую силу электроотталкивания между атомами. Металлы, как правило, имеют низкую электроотрицательность и малый энергетический разрыв между энергетическими уровнями атомов.
Неметаллы - это элементы, которые обладают противоположными свойствами по сравнению с металлами. Они обычно характеризуются низкой электропроводностью, неблеском, высокой электроотрицательностью и большой силой электроотталкивания между атомами. Чаще всего неметаллы образуют ковалентные связи и имеют высокий энергетический разрыв между уровнями атомов.
В таблице приведены некоторые примеры металлов:
- Железо (Fe)
- Алюминий (Al)
- Медь (Cu)
- Олово (Sn)
- Серебро (Ag)
А вот некоторые примеры неметаллов:
- Кислород (O)
- Углерод (C)
- Азот (N)
- Фтор (F)
- Хлор (Cl)
Понимание различий между атомами металлов и неметаллов помогает понять их химические и физические свойства, а также их роль в различных процессах и приложениях. Эти различия могут также влиять на их реактивность, способность образовывать соединения и другие характеристики, которые могут быть полезными в различных областях науки и промышленности.
Основные отличия

1. Металлы и неметаллы
Металлы и неметаллы представляют собой две основные категории элементов в периодической системе химических элементов. Металлы обладают такими характеристиками, как высокая электропроводность, блеск, хорошая пластичность и способность образовывать ионы с положительным зарядом (катионы). Неметаллы, напротив, имеют низкую электропроводность, некоторые из них могут быть прозрачными или хрупкими, и способны образовывать ионы с отрицательным зарядом (анионы).
2. Атомная структура
Металлы и неметаллы также различаются в своей атомной структуре. Атомы металлов обычно имеют маленькое количество электронов во внешней оболочке и образуют ионические связи, передавая электроны другим элементам. В то же время атомы неметаллов имеют высокую электроотрицательность и образуют ковалентные связи, которые включают обмен электронами между атомами для создания молекул.
3. Окисление и восстановление
Металлы и неметаллы также различаются в своих окислительных свойствах. Металлы имеют тенденцию хорошо окисляться, т.е. терять электроны, и работают как восстановители. Неметаллы, напротив, имеют тенденцию быть окислителями, т.е. принимать электроны, что делает их более реактивными.
4. Физические свойства
Металлы и неметаллы также различаются в своих физических свойствах. Металлы, как правило, обладают высокой плотностью, высокой температурой плавления и кипения, а также хорошей теплопроводностью и электропроводностью. Неметаллы обычно обладают низкой плотностью, низкой температурой плавления и кипения, и обычно являются непроводниками электричества и тепла.
5. Химические свойства
Металлы и неметаллы обладают различными химическими свойствами. Металлы имеют тенденцию образовывать щелочные или щелочноземельные оксиды, которые растворяются в воде, образуя основания. Неметаллы, напротив, образуют кислые оксиды, которые реагируют с водой, образуя кислоты. Кроме того, металлы могут образовывать ионы с положительным зарядом, тогда как неметаллы могут образовывать ионы с отрицательным зарядом.
Металлы

Металлы - это класс элементов химической системы, который обладает определенными физическими и химическими свойствами. Они обычно относятся к группе элементов на периодической таблице между металлоидами и неметаллами.
- Физические свойства металлов: большая электропроводность, высокая теплопроводность, блеск, высокая плавкость и ковкость.
- Химические свойства металлов: способность образовывать ионы с положительным зарядом, образование щелочных оксидов и оснований при реакции с кислородом и водой.
Металлы могут быть обработаны, чтобы получить различные формы и использоваться для создания различных продуктов и конструкций. Они широко применяются в промышленности, включая производство стали, производство электроники и использование в строительстве.
| Примеры металлов | Примечания |
|---|---|
| Железо | Широко используется в производстве металлических изделий и строительстве. |
| Алюминий | Легкий и прочный металл, часто используется в авиации и строительстве. |
| Медь | Используется в электротехнике и производстве проводников. |
Металлы также имеют различные сплавы, которые могут изменять их свойства и предоставлять дополнительные химические и физические свойства. Такие сплавы, как бронза и сталь, широко используются в различных отраслях промышленности и строительства.
Неметаллы

Неметаллы - это элементы, которые обладают отличными от металлов свойствами и химической структурой. Они находятся в правой части периодической таблицы элементов и включают такие элементы, как кислород, азот, сера и фтор.
Основные характеристики неметаллов включают низкую электропроводность, хрупкость, нежелание образовывать катионы и способность образовывать отрицательные ионы (анионы) в химических соединениях. Неметаллы обычно образуют простые молекулы или сетчатые структуры в кристаллической форме.
Неметаллы играют важную роль в химической промышленности, медицине и обычной жизни. Они используются в производстве пластиков, синтетических материалов, лекарственных препаратов и многих других продуктов. Некоторые неметаллы, такие как кислород и азот, являются важными газами, необходимыми для дыхания и различных химических процессов.
Неметаллы также имеют ряд других интересных свойств. Например, фтор является самым электроотрицательным элементом, что делает его очень реактивным и способным вступать во множество химических реакций. Сера образует красивые желтые кристаллы и используется в производстве порошкового сернистого взрывчатого вещества. Оксид азота, известный как смог, является главным загрязнителем воздуха и причиной многих проблем здоровья и окружающей среды.
Таким образом, неметаллы имеют особую роль и значение в нашей жизни и играют важную роль в различных отраслях науки и промышленности.
Физические свойства металлов
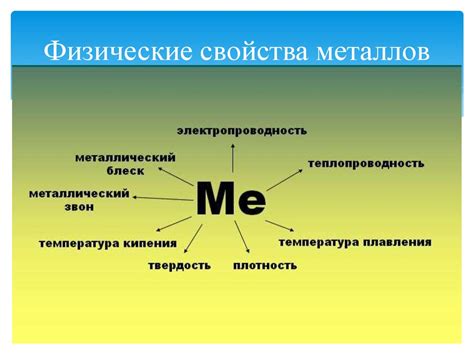
Металлы – это вещества, обладающие рядом характерных физических свойств, которые отличают их от других классов элементов в таблице Менделеева.
Внешне металлы обычно имеют блестящую поверхность, называемую металлическим блеском. Они могут быть серебристого, белого, желтого, или серого цвета, а также покрываться патиной, когда находятся в воздухе. Металлы характеризуются высокой теплопроводностью, электропроводностью и пластичностью.
У металлов есть высокая плотность, то есть они обладают большой массой на единицу объема. Кроме того, металлы обычно имеют высокую точку плавления и кипения, что делает их полезными в множестве промышленных процессов.
Металлы обычно образуют кристаллическую решетку, в которой положение и расположение атомов характеризуются особыми правилами и структурами. В результате этого у них обычно есть регулярная форма и решетчатая структура.
В целом, физические свойства металлов объясняются особыми свойствами и поведением их электронов, в особенности свободными электронами, которые могут легко передвигаться внутри металлической решетки.
Физические свойства неметаллов

Неметаллы отличаются от металлов своими особыми физическими свойствами. Одно из главных отличий заключается в том, что неметаллы в обычных условиях обладают низкой электропроводностью. Это связано с тем, что в атомах неметаллов отсутствуют свободные электроны, которые бы могли перемещаться по атомам и обеспечивать проводимость.
Другим важным физическим свойством неметаллов является их хрупкость. В отличие от металлов, которые могут быть подвержены пластической деформации, неметаллы обычно легко разрушаются при механическом воздействии. Это объясняется часто слабыми связями между атомами в структуре неметаллов.
Еще одним характерным физическим свойством неметаллов является их низкая плотность. По сравнению с металлами, у неметаллов обычно наблюдается низкая плотность атомарных структур. Это связано с отсутствием тяжелых элементов в атомных ядрах неметаллов.
Некоторые неметаллы также обладают свойством быть хорошими изоляторами тепла, благодаря низкому теплопроводности. Это позволяет использовать неметаллы в качестве теплоизоляционных материалов, например, в строительстве.
Однако неметаллы могут обладать и другими физическими свойствами, в зависимости от конкретного элемента. Например, некоторые неметаллы могут быть газообразными при комнатной температуре (например, кислород и азот), одновременно другие - твердыми (например, сера и фосфор).
Примеры атомов металлов

Атомы металлов обладают особыми свойствами и структурой, что делает их отличающимися от атомов неметаллов. Вот несколько примеров атомов металлов.
1. Железо (Fe): Железо является одним из самых распространенных металлов на Земле. Атом железа имеет атомный номер 26 и электронную конфигурацию [Ar] 3d^6 4s^2. Железо обладает высокой проводимостью электричества и тепла, а также имеет магнитные свойства.
2. Медь (Cu): Медь также является распространенным металлом и имеет атомный номер 29. Атом меди имеет электронную конфигурацию [Ar] 3d^10 4s^1. Медь отличается высокой электропроводностью и теплопроводностью, а также обладает отличными антикоррозионными свойствами.
3. Алюминий (Al): Алюминий является легким металлом с атомным номером 13. Атом алюминия имеет электронную конфигурацию [Ne] 3s^2 3p^1. Алюминий имеет низкую плотность, но при этом он обладает высокой прочностью и химической устойчивостью.
4. Свинец (Pb): Свинец также относится к металлам. Атом свинца имеет атомный номер 82 и электронную конфигурацию [Xe] 4f^14 5d^10 6s^2 6p^2. Свинец является мягким и пластичным металлом, а также обладает высокой плотностью и плавится при относительно низкой температуре.
Эти примеры иллюстрируют многообразие свойств и характеристик атомов металлов. Они имеют определенные электронные конфигурации и способность к образованию ионов, что делает их особенно полезными и ценными в различных областях науки и промышленности.
Примеры атомов неметаллов
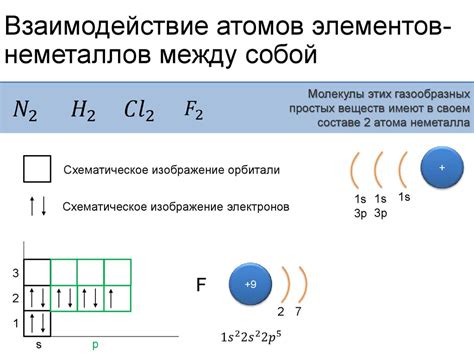
Неметаллы представляют собой группу элементов, характеризующихся отличными от металлов свойствами. Их атомы, в отличие от атомов металлов, обладают высокой электроотрицательностью, что позволяет им притягивать электроны к своему атомному ядру, образуя стабильные молекулы.
Примером неметалла может служить атом кислорода (O). Атом кислорода имеет 8 электронов, расположенных в двух энергетических оболочках. Внешняя оболочка атома кислорода содержит 6 электронов, что говорит о его высокой электроотрицательности. Кислород является ключевым элементом для поддержания жизни на Земле, так как он играет важную роль в дыхании живых организмов и окислительных процессах.
Другим примером неметалла является атом азота (N). Атом азота имеет 7 электронов, расположенных в двух энергетических оболочках. Внешняя оболочка содержит 5 электронов, что делает атом азота электроотрицательным. Азот является основным компонентом воздуха и играет важную роль в биологических процессах. Он является составной частью белков, нуклеиновых кислот и других важных молекул в организмах.
Еще одним примером неметалла является атом фтора (F). Атом фтора содержит 9 электронов, расположенных в двух энергетических оболочках. Имея высокую электроотрицательность, атом фтора с легкостью присоединяет электроны и образует стабильные молекулы. Фтор является одним из самых активных химических элементов и широко используется в стоматологии и химической промышленности.
Вопрос-ответ

Какие атомы считаются металлами, а какие - неметаллами?
Атомы считаются металлами, если они обладают следующими характеристиками: высокая электропроводность, блеск, хорошая теплоотдача. Атомы, которые не обладают этими свойствами, считаются неметаллами.
Какие элементы относятся к металлам, а какие - к неметаллам?
К металлам относятся такие элементы, как железо, алюминий, медь, свинец, золото и другие. К неметаллам относятся кислород, углерод, азот, фтор и другие.
Каким образом различаются атомы металлов и неметаллов по строению?
Атомы металлов обычно имеют маленькие радиусы и низкую электроотрицательность. Атомы неметаллов, напротив, имеют большие радиусы и высокую электроотрицательность.
Какие свойства отличают атомы металлов от атомов неметаллов?
Атомы металлов обычно обладают высокой электропроводностью, блеском и хорошей теплоотдачей. Атомы неметаллов больше склонны к образованию ковалентных связей и обладают более высокой электроотрицательностью.
