Азотная кислота (HNO3) является одним из наиболее распространенных химических соединений, которое активно применяется в различных отраслях промышленности и лабораториях. Одним из важных направлений исследований является изучение взаимодействия азотной кислоты с металлами, так как это процесс имеет большое значение для понимания механизмов химических реакций и получения новых материалов.
Особенности взаимодействия металлов с концентрированной азотной кислотой связаны с высокой реакционной способностью этого соединения. В результате взаимодействия происходит окисление металлов и образование соответствующих нитратов.
В зависимости от степени концентрации азотной кислоты и типа металла процесс взаимодействия может иметь различный характер. Высокая концентрация азотной кислоты ускоряет процесс окисления и может привести к образованию высокореакционных соединений. Кроме того, некоторые металлы могут образовывать защитные пленки оксидов, что препятствует дальнейшему окислению.
Результаты исследования взаимодействия металлов с концентрированной азотной кислотой являются важным основанием для разработки новых материалов с определенными химическими и физическими свойствами. Они также позволяют оптимизировать процессы получения и обработки металлических изделий и обеспечить их более долгий срок службы. Помимо этого, изучение взаимодействия металлов с азотной кислотой имеет значение в контексте экологической безопасности и обеспечения наиболее эффективного использования химических соединений в производстве.
Металлы и концентрированная азотная кислота
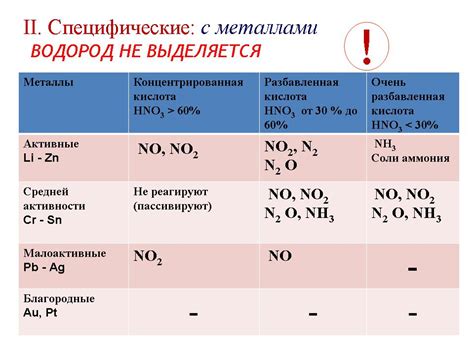
Металлы могут реагировать с концентрированной азотной кислотой, образуя соли и выделяя азотные оксиды. Эта реакция является одной из наиболее характерных для многих металлов и может иметь различные результаты, зависящие от условий и окружающей среды.
Взаимодействие металлов с концентрированной азотной кислотой может привести к образованию разнообразных продуктов. Некоторые металлы, например, железо, медь и никель, образуют нитраты, которые растворяются в кислоте и дают прозрачные растворы.
Другие металлы, такие как цинк и свинец, могут образовывать нитраты, но при этом происходит выделение гидроксида металла. Это связано с тем, что ионы гидроксида, образующиеся в результате реакции, не растворяются в кислоте и образуют осадок.
Некоторые металлы, например, алюминий и магний, реагируют с концентрированной азотной кислотой, образуя аммиак. Это связано с тем, что азотная кислота окисляет металлы до более высоких степеней окисления, при этом выделяется аммиак и образуются нитраты.
Реакция металлов с азотной кислотой
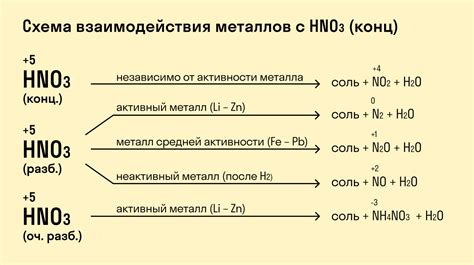
Азотная кислота является сильным окислителем и активно взаимодействует с металлами, приводя при этом к различным результатам. Реакция может протекать с выделением газа, образованием соединений или изменением цвета раствора.
Взаимодействие металлов с азотной кислотой зависит от их электрохимических свойств. Некоторые активные металлы, такие как натрий, калий, магний, алюминий, реагируют с азотной кислотой, выделяя аммиак и окисляясь до соответствующих ионов. В результате образуются нитраты металлов, которые растворяются в воде.
Другие металлы, такие как железо, медь и свинец, могут образовывать нитраты, но они не растворяются в воде и образуют покрытие на поверхности металла. Это покрытие защищает металл от дальнейшего окисления и коррозии.
Реакция металлов с азотной кислотой может протекать в различных условиях в зависимости от концентрации кислоты и времени взаимодействия. Изменение концентрации кислоты или времени реакции может влиять на скорость и интенсивность процесса.
Таким образом, взаимодействие металлов с азотной кислотой является сложным и многогранным процессом, результаты которого зависят от многих факторов. Изучение данного явления позволяет понять и применять его в различных областях, таких как химическая промышленность, аналитическая химия и материаловедение.
Влияние концентрации азотной кислоты на взаимодействие с металлами
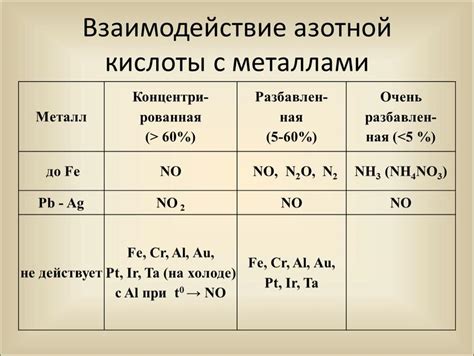
Взаимодействие металлов с концентрированной азотной кислотой является сложным процессом, который зависит от множества факторов, одним из которых является концентрация кислоты. Более высокая концентрация азотной кислоты может способствовать более интенсивному взаимодействию с металлами.
Увеличение концентрации азотной кислоты может привести к ускоренной реакции окисления металла, что в свою очередь может приводить к образованию большего количества окиси металла на поверхности. Это может быть особенно заметно при взаимодействии с более реактивными металлами, такими как медь или цинк.
Однако, при очень высокой концентрации азотной кислоты может происходить обратный эффект - металл может связаться с кислотой сильнее, что в результате приведет к образованию слоя пассивации на поверхности металла. Такой слой может защищать металл от дальнейшего разрушения и окисления.
Исходя из этого, можно сделать вывод о том, что концентрация азотной кислоты играет важную роль в процессе взаимодействия металлов с этой кислотой. Она может как ускорять, так и замедлять процесс окисления металла, что является фундаментальным фактором в изучении данного взаимодействия.
Поведение различных металлов в присутствии азотной кислоты
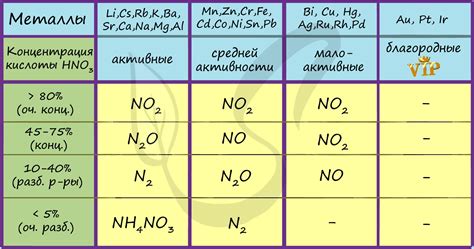
При взаимодействии различных металлов с концентрированной азотной кислотой происходят разнообразные химические реакции, которые могут привести к образованию различных продуктов и изменению свойств металла.
Например, медь при контакте с азотной кислотой выделяет диоксид азота и образует нитрат меди. При этом поверхность меди может облупиться и образоваться медный осадок.
Алюминий, в свою очередь, реагирует с азотной кислотой с образованием алюминиевого нитрата и выделением аммиака. При этом образующаяся пленка оксида алюминия может защитить металл от дальнейшего взаимодействия с кислотой.
Железо образует ферроусольную кислоту в результате взаимодействия с азотной кислотой и выделяет диоксид азота. В зависимости от концентрации кислоты и условий реакции может образоваться ржавчина на поверхности железа.
Металл цинк при столкновении с азотной кислотой образует нитрат цинка и диоксид азота. При этом может наблюдаться эффект "погружения" металла в раствор, связанный с образованием пленки оксида цинка.
Таким образом, поведение различных металлов в присутствии азотной кислоты зависит от их химической активности и может привести к образованию разнообразных продуктов, а также изменению физических и химических свойств металла.
Результаты реакций металлов с концентрированной азотной кислотой
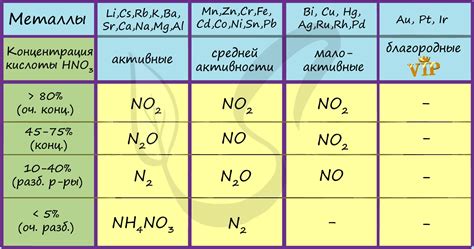
Азотная кислота, обычно известная как химическое соединение HNO3, является сильным окислителем и способна взаимодействовать с различными металлами. Реакции металлов с концентрированной азотной кислотой приводят к появлению характерных химических изменений и образованию соответствующих продуктов.
Реакция металлов с азотной кислотой протекает с выделением газа и образованием солей. При этом металл окисляется, а HNO3 восстанавливается. Например, реакция железа Fe с HNO3 приводит к образованию Fe(NO3)2, а при взаимодействии меди Cu с HNO3 образуется Cu(NO3)2.
Экспериментально было установлено, что скорость реакции зависит от ряда факторов, таких как концентрация азотной кислоты, поверхность металла и температура. Более реакционноспособные металлы, такие как алюминий, магний и цинк, быстро реагируют с азотной кислотой, приводя к образованию соответствующих солей и выделению газа.
Наблюдения показали, что при взаимодействии металлов с концентрированной азотной кислотой образуется густой, пахучий и ядовитый белый дым. Это в азотную кислоту взаимодействует с водой, образуя смесь оксидов азота, которая выделяется в виде дыма. Оксиды азота являются раздражающими веществами и могут вызывать различные проблемы со здоровьем.
Важность изучения взаимодействия металлов с азотной кислотой для промышленных процессов
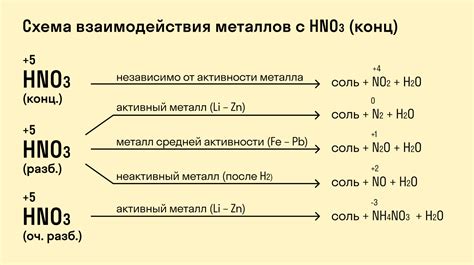
Изучение взаимодействия металлов с азотной кислотой имеет огромную важность для промышленных процессов. Металлы широко применяются в различных промышленных отраслях, и знание их поведения в условиях взаимодействия с азотной кислотой позволяет оптимизировать процессы производства.
Азотная кислота является сильным окислителем и обладает высокой химической активностью. Взаимодействие металлов с азотной кислотой может привести к различным химическим реакциям, таким как окисление, нитрование и даже разрушение материала. Изучение этих реакций позволяет предсказывать влияние азотной кислоты на материалы и разработывать специальные меры для защиты металлических конструкций.
Кроме того, изучение взаимодействия металлов с азотной кислотой является важным для разработки новых материалов и технологий. Понимание особенностей взаимодействия позволяет разрабатывать новые материалы с улучшенными химическими и физическими свойствами, которые могут быть эффективно использованы в промышленности.
Также изучение взаимодействия металлов с азотной кислотой позволяет определить оптимальные условия и параметры процессов производства, таких как процессы обработки, очистки или нанесения покрытий. Это позволяет улучшить эффективность и надежность процессов, а также снизить затраты на обслуживание и ремонт оборудования.
В целом, изучение взаимодействия металлов с азотной кислотой имеет большое практическое значение для промышленных процессов. Непосредственное применение результатов таких исследований может привести к улучшению качества и эффективности производства, а также повышению безопасности и надежности промышленных конструкций и оборудования.
Вопрос-ответ

Какие металлы взаимодействуют с концентрированной азотной кислотой?
С концентрированной азотной кислотой взаимодействуют многие металлы, включая железо, медь, цинк, алюминий, свинец и другие. Однако, скорость и характер взаимодействия могут различаться в зависимости от металла.
Каков механизм взаимодействия металлов с концентрированной азотной кислотой?
Механизм взаимодействия металлов с концентрированной азотной кислотой заключается в окислительно-восстановительной реакции. В процессе взаимодействия металл окисляется, а азотная кислота восстанавливается. Результатом такой реакции может быть образование солей азотной кислоты и выделение газа.
