Металлы - это один из основных классов веществ, обладающих удивительными свойствами и широким спектром применений. Одной из основных причин таких уникальных характеристик металлов является особенность их атомной структуры и особая природа металлической связи.
Металлическая связь - это электростатическое взаимодействие между положительно заряженными иоными ядрами металла и общими "облаками" свободных электронов. Она является одной из самых прочных и устойчивых связей и обеспечивает металлам такие уникальные свойства, как высокая теплопроводность, электропроводность, хорошая пластичность и формоизменность.
Причина возникновения металлической связи заключается в особенностях электронной структуры атомов металлов. В отличие от атомов неметаллов, атомы металлов имеют несколько энергетических уровней, наполненных электронами. При ионизации металла, электроны с самого внешнего уровня освобождаются и становятся свободными, что образует электронное "облако" в металле.
Металлическая связь объясняется моделью "электронного газа", где свободные электроны передвигаются между положительно заряженными ионами металла. Это создает эффект коллективного движения электронов, что обеспечивает высокую подвижность и электропроводность металлов.
Такому объяснению металлической связи соответствует и наличие свободных электронов в проводниках, которые способны перемещаться под действием электрического поля. Благодаря этим свободным электронам металлы могут легко проводить электрический ток, а также выдерживать большие механические нагрузки и изменять форму без разрушения.
Формирование кристаллической решетки
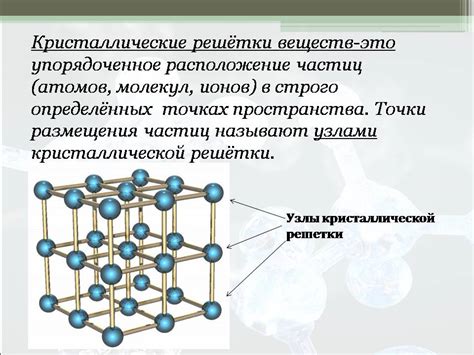
Металлы характеризуются наличием кристаллической решетки, которая образована атомами металла, расположенными в определенном порядке. Формирование кристаллической решетки в металлах объясняется особенностями металлической связи.
Кристаллическая решетка металлов обладает регулярной структурой, которая представляет собой трехмерную сетку, состоящую из однотипных кубических или гексагональных элементов. В каждом узле решетки находится атом металла, который окружен соседними атомами, образуя устойчивое кристаллическое положение.
Образование кристаллической решетки связано с двумя основными факторами: внутренним движением атомов и притяжением между ними. Внутреннее движение атомов происходит из-за их теплового движения, которое оказывает влияние на структуру и форму решетки. Притяжение между атомами металлов объясняется их специальными электронными оболочками.
Кристаллическая решетка металлов обладает рядом особенностей. Это высокая прочность материала, хорошая проводимость электричества и тепла, а также способность к деформации без разрушения. Ориентация и размеры кристаллов в решетке могут значительно варьироваться в зависимости от вида металла и условий его формирования.
Электронная структура металлов

Электронная структура металлов имеет свои особенности, которые объясняют многие свойства данных веществ. Основной элемент в электронной структуре металлов – металлическая сетка, состоящая из положительно заряженных ионов металла и свободных электронов, называемых электронами проводимости.
Ионная решетка металлов обладает высокой степенью упакованности. В металлической решетке ионы металла располагаются регулярно и тесно упакованы в кристаллическую решетку, что делает металлы плотными и твердыми материалами.
Электроны проводимости в металлах обладают свободной подвижностью внутри металлической сетки. Они образуют электронное море, которое позволяет металлам иметь хорошую электропроводность и теплопроводность. Свободные электроны могут перемещаться под воздействием электрического поля и создавать электрический ток. Благодаря этим свободным электронам металлы могут быть использованы в различных электрических и электронных устройствах.
Электронная структура металлов также объясняет их способность образовывать сплавы и легированные материалы. Присутствие свободных электронов в металлической решетке позволяет атомам других элементов встраиваться в эту решетку, образуя сплавы с улучшенными свойствами, такими как повышенная прочность или устойчивость к коррозии.
Проводимость электричества и тепла

Металлы обладают высокой проводимостью электричества и тепла благодаря особенностям их металлической связи. В металлической связи электроны в валентной зоне свободно перемещаются по кристаллической решетке металла, что позволяет металлу легко проводить электрический ток.
Проводимость электричества в металлах обусловлена высокой подвижностью электронов, которые в металлах находятся в общем электронном облаке, не принадлежащем к тому или иному атому. Такое общее облако электронов позволяет электронам свободно перемещаться внутри металла под воздействием электрического поля. Именно благодаря этой свободе перемещения электронов, металлы могут легко проводить электрический ток.
Теплопроводность металлов также связана с их металлической структурой и свободным перемещением электронов. Под воздействием разности температур, электроны перемещаются от области более высокой температуры к области более низкой температуры, передавая тепло другим электронам и атомам. В результате, металлы могут эффективно передавать тепло и обладают высокой теплопроводностью.
Пластичность и прочность металлов

Пластичность и прочность являются важными свойствами металлов, определяющими их способность выдерживать нагрузки и деформации.
Пластичность – это способность материала изменять форму без разрушения. Металлы обладают высокой пластичностью, что делает их идеальными материалами для производства различных конструкций и изделий.
Причина пластичности металлов заключается в особенностях их атомной структуры. В металлах атомы расположены рядами и связаны между собой электростатическими силами. При деформации металла, атомы сдвигаются, сохраняя свою связь и образуя новые контакты. Этот процесс называется скольжением атомов.
Прочность – это способность материала сопротивляться разрушению под действием внешних нагрузок. Металлы обладают высокой прочностью, благодаря своей кристаллической структуре и способности атомов связываться друг с другом.
Прочность металлов определяется несколькими факторами, такими как тип и количество примесей, способ изготовления материала и его термическая обработка.
Объяснение особенностей металлической связи

Металлическая связь - это уникальный тип химической связи, присущий только металлам. Она обусловлена особым строением атомов металла и их взаимодействием друг с другом. Главными особенностями металлической связи являются высокая проводимость электричества и тепла, а также металлический блеск и характерная форма кристаллов металлов.
Представьте себе, что атомы металла - это положительные ионы, расположенные в кристаллической решетке. Вокруг каждого иона металла находятся свободные электроны, которые образуют электронное облако. В результате сильного взаимодействия между положительно заряженными ионами и свободными электронами, металлы приобретают свои характерные свойства.
Электроны в металле могут свободно передвигаться по всей его структуре, что обеспечивает высокую проводимость электричества и тепла. Кроме того, металлы обладают металлическим блеском из-за способности свободных электронов поглощать и испускать световые кванты при прохождении электромагнитных волн.
Структура металла также влияет на его пластичность и прочность. Благодаря движению свободных электронов между ионами, металлы могут быть формованы и изгибаться без разрушения своей структуры. Кристаллическая решетка в металле также способствует высокой термической и механической стабильности.
Все эти особенности объясняются металлической связью - взаимодействием между положительно заряженными ионами и свободными электронами. Эта особая связь отличает металлы от других химических элементов и позволяет им обладать уникальными физическими и химическими свойствами.
Вопрос-ответ

Какие свойства обладают металлы?
Металлы обладают рядом характерных свойств, таких как высокая теплопроводность, электропроводность, пластичность и блеск.
Почему металлы обладают высокой электропроводностью?
Высокая электропроводность металлов объясняется наличием свободных электронов в их структуре. Эти электроны могут свободно перемещаться по материалу, образуя электрический ток.
Каким образом металлы обладают пластичностью?
Пластичность металлов обусловлена наличием металлической связи, которая характеризуется свободным движением между атомами. Благодаря этому, металлы могут принимать различные формы без разрушения.
Почему металлы являются отличными теплопроводниками?
Металлы обладают высокой теплопроводностью из-за свободного перемещения электронов. Свободные электроны быстро передают тепловую энергию от одной частицы к другой, что обеспечивает эффективную теплопроводность.
Почему металлы блестят?
Блеск металлов связан с рассеянием света свободными электронами. Когда свет падает на поверхность металла, электроны начинают колебаться под его воздействием и излучают свет, создавая блеск.
