Металлы первой группы таблицы Менделеева включают такие элементы, как литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs). Они являются химическими элементами, характеризующимися своим металлическим блеском и высокой электропроводностью.
Одним из основных свойств металлов первой группы является их низкая плотность. Например, литий, который является наименее плотным металлом и первым элементом в этой группе, обладает плотностью всего 0,53 г/см³. Натрий, калий, рубидий и цезий также обладают низкой плотностью, что делает их легкими и податливыми для обработки.
Еще одним характерным свойством металлов первой группы является их низкая температура плавления. Например, металлы этой группы плавятся при относительно низких температурах: литий – при 180°C, натрий – при 98°C, калий – при 63°C, рубидий – при 39°C и цезий – при 28°C. Это делает их полезными в различных промышленных процессах, где требуется низкая температура плавления.
Кроме того, металлы первой группы обладают высокой реактивностью, особенно при контакте с водой. Например, при взаимодействии с водой литий и натрий очень быстро реагируют и выбрасываются горючим веществом. Однако, калий, рубидий и цезий реагируют менее интенсивно, но все равно способны возгораться при попадании воды.
Свойства металлов первой группы

Металлы первой группы таблицы Менделеева включают литий, натрий, калий, рубидий, цезий и франций. Это алкалинные металлы, которые обладают рядом характерных свойств.
1. Активность: Алкалинные металлы первой группы являются очень реактивными. Они легко реагируют с водой, выделяя водород, и с большинством неметаллических элементов.
2. Мягкость и низкая плотность: Металлы первой группы обладают мягкой текстурой и низкой плотностью. Например, литий – наимягчайший металл, который можно надрезать ножом.
3. Реакция с водой: Когда алкалинные металлы первой группы взаимодействуют с водой, они образуют гидроксиды и выделяются водородный газ. Реакция происходит более интенсивно с возрастанием атомного номера металла: от лития до цезия.
4. Теплопроводность и электропроводность: Металлы первой группы обладают высокой теплопроводностью и электропроводностью. Это связано с наличием свободных электронов в их кристаллической решетке.
5. Окислительные свойства: Алкалинные металлы первой группы имеют выраженные окислительные свойства. Они способны легко отдавать электроны и образовывать ионы с положительным зарядом.
6. Цвет и блеск: Алкалинные металлы первой группы имеют характерный металлический блеск. Некоторые из них, такие как натрий и калий, могут иметь ярко-серо-белый цвет.
В целом, свойства металлов первой группы делают их полезными и широко применяемыми в различных областях науки и промышленности.
Физические свойства металлов первой группы
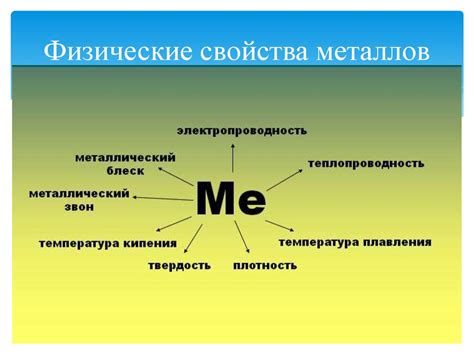
Металлы первой группы таблицы Менделеева обладают рядом характерных физических свойств, которые делают их уникальными и широко применяемыми в различных областях науки и промышленности.
Первым существенным свойством этих металлов является их благородный блеск, который наблюдается на поверхности образцов. Этот блеск делает металлы первой группы приятными на ощупь и привлекательными визуально. Блеск возникает из-за способности металлов отражать свет, что создает эффект металлического блеска.
Другим важным физическим свойством этих металлов является их высокая электропроводность. Металлы первой группы обладают свободными электронами, которые движутся по всему объему материала. Это делает их отличными проводниками электрического тока и позволяет использовать их в производстве электронных компонентов и электротехнических устройствах.
Также металлы первой группы характеризуются высокой теплопроводностью. Они способны быстро и эффективно передавать тепло, что делает их идеальными материалами для теплообмена в различных устройствах. Благодаря этому свойству, металлы первой группы широко используются в производстве радиаторов, теплообменников и других теплоотводящих элементов.
Наконец, металлы первой группы обладают высокой плотностью, что делает их тяжелыми и прочными материалами. Они способны выдерживать большие нагрузки без деформации и сохранять свою структуру при высоких температурах. Благодаря этим свойствам, металлы первой группы широко используются в строительстве, производстве автомобилей, самолетов и других транспортных средств.
Химические свойства металлов первой группы
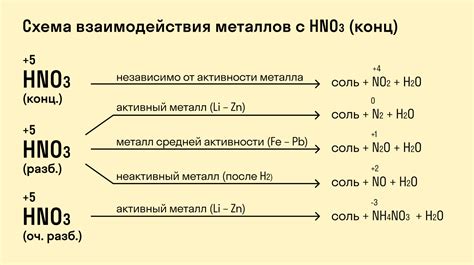
Металлы первой группы таблицы Менделеева включают такие элементы, как литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). У этих металлов есть ряд общих химических свойств.
Во-первых, металлы первой группы обладают низкой электроотрицательностью, что делает их хорошими ионными реагентами. Они образуют ионы, имеющие положительный заряд, легко отдают свои электроны и образуют оксиды, гидроксиды и соли с отрицательными ионами.
Во-вторых, металлы первой группы реагируют с водой. Процесс реакции с водой протекает очень интенсивно и с выделением большого количества энергии. При контакте с водой, металлы первой группы образуют гидроксиды и высвобождают водород. Данную реакцию легко наблюдать, так как вода начинает пениться и выделяется взрывоопасный газ.
В-третьих, металлы первой группы реагируют с кислотами. Они образуют соли металлов и высвобождают водородный газ. При этой реакции образуется адексхотическое выделение водорода.
В-четвертых, металлы первой группы обладают способностью образовывать соединения с кислородом. Они реагируют с кислородом воздуха и образуют оксиды металлов, которые часто выделяют ярко-насыщенные цвета.
В-пятых, металлы первой группы образуют соли с различными отрицательными ионами. Например, хлориды, бромиды, йодиды и фториды этих металлов образуются при реакции с соответствующими галогенами. Эти соли имеют разнообразные применения и широко используются в химической промышленности.
Таким образом, металлы первой группы таблицы Менделеева обладают уникальными химическими свойствами, которые делают их важными и широко применяемыми элементами в различных областях нашей жизни.
Некоторые промышленно важные свойства металлов первой группы
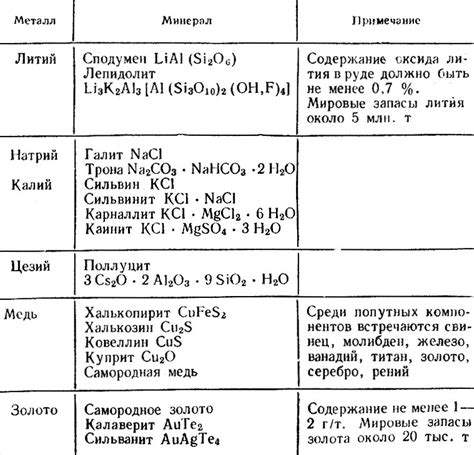
1. Химическая активность: Металлы первой группы, такие как литий, натрий, калий, обладают высокой химической активностью. Они с легкостью реагируют с кислородом, водой, кислотами и другими веществами. Это свойство делает их полезными в различных промышленных процессах.
2. Низкая плотность: Металлы первой группы обладают низкой плотностью, что делает их легкими и удобными для использования в различных приложениях. Например, литий используется в легких аккумуляторах, а натрий и калий - в производстве различных сплавов.
3. Высокая электропроводность: Металлы первой группы являются отличными проводниками электричества. Они обладают высокой электропроводностью и используются в электротехнике и электронике для создания проводов, контактов и других электрических компонентов.
4. Источники энергии: Металлы первой группы широко используются в производстве батареек и аккумуляторов. Литий-ионные аккумуляторы, содержащие литий, натрий или калий, обеспечивают надежный и долговечный источник энергии для многих устройств, включая мобильные телефоны и электромобили.
5. Фотокаталитическая активность: Некоторые металлы первой группы, в частности, дрожжевой металл (калий), обладают фотокаталитической активностью. Это свойство позволяет использовать их в солнечных панелях и процессах фотохимической конверсии энергии.
Реактивность и взаимодействие металлов первой группы с другими веществами
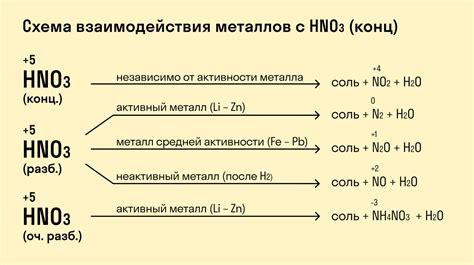
Металлы первой группы таблицы Менделеева (литий, натрий, калий, рубидий и цезий) являются самыми реактивными металлами из всех элементов. Они легко взаимодействуют с другими веществами, что объясняется наличием одной валентной электронной оболочки и низкой энергией ионизации.
Эти металлы активно реагируют с водой, образуя щелочные гидроксиды и выделяя водород. Например, литий реагирует с водой очень интенсивно, выделяя пламя, а натрий шипит и движется по поверхности воды.
Кроме того, металлы первой группы реагируют с кислородом, жидкими аммиаком и хлоридами металлов. Они также обладают способностью образовывать сплавы с другими металлами.
Реактивность этих металлов возрастает от лития к цезию. Например, цезий реагирует с водой еще интенсивнее, чем литий, и может при этом даже вызвать взрыв.
Взаимодействие металлов первой группы с другими веществами подтверждает их химическую активность и ставит их ведущими элементами во многих химических процессах.
Вопрос-ответ

Какие свойства характерны для металлов первой группы таблицы Менделеева?
Металлы первой группы таблицы Менделеева обладают рядом характерных свойств. Их атомы обычно имеют одну электронную оболочку, которая состоит из одного электрона. В связи с этим, металлы первой группы обладают малым энергетическим уровнем валентной оболочки, что делает их очень реакционноспособными. Они активно вступают в химические реакции, особенно с водой и кислородом. Кроме того, металлы первой группы хорошо проводят электричество и тепло, имеют металлический блеск, обладают низкими плотностью и температурой плавления.
Какие элементы относятся к металлам первой группы в таблице Менделеева?
К металлам первой группы таблицы Менделеева относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Все эти элементы имеют одну электронную оболочку с одним электроном в валентной области. Они являются щелочными металлами и образуют ионы с положительным зарядом, легко вступая в реакции с другими элементами.
Каковы особенности реактивности металлов первой группы таблицы Менделеева?
Металлы первой группы таблицы Менделеева обладают высокой реакционной способностью из-за наличия одного электрона в валентной области. Этот электрон слабо привязан к ядру и легко отделяется, что способствует активному вступлению металлов в реакции. Они реагируют с водой, кислородом и многими другими веществами. Например, щелочные металлы (натрий, калий) быстро реагируют с водой, выделяя водород и образуя оксиды.
