Оксиды металлов – это соединения химических элементов, в которых металл образует положительный ион, а кислород – отрицательный. Оксиды металлов представляют собой широкий класс соединений, которые обладают различными физическими и химическими свойствами. В зависимости от своих характеристик, оксиды металлов находят широкое применение в различных отраслях промышленности и научных исследованиях.
Одно из основных свойств оксидов металлов – это их электропроводность. Многие оксиды металлов являются полупроводниками или даже проводниками электричества. Это обусловлено наличием свободных электронов в структуре оксида, которые могут двигаться под воздействием электрического поля. Благодаря этому свойству оксиды металлов находят применение в производстве электроники, солнечных батарей, термоэлектрических преобразователей и других устройств.
Кроме того, оксиды металлов обладают высокой устойчивостью к теплу и химическим воздействиям. Они являются стойкими к высоким температурам и агрессивным средам, что позволяет использовать их в производстве керамики, огнеупорных материалов, эмали, катализаторов и других материалов, которые должны выдерживать экстремальные условия.
Важно отметить, что оксиды металлов имеют различные цвета, что позволяет использовать их в качестве пигментов и красителей. Например, оксид железа Fe2O3 является основным составом красок и пигментов красного и желтого цветов. Оксид кобальта Co3O4 используется в производстве синего и розового красителей.
Использование оксидов металлов в промышленности и научных исследованиях является важным направлением развития современных технологий. Они находят применение в производстве электроники, керамики, красителей, катализаторов, солнечных батарей, эмалей и многих других изделий. Благодаря своим уникальным свойствам, оксиды металлов играют важную роль в современном обществе.
Свойства оксидов металлов
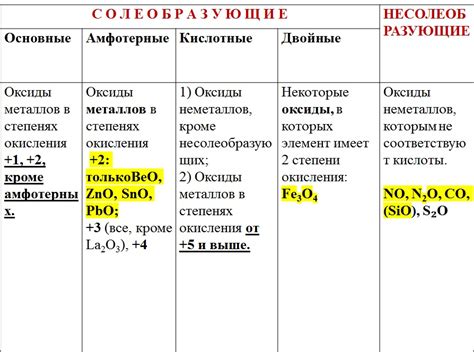
Оксиды металлов – это химические соединения, состоящие из кислорода и металлического элемента. Они обладают рядом особых свойств, которые делают их важными для различных приложений.
Первое свойство оксидов металлов – это их высокая термическая и химическая стабильность. Благодаря этому, они могут быть использованы в высокотемпературных процессах, таких как обжиг керамики или плавка стекла.
Оксиды металлов обладают также электрохимическими свойствами. Они могут быть использованы в качестве каталитических материалов в различных процессах, таких как конверсия энергии или очистка отходов. Кроме того, некоторые оксиды металлов имеют полупроводниковые свойства и используются в производстве электроники.
Оксиды металлов также обладают оптическими свойствами, такими как прозрачность или цветность. Например, оксид железа (Fe2O3) имеет красный цвет, что делает его полезным для производства красок и пигментов.
Важным свойством оксидов металлов является их способность реагировать с другими химическими соединениями. Они могут использоваться в процессах окисления и восстановления во многих отраслях промышленности, таких как металлургия или производство керамических материалов.
Таким образом, оксиды металлов обладают разнообразными и полезными свойствами, которые делают их важными материалами для множества промышленных и научных приложений.
Структура и состояние оксидов металлов
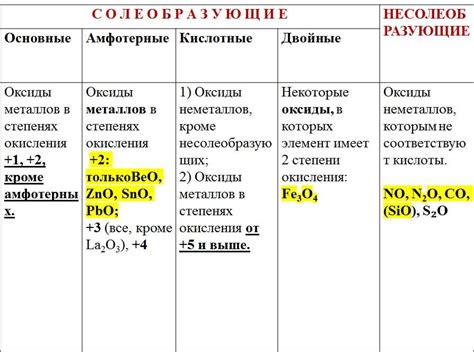
Оксиды металлов представляют собой химические соединения, состоящие из металла и кислорода. Они обладают различной структурой и состоянием в зависимости от своих физических и химических свойств.
Структура оксидов металлов может быть кристаллической или аморфной. Кристаллические оксиды образуют регулярную решетку, состоящую из атомов металла и атомов кислорода, с определенными межатомными расстояниями. Аморфные оксиды не имеют такой регулярной структуры и представляют собой аморфные твердые вещества.
Состояние оксидов металлов может быть различным: твердым, жидким или газообразным. Большинство оксидов металлов являются твердыми веществами, но есть и жидкие оксиды, например, хлориды кремния и титана. Также существуют газообразные оксиды, например, оксид углерода.
Состояние оксидов металлов зависит от их температуры и давления. Некоторые оксиды металлов при нормальных условиях являются газами, но могут конденсироваться при понижении температуры или повышении давления. Температура плавления и кипения оксидов металлов также различается и зависит от их структуры и химического состава.
Физические свойства оксидов металлов

Оксиды металлов – это соединения металлов с кислородом. Они обладают рядом физических свойств, которые определяют их поведение и применение.
Первое из основных физических свойств оксидов металлов – это их цвет. Оксиды металлов обычно имеют яркую окраску, которая определяется их химическим составом. Некоторые оксиды металлов могут иметь желтый, синий, красный или черный цвет.
Второе физическое свойство оксидов металлов – это их плотность. Оксиды металлов обычно имеют высокую плотность, что делает их тяжелыми и плотными соединениями. Плотность оксидов металлов может варьироваться в зависимости от конкретного металла и его сочетания с кислородом.
Третье физическое свойство оксидов металлов – это их твердость. Оксиды металлов обычно являются твердыми веществами, которые могут быть хрупкими или прочными. Твердость оксидов металлов зависит от структуры исходного металла, а также от особенностей его сочетания с кислородом.
Четвертое физическое свойство оксидов металлов – это их точка плавления. Оксиды металлов обычно обладают высокой точкой плавления, что делает их стабильными при высоких температурах. Точка плавления оксидов металлов может варьироваться в зависимости от конкретного металла и его сочетания с кислородом.
Физические свойства оксидов металлов играют важную роль в их применении. Например, оксиды металлов могут использоваться в производстве красителей, керамики, электроники, а также в медицине и других отраслях промышленности.
Химические свойства и применение оксидов металлов
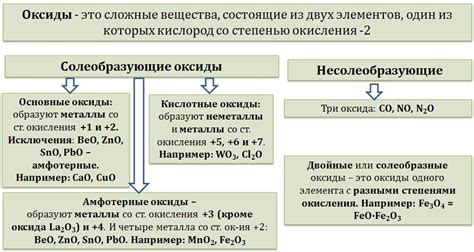
Оксиды металлов - это химические соединения, состоящие из металла и кислорода. Они образуются в результате окисления металлов и играют важную роль в различных сферах жизни.
Одним из ключевых свойств оксидов металлов является их кислотность или щелочность. Некоторые оксиды металлов обладают кислотными свойствами и реагируют с водой, образуя кислотные растворы. Такие оксиды называются кислотными оксидами. Например, оксид серы SO2 - кислотный оксид. Другие оксиды металлов проявляют щелочные свойства и при растворении в воде образуют щелочные растворы. Они называются щелочными оксидами. Например, оксид натрия Na2O - щелочной оксид.
Оксиды металлов широко применяются в разных отраслях. Например, оксид железа Fe2O3, известный как красная глина, используется в производстве строительных материалов и красок. Оксид алюминия Al2O3, известный как алюминий, используется в производстве алюминиевой фольги, конструкций и электроники. Оксид цинка ZnO широко применяется в производстве косметики, солнцезащитных средств и лекарственных препаратов. Оксид кальция CaO, известный как известь, используется в строительстве и сельском хозяйстве.
Кроме того, оксиды металлов используются в качестве катализаторов, в процессах сжигания и очистки отходов, а также в производстве электроэнергии. Например, оксид меди CuO используется в производстве катализаторов для химических реакций, а оксиды ртути HgO и цинка ZnO используются в батарейках.
Вопрос-ответ

Какие свойства имеют оксиды металлов?
Оксиды металлов обладают несколькими основными свойствами. Во-первых, они являются твердыми веществами при комнатной температуре и обычно имеют высокую температуру плавления. Во-вторых, они обладают высокой электропроводностью в расплавленном или растворенном состоянии, но не проводят электричество в твердом состоянии. В-третьих, они имеют кислый, щелочной или нейтральный характер и могут образовывать соли в реакции с кислотами или щелочами.
Какие металлы образуют оксиды?
Оксиды образуются практически со всеми металлами. Некоторые из самых распространенных оксидов металлов включают оксиды алюминия, железа, магния, кальция, натрия и калия. Однако практически все металлы могут образовывать оксиды в различных стехиометрических соотношениях.
Какие применения имеют оксиды металлов?
Оксиды металлов имеют множество применений в различных областях. Некоторые из них используются в качестве катализаторов в химических реакциях, другие служат в качестве пигментов для красок и керамики, а некоторые оксиды металлов используются в производстве стекла и стекловолокна. Кроме того, оксиды металлов находят широкое применение в электронике и полупроводниковой промышленности.
Как оксиды металлов влияют на окружающую среду?
Оксиды металлов могут иметь как положительное, так и отрицательное воздействие на окружающую среду. Некоторые оксиды металлов, такие как оксиды железа и алюминия, являются естественными компонентами почвы и воды и не представляют опасности для окружающей среды. Однако некоторые оксиды металлов, такие как оксиды свинца и ртути, являются токсичными и могут негативно сказываться на здоровье людей и животных.
