Коррозия металлов - это процесс разрушения материала под воздействием окружающей среды. Коррозия может привести к значительному ухудшению свойств и срока службы металлических изделий, поэтому разработка методов защиты от коррозии является актуальной задачей в современной инженерной практике.
Один из основных методов защиты металлов от коррозии - использование химических реакций. Они позволяют изменить условия окружающей среды или металла таким образом, чтобы уменьшить или полностью исключить разрушительное воздействие коррозии.
Одним из наиболее распространенных методов защиты металлов от коррозии является использование покрытий. Это процесс покрытия поверхности металла защитным слоем, который создается благодаря проведению ряда химических реакций. Как правило, покрытия создаются путем нанесения на поверхность металла специальных составов, содержащих вещества, способные реагировать с окружающей средой и образовывать стабильные соединения, которые предотвращают разрушительное действие коррозии. Таким образом, покрытие металла защитным слоем позволяет сохранить его свойства и продлить срок его службы.
Основные методы защиты металлов

Для защиты металлических изделий от коррозии существует несколько основных методов. Один из них – нанесение защитного покрытия. Чаще всего для этой цели используются лаки, эмали или пленки, которые наносятся на поверхность металла. Такие покрытия создают защитный барьер, не позволяющий влаге и воздуху взаимодействовать с металлом.
Ещё одним методом защиты металлов является гальваническая защита. Она основана на принципе спаривания металлов, с помощью которого происходит защита более активного металла за счет менее активного. В этом случае, менее активный металл выступает в качестве анода, который окисляется вместо активного металла, предотвращая его коррозию.
Ещё одним способом защиты металлов от коррозии является использование антикоррозионных добавок. Они вводятся в состав металлической поверхности, образуя пассивную пленку, которая предотвращает воздействие агрессивных сред. Данный метод особенно эффективен в случае эксплуатации металлов в условиях повышенной влажности или коррозионной среды.
Неотъемлемой частью защиты металлов от коррозии является катодная защита. Она основана на принципе электрохимического воздействия на металл. Защита осуществляется за счет подключения металлической поверхности к источнику тока, который уравновешивает реакции окисления и восстановления, предотвращая коррозию.
Химические реакции в борьбе с коррозией
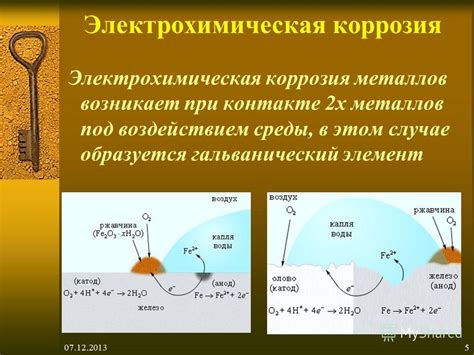
Коррозия является одной из основных проблем, с которой сталкиваются металлические конструкции. Она происходит в результате химической реакции между металлом и окружающей средой. В борьбе с коррозией широко применяются различные методы, основанные на химических реакциях.
Один из методов защиты от коррозии - покрытие металла слоем защитного материала. Для этого используются различные химические реакции. Например, нанесение покрытия из цинка на поверхность металла при помощи горячего цинкования. В результате реакции между цинком и металлом образуется защитный слой, который предотвращает контакт металла с окружающей средой.
Еще один метод защиты металлов от коррозии - использование антикоррозионных покрытий на основе оцинкованной стали. В этом случае происходит реакция между цинком и окружающей средой, при которой цинк растворяется, а металл остается неповрежденным. Таким образом, химические реакции обеспечивают защиту металла от коррозии.
Также существуют методы, основанные на химических реакциях, которые позволяют восстановить поврежденные металлические поверхности. Например, для удаления коррозионных отложений используется реакция с применением кислот. Кислота реагирует с коррозионным слоем и растворяет его, восстанавливая первоначальное состояние поверхности металла.
Таким образом, химические реакции играют ключевую роль в борьбе с коррозией металлов. Они позволяют предотвращать коррозию, создавать защитные слои и восстанавливать поврежденные поверхности. Правильный выбор методов защиты и применение соответствующих химических реакций позволяют продлить срок службы металлических конструкций и улучшить их эксплуатационные характеристики.
Реакция окисления для предотвращения коррозии
Коррозия металлов является одной из основных проблем при эксплуатации различных конструкций и механизмов. Одним из эффективных методов защиты металлов от коррозии является применение реакции окисления.
В процессе окисления металла образуется оксидная пленка, которая служит защитным барьером от агрессивного воздействия внешних факторов. Пленка оксида надежно закрывает поверхность металла и предотвращает проникновение кислорода и влаги, что способствует снижению скорости коррозии.
Реакция окисления широко применяется для защиты различных металлических изделий, включая конструкции из стали, алюминия, цинка и других металлов. В зависимости от условий эксплуатации и требований к защите, используются различные методы окисления, такие как горячее окисление, электрохимическое окисление и химическое окисление.
Преимуществами реакции окисления являются низкая стоимость и простота применения. Кроме того, окисленные поверхности обладают повышенной стойкостью к механическим повреждениям и атмосферному воздействию.
Однако, необходимо учитывать, что реакция окисления может привести к изменению внешнего вида и цвета металла. Поэтому перед применением метода окисления необходимо провести тщательное тестирование и выбрать оптимальные условия для достижения требуемого результата.
Электрохимическая защита от коррозии
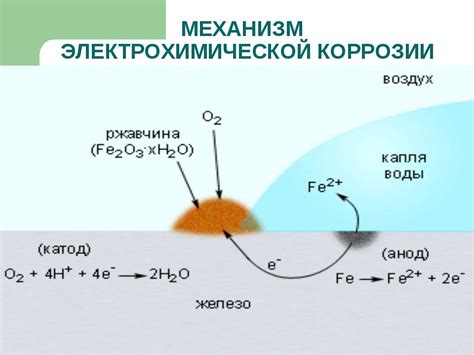
Электрохимическая защита от коррозии - это метод, основанный на использовании разности потенциалов между металлами, которые находятся в контакте с коррозионной средой. Основными методами этой защиты являются катодная и анодная защита.
Катодная защита заключается в том, что к металлическому изделию подключается электрический источник тока, который создает разность потенциалов с другим металлом, выступающим в роли анода. Таким образом, изделие становится катодом, а анод выполняет функцию жертвенного металла, который подвергается коррозии. Этот метод эффективен для защиты больших металлических конструкций, например, судов, трубопроводов и т.д.
Анодная защита, наоборот, заключается в использовании анода, который состоит из металла с большей реактивностью, чем металл защищаемого изделия. Анод подключается к источнику тока, и ток протекает от него к защищаемому изделию. За счет этого процесса металлическое изделие превращается в катод и становится защищенным от коррозии. Этот метод эффективен для защиты небольших металлических изделий, таких как детали автомобилей, электроники и т.д.
Оба метода электрохимической защиты требуют контроля и поддержания правильной разности потенциалов, что достигается регулировкой силы и напряжения источника тока. Это позволяет значительно снизить скорость коррозионного процесса и увеличить срок эксплуатации металлических изделий.
Вопрос-ответ

Какие методы защиты металлов от коррозии существуют?
Существует несколько методов защиты металлов от коррозии. Один из самых распространенных методов - нанесение защитного покрытия на поверхность металла. Защитные покрытия могут быть органическими (например, краской) или неорганическими (например, оксидами металла). Еще один метод - использование антикоррозионных пигментов, добавляемых в материалы, используемые для покрытия металла. Также существуют методы электрохимической защиты, такие как катодная защита и анодная защита.
Что такое катодная защита?
Катодная защита - это метод защиты металлов от коррозии, основанный на принципе электрохимической защиты. При катодной защите на металлическую поверхность подводится постоянный электрический ток, который принуждает металл вести себя как катод в электрохимической реакции, снижая скорость коррозии. Для проведения катодной защиты необходимо создать анодный и катодный режимы, используя специальные анодные материалы и источник постоянного тока.
Как происходит анодная защита металлов?
Анодная защита - это метод защиты металлов от коррозии, в котором за счет введения в среду ингибиторов или использования пассивирующих покрытий создается защитный слой на поверхности металла, который предотвращает контакт с коррозионно-активными факторами. В результате создается электрохимическая реакция, в которой металл ведет себя как анод, что препятствует коррозии. Анодная защита может быть реализована путем покрытия металла специальными анодными материалами или использованием химических веществ, которые позволяют создать пассивирующие покрытия на поверхности металла.
