Металлы активно используются в процессе восстановления азотной кислоты, которая является важным химическим соединением. В результате взаимодействия металлов с азотной кислотой образуются различные продукты, которые находят применение в различных отраслях промышленности и научных исследованиях.
Одним из основных продуктов восстановления азотной кислоты металлами является аммиак (NH3). Аммиак широко применяется в производстве удобрений, пищевой промышленности, химической промышленности и других отраслях. Он используется в качестве сырья для производства азотных удобрений, а также для получения различных органических и неорганических соединений.
Еще одним продуктом восстановления азотной кислоты металлами является нитрит (NO2), который используется в производстве различных пищевых добавок, консервантов и красителей. Нитрит также применяется в качестве окислителя в различных химических процессах и при производстве различных материалов.
Более сложным продуктом восстановления азотной кислоты металлами является азотная кислота (HNO3). Она применяется в процессе производства пластмасс, взрывчатых веществ, удобрений и других химических соединений. Азотная кислота также широко используется в лабораторных исследованиях, аналитической химии и других областях науки.
Почему важны продукты восстановления азотной кислоты металлами?

Продукты восстановления азотной кислоты металлами играют важную роль в различных промышленных процессах и научных исследованиях. Они обладают рядом уникальных свойств, которые делают их важными и эффективными в использовании.
Во-первых, продукты восстановления азотной кислоты металлами, такие как аммиак и гидразин, широко применяются в производстве удобрений. Азот является важным элементом для роста растений, и эти продукты позволяют обеспечить растения необходимыми питательными веществами.
Во-вторых, аммиак, получаемый в результате восстановления азотной кислоты металлами, является одним из основных сырьевых компонентов для синтеза различных химических соединений. Он используется для производства пластмасс, удобрений, взрывчатых веществ и многих других продуктов.
В-третьих, продукты восстановления азотной кислоты металлами используются в области водоочистки. Аммиак, полученный в результате восстановления азотной кислоты, может быть использован для удаления загрязнений из воды, таких как тяжелые металлы и органические соединения.
Также стоит отметить, что продукты восстановления азотной кислоты металлами могут быть использованы в научных исследованиях. Они могут служить исходным материалом для синтеза новых соединений или использоваться в процессе каталитических реакций. Важно отметить, что металлы, используемые для восстановления азотной кислоты, должны быть выбраны с учетом их химических свойств и степени реактивности, чтобы обеспечить эффективность и безопасность процесса восстановления и получения продуктов.
Таким образом, продукты восстановления азотной кислоты металлами являются важными в промышленности, сельском хозяйстве, научных исследованиях и других областях. Их уникальные свойства и широкий спектр применения делают их неотъемлемой частью современной жизни.
Какие металлы используются для восстановления азотной кислоты?
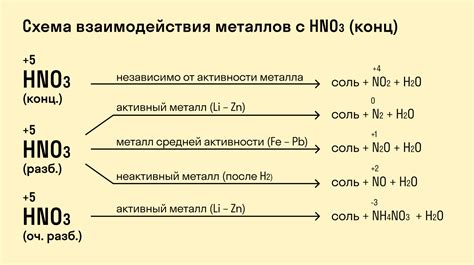
Восстановление азотной кислоты – это процесс, при котором атомы кислорода в нейтральных молекулах соединений с азотом замещаются атомами водорода. Для этого используют различные металлы, способные осуществлять реакцию восстановления.
Одним из наиболее распространенных металлов, используемых для восстановления азотной кислоты, является железо. Железо обладает высокой активностью и может служить эффективным восстановителем, особенно в присутствии каталитических веществ.
Кроме железа, для восстановления азотной кислоты также используются такие металлы, как алюминий, цинк и медь. Алюминий обладает высокими каталитическими свойствами и имеет хорошую активность в реакциях восстановления. Цинк, в свою очередь, находится в конце ряда активности металлов и хорошо восстанавливает азотную кислоту. Медь, хотя и менее активна, может быть использована в некоторых реакциях восстановления.
Выбор металла для восстановления азотной кислоты зависит от реакционных условий и требуемой эффективности процесса. Кроме того, важно учитывать стойкость и стоимость металла, а также его влияние на окружающую среду.
Восстановление азотной кислоты металлическим железом
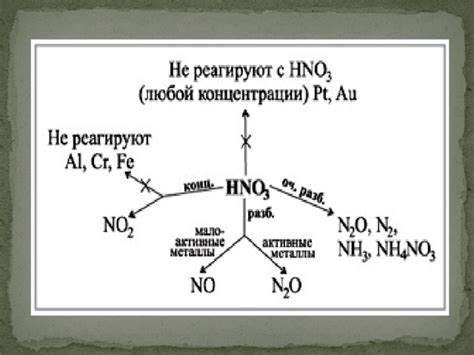
Азотная кислота (HNO3) – химическое соединение, широко используемое в промышленности и лабораторных работах. При реакции с металлами она может быть восстановлена, образуя различные продукты. Один из способов восстановления азотной кислоты – использование металлического железа.
Металлическое железо эффективно восстанавливает азотную кислоту, переходя в соединение, известное как азотнокислое железо, или железо(II)нитрат (Fe(NO3)2). При этой реакции выделяется обильное количество железных и азотных соединений, в том числе оксидов азота.
Процесс восстановления азотной кислоты металлическим железом активно применяется в промышленности для производства азотнокислого железа, которое затем используется в качестве удобрения. Это соединение содержит азот и железо, которые играют важную роль в росте растений.
В лаборатории восстановление азотной кислоты металлическим железом может проводиться для получения азота или других соединений. Данная реакция широко применяется при проведении экспериментов и исследований в области химии и физики, а также для получения необходимых продуктов.
Восстановление азотной кислоты медью

Восстановление азотной кислоты медью – это процесс, при котором медь служит восстановителем для превращения азотной кислоты в другие соединения. Этот процесс является одним из основных методов получения азотных продуктов, таких как аммиак и нитраты.
Восстановление азотной кислоты медью происходит в несколько этапов. Сначала медь окисляется до двухвалентного иона Cu2+, а азотная кислота вступает в реакцию с однонатриевой солью диспрозии. Образуется диспрозийхлорид, азотная кислота превращается в аммиак и воду, а медь восстанавливается до одновалентного иона Cu+.
Далее происходит реакция между аммиаком и кислородом, в результате которой образуется азотная кислота. Медь в этой реакции используется как катализатор. После этого азотная кислота может быть использована для получения различных азотных продуктов, таких как нитраты, которые имеют широкое применение в сельском хозяйстве и промышленности.
Восстановление азотной кислоты медью является важным процессом, который позволяет получать большие объемы азотных продуктов. Медь в данной реакции выполняет роль восстановителя и катализатора, что делает этот метод эффективным и экономически выгодным.
Восстановление азотной кислоты цинком
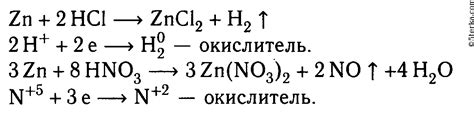
Азотная кислота, также известная как азотистая кислота, представляет собой химическое соединение, состоящее из атомов азота и кислорода. Она широко применяется в различных отраслях промышленности, включая производство удобрений, взрывчатых веществ, красителей и медицинских препаратов.
Цинк является одним из металлов, способных восстанавливать азотную кислоту. В процессе восстановления цинк вступает в реакцию с азотной кислотой, принимая на себя кислородные группы из кислоты и образуя оксид цинка, азотной оксид и воду. Реакция может быть описана следующим образом:
Zn + 2HNO3 → Zn(NO3)2 + H2O + 2NO
Восстановление азотной кислоты цинком осуществляется в присутствии катализатора, такого как хлористый цинк. Катализатор повышает скорость реакции, облегчая процесс восстановления и улучшая выход продуктов.
Применение цинка для восстановления азотной кислоты имеет ряд преимуществ. Во-первых, цинк является относительно недорогим и широко доступным металлом. Во-вторых, реакция восстановления азотной кислоты цинком является относительно безопасной и не требует использования опасных реагентов.
Однако, необходимо учитывать, что восстановление азотной кислоты цинком может привести к образованию нитритных и нитратных соединений, которые могут быть опасными для окружающей среды и здоровья человека. Поэтому при осуществлении данного процесса необходимо соблюдать все меры предосторожности и выполнять его в соответствии с регуляторными нормами и требованиями.
Научно-технические аспекты восстановления азотной кислоты металлами

Восстановление азотной кислоты металлами является важным процессом научно-технической сферы, в котором используются различные металлические соединения для преобразования азотной кислоты в другие соединения. Этот процесс является важной технологией в производстве удобрений, взрывчатых веществ, красителей и других химических продуктов.
Восстановление азотной кислоты металлами осуществляется при помощи процесса, известного как каталитическая аммиаковая синтез. В этом процессе металлы действуют как катализаторы, ускоряющие реакцию между азотной кислотой и водородом. Среди металлических соединений, широко используемых для восстановления азотной кислоты, можно назвать родий, платину, никель и другие.
Каталитическое восстановление азотной кислоты металлами имеет несколько преимуществ. Во-первых, этот метод более экономически эффективен, чем альтернативные способы восстановления. Во-вторых, использование металлов в этом процессе позволяет сохранить высокие показатели эффективности, что особенно важно при массовом производстве химических продуктов.
Научно-технические исследования в области восстановления азотной кислоты металлами направлены на поиск новых катализаторов, которые были бы более эффективными и устойчивыми. Ученые проводят эксперименты с различными металлами и их соединениями, а также исследуют влияние различных факторов, таких как температура, концентрация и давление, на каталитическую реакцию.
В целом, научно-технические аспекты восстановления азотной кислоты металлами являются важной областью исследований в химии и технологии. Разработка новых и улучшение существующих методов восстановления способствуют повышению эффективности производства химических продуктов и важны для достижения устойчивого развития.
Вопрос-ответ

Какие металлы можно использовать для восстановления азотной кислоты?
Для восстановления азотной кислоты можно использовать различные металлы, такие как железо, цинк, алюминий, медь и другие. Каждый металл имеет свои особенности и может использоваться в зависимости от конкретной задачи.
Какими продуктами образуется восстановление азотной кислоты металлами?
При восстановлении азотной кислоты металлами образуются различные продукты, включая аммиак (NH3), окислы азота (N2O, NO), нитриты, нитраты и другие соединения. Образование конкретного продукта зависит от условий реакции и используемого металла.
