Оксиды переходных металлов представляют собой вещества, содержащие по крайней мере один атом переходного металла и один атом кислорода. Эти соединения обладают различными свойствами и находят широкое применение в разных областях науки и промышленности.
Переходные металлы имеют переменное число степеней окисления, что позволяет им образовывать оксиды с разными химическими свойствами. Некоторые из них являются основными оксидами, что означает их способность образовывать основания при взаимодействии с водой. Например, оксид железа (III) (Fe2O3), оксид меди (I) (Cu2O) и оксид титана (IV) (TiO2) имеют базичные свойства и могут растворяться в воде, образуя гидроксиды металлов.
Основные оксиды переходных металлов находят применение в разных областях. Оксид железа (III), известный также как гематит, используется в производстве стали, красок, керамики и магнитных материалов. Оксид меди (I), или куприт, применяется в электронике, производстве стекла и керамики, а также в изготовлении пигментов для красок. Оксид титана (IV), или рутил, находит применение в солнечных батареях, косметике, лакокрасочных материалах и даже в пищевой промышленности.
Свойства основных оксидов переходных металлов

Основные оксиды переходных металлов обладают рядом характерных свойств, которые определяют их важность и широкое применение в различных областях науки и промышленности.
Во-первых, основные оксиды переходных металлов обладают высокой электроотрицательностью и способностью взаимодействовать с кислородом. Это позволяет им быть эффективными окислителями в химических реакциях.
Во-вторых, основные оксиды переходных металлов обладают высокой степенью термической и химической устойчивости. Они выдерживают высокие температуры и не разлагаются при взаимодействии с кислотами или щелочами. Это делает их незаменимыми в процессах обжига, горения и синтеза.
В-третьих, основные оксиды переходных металлов обладают специфическими физическими свойствами, такими как высокая проводимость электричества и тепла, магнитные свойства и способность к ферромагнетизму. Именно благодаря этим свойствам они находят применение в электронике, магнитных материалах и других сферах науки и техники.
Кроме того, основные оксиды переходных металлов обладают специфическими каталитическими свойствами. Они способны активировать реакции, ускоряя их ход и делая их более эффективными. Это позволяет использовать эти оксиды в качестве катализаторов в промышленном производстве различных химических веществ.
Таким образом, свойства основных оксидов переходных металлов определяют их важность и широкое применение в различных областях науки и промышленности, от химии до электроники и магнетизма.
Применение основных оксидов переходных металлов
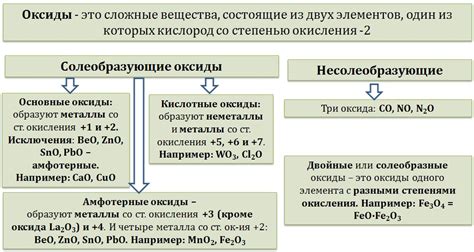
Основные оксиды переходных металлов являются важными компонентами в различных областях науки и техники, благодаря своим уникальным свойствам и широкому спектру применения.
Оксид железа (FeO) используется в производстве стекла, керамики и магнитных материалов. Он также является важным компонентом в процессе производства стали, где служит как восстановитель и катализатор.
Оксид хрома (Cr2O3), известный также как зеленое касситеритовое пигментное вещество, применяется в производстве красок, эмалей, стекла и керамики. Оксид хрома также используется в катализаторах и в производстве лекарственных препаратов.
Оксид меди (CuO) широко используется в электротехнике и электронике, в производстве полупроводников, солнечных батарей, электрических контактов и проводников. Оксид меди также применяется в катализаторах и в производстве стекла и керамики.
Оксид цинка (ZnO) является важным компонентом в производстве лакокрасочных материалов, резин, пластмасс и косметических продуктов. Он также используется в производстве лекарственных препаратов, катализаторов, солнечных батарей и электронных устройств.
Оксид титана (TiO2) имеет широкое применение в производстве красок, эмалей, пигментов, солнечных батарей, косметики и лекарственных препаратов. Оксид титана также используется в сфере медицины, в производстве катализаторов и высокотемпературных материалов.
Оксид никеля (NiO) применяется в производстве катализаторов, керамики, стекла и электроники. Оксид никеля также используется в химической промышленности, при производстве лекарственных препаратов и аккумуляторов.
Таким образом, основные оксиды переходных металлов нашли широкое применение в различных отраслях промышленности, науки и медицины благодаря своим полезным свойствам и уникальной химической активности.
Оксиды как каталитические соединения

Оксиды переходных металлов широко используются в качестве каталитических соединений. Катализаторы на основе оксидов переходных металлов играют важную роль в промышленных процессах, таких как производство пластиков, нефтехимическая и фармацевтическая промышленность.
Оксиды переходных металлов обладают высокой активностью и выборочностью в каталитических реакциях. Они могут служить каталитическими центрами, активно участвуя в реакциях окисления, гидрирования, дегидрирования и других процессах.
Катализаторы на основе оксидов переходных металлов обычно имеют высокую поверхностную активность, что позволяет им эффективно взаимодействовать с реагентами, ускоряя химические реакции. Это позволяет снизить энергию активации и повысить производительность процесса.
Кроме того, оксиды переходных металлов часто используются в качестве носителя для других активных катализаторов. Использование таких композитов позволяет улучшить стабильность и селективность катализатора, а также увеличить его долговечность.
В целом, использование оксидов переходных металлов в качестве каталитических соединений играет ключевую роль в промышленных процессах и способствует эффективной и экономичной реализации различных химических реакций.
Роль основных оксидов в химических процессах
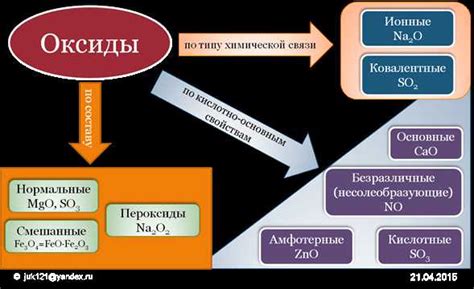
Основные оксиды переходных металлов играют важную роль во многих химических процессах. Они обладают высокой реакционной способностью и широким спектром применения.
Во-первых, основные оксиды используются в качестве катализаторов при промышленных процессах. Они способны активировать реагенты и ускорять химические реакции, что позволяет снизить энергию активации и повысить производительность процесса.
Во-вторых, основные оксиды служат источником переходных металлов для получения различных соединений. Многие переходные металлы имеют каталитические свойства, и их соединения используются в производстве пластмасс, лекарственных препаратов, красителей и других продуктов.
Кроме того, основные оксиды переходных металлов активно применяются для получения электрической энергии в гальванических элементах и аккумуляторах. Они являются одной из основных составляющих электродов и позволяют конвертировать химическую энергию в электрическую.
Необходимо отметить, что некоторые основные оксиды переходных металлов также имеют важное применение в качестве пигментов в производстве красок и покрытий. Они придают материалам желаемый цвет и обладают хорошей стойкостью к воздействию внешних факторов.
Вопрос-ответ

Что такое оксиды переходных металлов?
Оксиды переходных металлов - это химические соединения, состоящие из атомов кислорода и атомов переходных металлов. Они обладают различными свойствами и широко используются в различных областях, таких как катализ, электрохимия и материаловедение.
Какие свойства имеют основные оксиды переходных металлов?
Основные оксиды переходных металлов обладают следующими свойствами: они имеют щелочную реакцию, т.е. растворяются в воде и образуют щелочные растворы; они обладают высокой электропроводностью и могут быть использованы в электрохимических устройствах; они образуют стойкие соединения с кислородом и другими элементами, что позволяет использовать их в процессах окисления и восстановления.
В каких областях применяются основные оксиды переходных металлов?
Основные оксиды переходных металлов широко применяются в различных областях. Например, они используются в катализаторах для ускорения химических реакций. Также они находят применение в электрохимических устройствах, таких как аккумуляторы и топливные элементы. Основные оксиды переходных металлов также используются в материаловедении, например, для создания специальных покрытий, обладающих определенными свойствами.
