Оксиды — это химические соединения, состоящие из кислорода и одной или нескольких других химических элементов. В зависимости от химической природы элемента, оксиды могут обладать различными свойствами и играть разные роли в химических реакциях.
Одной из важных ролей оксидов является их участие в образовании оснований. Основания — это химические соединения, которые обладают способностью взаимодействовать с кислотами и образовывать соли и воду. Именно оксиды служат основой для образования оснований, так как они содержат кислород и могут отдавать его при реакции с водой.
Связь между оксидами и образованием оснований обусловлена способностью оксидов реагировать с водой и образовывать щелочные растворы. При контакте с водой, оксиды проявляют свою основную природу, образуя щелочные растворы и водяные растворы оснований. Это объясняется тем, что оксиды с кислородом обладают способностью принять протоны от воды, что приводит к образованию гидроксидов — оснований.
Основные оксиды и их роль в образовании оснований
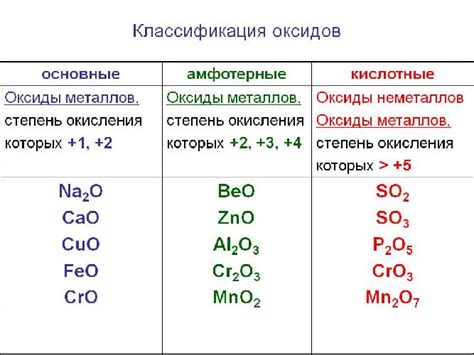
Основные оксиды – это химические соединения, образующиеся при соединении металлов с кислородом. Они обладают выраженной щелочностью и могут образовывать основания при реакции с водой или кислотами.
Важнейшая роль основных оксидов в образовании оснований связана с их способностью давать гидроксиды. При контакте с водой основные оксиды реагируют, образуя гидроксид металла и выделяя воду. Например, оксид натрия (Na2O) с водой образует гидроксид натрия (NaOH).
Основные оксиды также могут образовывать основания при взаимодействии с кислотами. При реакции основного оксида с кислотой, происходит образование соли и воды. Например, оксид кальция (CaO) с соляной кислотой (HCl) образует хлорид кальция и воду.
Важно отметить, что свойства основных оксидов и их способность образовывать основания зависят от металла, с которым они соединены. Различные металлы могут образовывать разные основные оксиды и, соответственно, разные основания. Например, оксид калия (K2O) образует гидроксид калия (KOH), а оксид кальция (CaO) образует гидроксид кальция (Ca(OH)2).
Таким образом, основные оксиды активно взаимодействуют с водой и кислотами, образуя основания. Это делает их важными компонентами в химических реакциях, а также в процессах, связанных с образованием и использованием оснований.
Основные оксиды: определение и свойства

Основные оксиды – это неорганические химические соединения, которые образуются при соединении металла с кислородом. Они обладают рядом характерных свойств, которые определяют их основные функции и роль в химических реакциях.
Одним из ключевых свойств основных оксидов является их способность реагировать с водой, образуя основания. Это происходит при контакте с влагой или водяными растворами и сопровождается выделением тепла. Такая реакция называется гидратацией или гидролизом. После гидратации оксид превращается в основание, которое обладает щелочными свойствами, способными нейтрализовать кислоты.
Основные оксиды также обладают высокой щелочностью и могут вступать в реакции непосредственно с кислотами. При контакте с кислотным раствором происходит нейтрализация, при которой оксид и кислота образуют соль и воду. Данный процесс называется щелочной нейтрализацией и является одним из способов использования основных оксидов в промышленности и химической лаборатории.
Степень щелочности основных оксидов зависит от их химического состава и пропорций. Например, натриевый оксид (Na2O) проявляет сильные щелочные свойства, в то время как магниевый оксид (MgO) является слабым основанием. Также основные оксиды могут выступать в роли амфотерных соединений и реагировать как с кислотами, так и с основаниями в зависимости от условий реакции.
Взаимодействие основных оксидов с водой

Основные оксиды, также известные как неферзные оксиды, являются соединениями металлов с кислородом. При контакте с водой они могут реагировать, образуя основания. Этот процесс называется гидратацией основных оксидов.
При гидратации основного оксида вода проникает в его структуру и ионы гидроксила (OH-) образуются. Эти ионы придают раствору щелочные свойства. Гидратация также сопровождается выделением тепла, что означает, что реакция экзотермическая.
Взаимодействие основных оксидов с водой может быть представлено следующим образом:
- Натриевый оксид (Na2O) + H2O → 2NaOH
- Калиевый оксид (K2O) + H2O → 2KOH
- Железо(III) оксид (Fe2O3) + 3H2O → 2Fe(OH)3
Образовавшиеся основания могут быть использованы в различных областях, таких как производство мыла, очистка сточных вод и в медицине. Они также используются в процессах нейтрализации кислот, так как основания реагируют с кислотами, образуя соль и воду.
Образование гидроксидов при взаимодействии основных оксидов с водой

Основные оксиды представляют собой химические соединения, состоящие из металла и кислорода. Когда эти оксиды взаимодействуют с водой, происходит образование гидроксидов - основных соединений, способных образовывать растворы с щелочной реакцией.
Вода, являясь слабым электролитом, диссоциирует на ионы водорода и гидроксидные ионы. При взаимодействии основных оксидов с водой, происходит гидратация основного оксида, что приводит к образованию гидроксидов. Гидратация представляет собой реакцию, в результате которой к основному оксиду присоединяются молекулы воды.
Образование гидроксидов при взаимодействии основных оксидов с водой осуществляется по следующей схеме:
- Основные оксиды вступают в реакцию с молекулами воды;
- Молекулы воды гидратируют основной оксид;
- В результате гидратации образуется гидроксид металла и высвобождаются гидроксидные ионы;
- Гидроксидные ионы диссоциируют в растворе, образуя щелочную среду.
Примером реакции образования гидроксида при взаимодействии основного оксида с водой может служить реакция образования гидроксида кальция (Ca(OH)2) при взаимодействии кальция с водой. В результате данной реакции образуется гидроксид кальция и высвобождаются гидроксидные ионы, придающие раствору щелочную реакцию.
Виды оснований, образующихся при реакции основных оксидов с водой
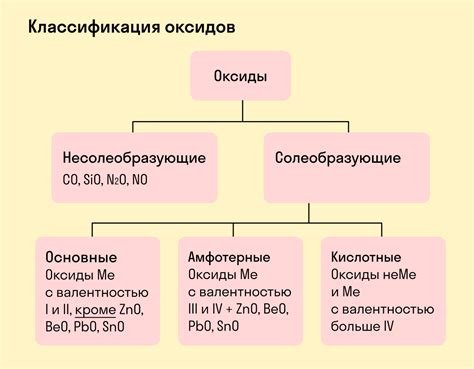
Основные оксиды - это соединения, образующиеся при соединении металла с кислородом. При контакте основных оксидов с водой происходит химическая реакция, в результате которой образуются основания. В зависимости от свойств основных оксидов и условий реакции, могут образовываться различные виды оснований.
Одним из наиболее распространенных видов оснований являются гидроксиды. Гидроксиды формируются при реакции основного оксида с водой, когда кислородная группа оксида заменяется гидроксильной группой. Например, реакция между натриевым оксидом и водой приводит к образованию натриевого гидроксида (NaOH), который широко применяется в промышленности.
Кроме гидроксидов, могут образовываться амиды - основания, содержащие азотную группу. Обычно амиды получаются при взаимодействии оксидов металлов с водой. Например, реакция алюминия с водой приводит к образованию алюминиевого амидида (Al(NH2)3). Амиды часто используются как катализаторы в органическом синтезе.
Также при взаимодействии основных оксидов с водой могут образовываться и другие виды оснований, включая гидразиды, гидрокарбонаты и другие соединения. Реакция между основными оксидами и водой является важным способом получения различных оснований, которые широко применяются в различных отраслях промышленности и научных исследованиях.
Примеры применения основных оксидов и образования оснований в промышленности и повседневной жизни
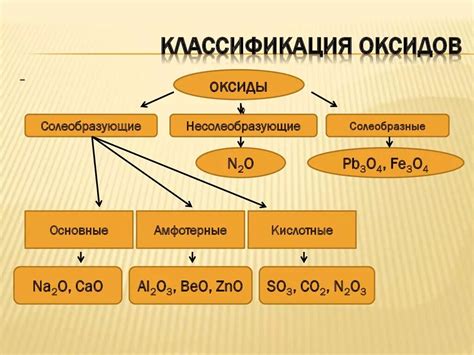
1. Производство щелочей и дезинфицирующих средств: Одним из примеров применения основных оксидов в промышленности является производство щелочей и дезинфицирующих средств. Натрий и калий являются основными элементами, которые могут образовывать оксиды и основания. Так, натрий образует оксид натрия (Na2O), который при реакции с водой образует щелочь натряшку (NaOH). Данная щелочь широко используется в бытовых и промышленных целях, например, в производстве мыла и моющих средств, очистке сточных вод, а также в процессе дезинфекции.
2. Производство стекла: Еще одним примером применения основных оксидов является производство стекла. Кремний, алюминий и кальций являются основными компонентами оксидов, которые при нагревании и плавлении образуют стекло. Например, оксид кремния (SiO2) является основным компонентом песчаника, который при плавлении превращается в кремниевое стекло. Стекло широко используется в повседневной жизни, например, в производстве окон, зеркал, посуды, упаковки и других изделий.
3. Производство удобрений: Основные оксиды также применяются в производстве удобрений. Фосфор и калий являются основными элементами, которые входят в состав фосфатных и калийных удобрений. Например, оксид фосфора (P2O5) может образовывать фосфаты, которые являются важными компонентами удобрений. Фосфаты и калийные соединения применяются для повышения плодородия почвы и увеличения урожайности растений.
4. Нейтрализация кислот: Основные оксиды и основания также применяются для нейтрализации кислот. Когда реагируют кислоты и основания, происходит процесс нейтрализации, при котором образуются соль и вода. Например, оксид кальция (CaO) является одним из основных компонентов извести, который используется для нейтрализации кислотных почв или отвода кислотных отходов в промышленности. Такой процесс нейтрализации обеспечивает поддержание оптимального pH-уровня и способствует улучшению качества почвы или очистке отходных вод.
Таким образом, применение основных оксидов и образование оснований в промышленности и повседневной жизни является неотъемлемой частью множества процессов и производств. Они играют важную роль в производстве щелочей и дезинфицирующих средств, производстве стекла, производстве удобрений и нейтрализации кислот. Эти процессы исключительно важны для обеспечения комфорта и эффективности в повседневной жизни, а также для развития промышленности и сельского хозяйства.
Вопрос-ответ

Что такое основные оксиды?
Основные оксиды - это неорганические вещества, состоящие из кислорода и металла. Они проявляют основные свойства и образуют основания при реакции с водой.
Какие основные оксиды существуют?
Существует множество основных оксидов, например, оксид натрия (Na2O), оксид калия (K2O), оксид кальция (CaO) и многие другие.
Как происходит образование оснований из основных оксидов?
При реакции основных оксидов с водой образуются основания. Основной оксид реагирует с молекулой воды, происходит образование оксида самого металла и образование основания.
Какие свойства имеют основные оксиды?
Основные оксиды проявляют основные свойства. Они способны нейтрализовывать кислоты, образуя соль и воду. Они также могут растворяться в воде, образуя растворы с щелочной реакцией.
Зачем нужны основные оксиды и основания?
Основные оксиды и основания широко используются в различных сферах. Они служат для получения солей, используются в процессе нейтрализации кислот, а также в производстве различных химических соединений.
