Основания - это вещества, которые обладают способностью принимать протоны (H+) и образовывать гидроксидные ионы (OH-) в растворе. Роль оснований в химических реакциях очень важна, так как они являются одной из трех основных типов реагентов, вместе с кислотами и солями.
Основания могут быть классифицированы на основании роли, которую играют катионы водорода и металлы, а также анионы. Катионы водорода имеют способность принимать протоны от кислот и образовывать воду. Они обычно представлены соответствующими ионами металлов, которые обладают основными свойствами. Примерами катионов водорода являются гидроксидные ионы (OH-) и аммониевые ионы (NH4+).
Металлические основания играют важную роль в протолитических реакциях, так как они образуют гидроксиды, которые являются наиболее распространенными типами оснований. Гидроксиды металлов образуются в результате реакции металла с водой. Именно гидроксидные ионы дают основаниям свойство образовывать гидроксидные ионы (OH-) и принимать протоны.
Анионы, в свою очередь, играют важную роль в свойствах оснований. Они могут быть представлены различными группами элементов, такими как оксиды (O2-), карбонаты (CO3^2-), гидрокарбонаты (HCO3-), фенидаты (F-) и другие. Анионы имеют способность принимать протоны от кислот и образовывать основные соединения.
Свойства оснований зависят от комбинации катионов водорода, металлов и анионов, которые являются их составляющими. Это позволяет основаниям обладать различными химическими и физическими свойствами, а также использоваться в различных областях, таких как промышленность, медицина и научные исследования.
Влияние катионов водорода на свойства оснований

Катионы водорода являются одним из важных факторов, влияющих на свойства оснований. Наличие катионов H+ в растворе изменяет pH, уровень концентрации гидроксидных ионов и, следовательно, их щелочность. Чем больше концентрация катионов водорода, тем кислее будет реакция и тем меньше щелочности будет проявлять основание.
Кроме того, катионы водорода могут влиять на скорость и механизм реакции между основанием и кислотой. Катион H+ может совместно с анионом OH- образовывать молекулы воды, что влияет на скорость реакции основания и кислоты. Например, в реакции нейтрализации катион водорода Н+ и анион гидроксида OH- образуют воду H2O, что способствует ее образованию в большем количестве.
Кроме того, наличие катионов водорода может влиять на растворимость оснований. Если катион H+ является сильнейшей кислотой, чем катион металла М+, основание может раствориться в кислоте. Это связано с сильным взаимодействием катиона металла М+ с анионом гидроксида OH-, что приводит к образованию растворимого комплексного иона.
Таким образом, катионы водорода играют важную роль в определении свойств оснований. Их присутствие влияет на pH, концентрацию гидроксидных ионов, скорость и механизм реакций с кислотами, а также на растворимость оснований.
Роль металлических катионов в свойствах оснований
Металлические катионы играют важную роль в свойствах оснований. Они являются положительно заряженными ионами, которые образуются в результате потери одного или нескольких электронов металлом. Катионы водорода и многих металлов схожи по своему действию на основания и их свойства.
Катионы водорода являются составной частью многих оснований и определяют их pH-значение. Они образуют ионные связи с анионами, обладающими отрицательной зарядом. Некоторые из оснований, содержащих катионы водорода, можно найти в бытовых средствах, таких как щелочные моющие средства или мочевина.
Металлические катионы, такие как катионы щелочных и щелочноземельных металлов, также играют важную роль в свойствах оснований. Они имеют большую электроотрицательность и способны эффективно принимать электроны от анионов. Это делает основания с металлическими катионами сильными, обладающими высокими щелочными свойствами.
Металлические катионы также влияют на растворимость оснований и их реактивность. Некоторые металлические катионы могут образовывать осадки или растворяться в воде с образованием гидроксидов, что влияет на их использование в различных областях, таких как промышленность и медицина.
Таким образом, металлические катионы играют важную роль в свойствах оснований, определяя их pH-значение, реактивность и растворимость. Их наличие в основаниях обуславливает их способность взаимодействовать с кислотами и регулировать различные химические процессы.
Анионы и их влияние на основания

В химии основания представляют собой вещества, которые могут принимать на себя протоны (или катионы водорода) и образовывать гидроксиды. Однако, помимо катионов водорода, на основания может оказывать влияние и тип анионов, присутствующих в соединении.
Некоторые анионы могут усиливать свойства оснований, делая их более реактивными и способными принимать протоны. Например, анионы таких элементов, как гидроксид (OH-), оксид (O2-), карбонат (CO32-) и гидрокарбонат (HCO3-), могут значительно увеличивать щелочность основания.
Однако, не все анионы способны усиливать свойства оснований. Например, анионы слабых кислот или анионы, образующие стабильные комплексы с металлами, могут ослабить базические свойства основания.
Таким образом, анионы играют важную роль в определении химических свойств оснований. Они могут как усиливать, так и ослаблять базические свойства оснований, в зависимости от своего типа и способности взаимодействовать с молекулами вещества.
Свойства оснований в присутствии катионов водорода и металлов
Основания - это химические вещества, которые обладают способностью принимать водородные ионы (H+) из раствора и образовывать ионы гидроксида (OH-). При этом основания играют активную роль в различных химических процессах и имеют свои свойства в присутствии различных катионов, таких как катионы водорода и металлов.
Катионы водорода играют важную роль в свойствах оснований. При образовании гидроксидных ионов они вступают в реакцию с основанием и образуют воду. Это происходит благодаря донорно-акцепторным свойствам водородных ионов, которые передают свой протон основанию. Таким образом, взаимодействие катионов водорода с основаниями повышает их активность и способность к образованию гидроксидов.
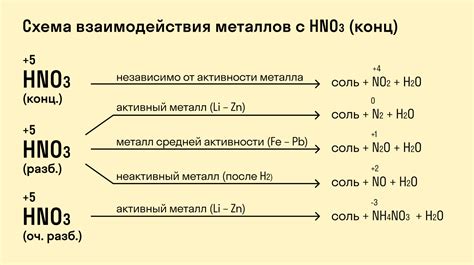
Кроме катионов водорода, основания могут реагировать и с катионами металлов. Это происходит из-за различной донорной активности металлических катионов. Некоторые металлы имеют большую электроотрицательность и, следовательно, активность в реакциях с основаниями. Такие основания могут образовывать стабильные соединения, например, гидроксиды металлов, которые имеют важное применение в различных областях химии и промышленности.
В общем, свойства оснований в присутствии катионов водорода и металлов зависят от их донорно-акцепторных свойств, которые обусловлены различием электроотрицательности и степени ионизации данных катионов. Это позволяет основаниям активно участвовать в различных химических реакциях и обладать разнообразными полезными свойствами.
Взаимодействие анионов с основаниями

Анионы, являясь отрицательно заряженными ионами, играют важную роль во взаимодействии с основаниями. Они могут вступать в реакцию с катионами водорода и металлами, образуя соли и гидроксиды.
Когда анион взаимодействует с катионом водорода в растворе основания, образуется соединение, называемое кислотным солем. Эти соединения обладают кислотными свойствами и могут отдавать протоны.
В случае взаимодействия анионов со металлами возникают металлические соли и гидроксиды. Гидроксиды являются основаниями и обладают щелочными свойствами. Эти соли и гидроксиды образуются в результате обменных реакций, когда анион замещает другой анион или группу атомов в соединении.
Анионы также могут взаимодействовать с сильными основаниями, образуя более сложные соединения. Например, гидроксид калия взаимодействует с фосфатным ионом, образуя соединение К3PO4 — фосфат калия.
Взаимодействие анионов с основаниями играет важную роль в химических реакциях и позволяет образовывать разнообразные соединения с разными свойствами. Это является основой для понимания и изучения химии и ее применения в различных областях науки и техники.
Изменение свойств оснований в зависимости от анионов
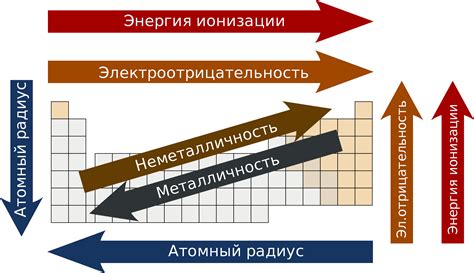
Свойства оснований могут существенно изменяться в зависимости от типа анионов, с которыми они реагируют. Анионы могут влиять на различные физические и химические свойства оснований, в том числе на их растворимость, кислотно-основные свойства и способность образовывать соединения с другими веществами.
Например, основания с анионами кислых оксидов (например, SO42-, NO3- и PO43-) обычно обладают высокой растворимостью в воде. Это связано с тем, что кислые оксиды обладают высокой электроотрицательностью и способны образовывать ионные связи с положительно заряженными ионами. Это делает эти анионы гидрофильными и способствует их растворению в воде.
С другой стороны, основания с анионами металлических оксидов (например, O2-, OH- и O22-) обычно обладают базовыми свойствами. Это связано с тем, что металлические оксиды обладают высокой активностью и способностью образовывать ионные связи с отрицательно заряженными ионами. Это делает анионы металлических оксидов гидрофобными и способствует образованию сильных ковалентных связей с ионами водорода или другими металлами.
Некоторые анионы также могут влиять на кислотно-основные свойства оснований. Например, анионы азота (например, NO3-) могут делать основания более кислотными, тогда как анионы серы (например, SO42-) могут делать их менее кислотными.
Таким образом, анионы играют важную роль в определении свойств оснований и их поведения в различных химических реакциях. Понимание влияния анионов позволяет углубить наши знания о химической природе оснований и использовать их с умом в различных областях науки и техники.
Вопрос-ответ

Какова роль катионов водорода и металлов в свойствах оснований?
Роль катионов водорода и металлов в свойствах оснований состоит в том, что они образуют ионы гидроксида (OH-) и определяют степень основности растворов. Катионы водорода (H+) определяют кислотность раствора, а катионы металлов, такие как натрий (Na+), калий (K+), кальций (Ca2+), магний (Mg2+) и др., определяют основность раствора. Катионы водорода и металлов реагируют с анионами гидроксида (OH-) в растворе, образуя воду (H2O) и соли. Ионные связи между катионами и анионами определяют стойкость основания и его способность нейтрализовать кислоты.
Как анионы влияют на свойства оснований?
Анионы играют важную роль в свойствах оснований. Они образуют ионы гидроксида (OH-) в растворе и определяют основность раствора. Анионы, такие как гидроксид (OH-), оксид (O2-), карбонат (CO3^2-), гидрокарбонат (HCO3-) и др., обладают негативным зарядом и могут реагировать с катионами водорода (H+) и металлов, образуя соли и воду. Чем больше концентрация анионов гидроксида в растворе, тем сильнее будет основание. Анионы также могут влиять на растворимость оснований и их способность образовывать отложения при взаимодействии с кислотами или другими соединениями.
