Взаимодействие металлов с растворами солей является важным объектом исследования в современной химии. Изучение этого процесса позволяет понять механизм образования соединений между металлами и солями, а также разработать новые способы синтеза и получения материалов с определенными свойствами.
Таблицы элементов взаимодействия металлов с растворами солей являются удобным источником информации о степени и скорости окисления металлов в различных условиях. Они включают в себя данные о химических реакциях, балансовых уравнениях и потенциалах электродов, что позволяет оценить активность и реакционную способность каждого металла.
Изучение элементов взаимодействия металлов с растворами солей имеет широкий практический интерес. Например, на основе этих данных можно определить возможность использования определенного металла в производстве сопротивлений, электродов, каталитических систем и других важных технических устройств. Таблицы также помогают оценить степень окисления металла в агрессивных средах и предотвратить его разрушение.
Взаимодействие металлов с растворами солей
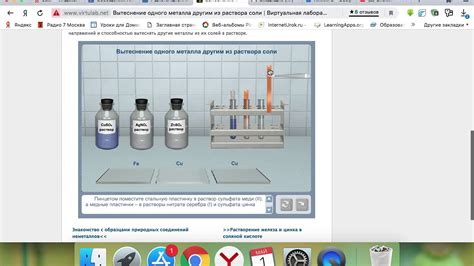
Взаимодействие металлов с растворами солей представляет собой важную область изучения химии. Это процесс, при котором металлы реагируют с растворами солей, образуя новые вещества и проявляя различные химические свойства.
Одним из примеров такого взаимодействия является реакция металла железа с раствором соли меди. В результате этой реакции образуется осадок из меди, а железо окисляется. Такие реакции имеют свои особенности в зависимости от конкретных металлов и солей, которые взаимодействуют между собой.
Взаимодействие металлов с растворами солей может сопровождаться не только образованием осадков, но и изменением цвета раствора или эволюцией газа. Например, металл цинк при контакте с раствором соли меди приводит к изменению цвета раствора из голубого в зеленый, так как происходит образование комплексного иона меди.
Важно отметить, что взаимодействие металлов с растворами солей может происходить как водных, так и неводных растворах. У каждого металла есть своя химическая активность, которая влияет на его способность вступать в реакцию с растворами солей. Например, металлы алкалийных металлов очень активны и легко реагируют даже с водой, образуя гидроксиды и выделяя водородный газ.
Таким образом, изучение взаимодействия металлов с растворами солей позволяет понять и увидеть химические свойства металлов, их реакционную способность и поведение в различных условиях. Это знание имеет большое практическое применение в различных отраслях, таких как металлургия, электрохимия, катализ и другие.
Определение взаимодействия

Взаимодействие металлов с растворами солей - это процесс, при котором металл вступает в реакцию с раствором соли, образуя продукты реакции: осадок, газы или ионы в растворе. Такое взаимодействие может иметь различные последствия и может служить основой для проведения различных химических экспериментов и исследований.
Определение взаимодействия металлов с растворами солей проводится путем введения металла в раствор соли и наблюдения за возникающими изменениями. В процессе испытания важную роль играют физические свойства металла, такие как его активность, плотность, электропроводность и коррозионная стойкость.
Чтобы определить возможное взаимодействие металла с раствором соли, используют различные методы и реактивы. Одним из таких методов является определение образования осадка. Если металл может реагировать с раствором соли, то при взаимодействии будет образовываться видимый осадок, который можно наблюдать невооруженным глазом или с помощью микроскопа.
Другой метод - определение образования газа. Некоторые металлы, взаимодействуя с растворами солей, образуют газы, которые можно обнаружить с помощью тестовых трубок или индикаторов. Это может быть использовано для идентификации металла или оценки его активности.
Также для определения взаимодействия металлов с растворами солей могут применяться различные ионоселективные электроды или физико-химические методы, такие как потенциометрия или вольтамперометрия. Эти методы позволяют точно измерить концентрацию ионов металла в растворе после его взаимодействия с раствором соли.
Виды взаимодействия металлов

Металлы обладают способностью взаимодействовать с другими веществами, включая растворы солей. В результате таких взаимодействий могут происходить различные химические реакции, которые можно классифицировать на несколько видов:
- Окисление и восстановление:
- Металл может быть окислен, то есть отдать электроны, при взаимодействии с раствором соли. При этом он превращается в ион положительного заряда (катион).
- Наоборот, металл может восстановиться, т.е. принять электроны от раствора соли и превратиться обратно в нейтральное атомное состояние.
- Взаимодействие с кислотами:
Некоторые металлы могут реагировать с кислотами, причем вид этой реакции может быть разным:
- Металл может замещать водород из кислоты, образуя соль и выделяя водород в виде пузырьков.
- Также металл может растворяться в кислоте с образованием ионов металла и соли.
- Некоторые металлы не реагируют с кислотами, например, золото и платина.
- Образование осадков:
При взаимодействии металлов с растворами солей может образовываться осадок - твердое вещество, которое выделяется из раствора. Осадок образуется в результате реакции металла с анионами (отрицательными ионами) в растворе.
Это лишь некоторые примеры видов взаимодействия металлов с растворами солей. Каждая реакция зависит от свойств конкретного металла и раствора, с которым он взаимодействует.
Свойства элементов
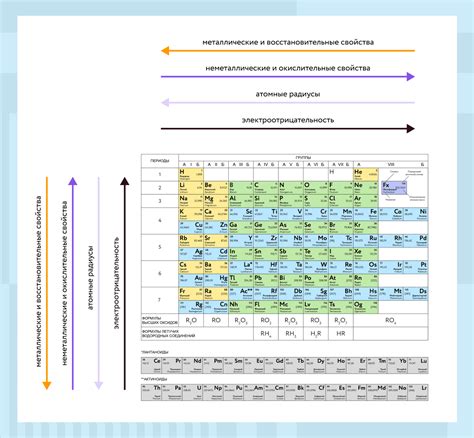
Металлы имеют ряд характерных свойств, которые определяют их поведение при взаимодействии с растворами солей. Одно из основных свойств металлов - это их способность образовывать ионы положительного заряда (катионы). Катионы металлов обычно имеют низкую энергию ионизации, что позволяет им легко отдавать электроны и образовывать положительные ионы.
Другим свойством металлов является их высокая проводимость тепла и электричества. Это связано с наличием свободных электронов в структуре металлов, которые свободно движутся под действием внешнего электрического поля. Благодаря этим свободным электронам металлы обладают металлическим блеском и хорошо проводят тепло и электричество.
Еще одним важным свойством металлов является их высокая плотность. Благодаря плотной упаковке атомов в кристаллической решетке, металлы обладают значительной массой по сравнению с другими материалами. Это обуславливает их прочность и твердость, а также способность выдерживать большие нагрузки и деформации.
Металлы также обладают химической активностью, которая проявляется в их способности образовывать соединения с другими веществами, в том числе растворами солей. В результате таких реакций образуются различные ионы и комплексы металлов, которые могут иметь различные свойства и применяться в различных областях науки и техники.
Вопрос-ответ

Какие металлы взаимодействуют с растворами солей?
Металлы, такие как натрий, калий, железо, цинк, медь, серебро, взаимодействуют с растворами солей.
Какова таблица элементов взаимодействия металлов с растворами солей?
Таблица элементов взаимодействия металлов с растворами солей представляет собой перечень металлов, упорядоченных по способности взаимодействовать с растворами солей. Каждый металл имеет свое место в таблице, которое определяется его реакционной способностью.
Какие реакции происходят при взаимодействии металлов с растворами солей?
При взаимодействии металлов с растворами солей могут происходить различные реакции. Например, активные металлы, такие как натрий или калий, могут вытеснять менее активные металлы из их растворов солей. Это называется обменной реакцией. Также металлы могут образовывать осадки или газы в результате взаимодействия с растворами солей.
