Щелочные металлы являются одной из основных групп химических элементов. Их свойства исследуются и изучаются в химии уже на протяжении многих веков. Важно понимать, что знание о щелочных металлах имеет большое практическое значение и помогает развивать науку и промышленность.
Щелочные металлы включают в себя такие элементы, как литий, натрий, калий, рубидий и цезий. В химии они часто используются в качестве важных реактивов и катализаторов. Они обладают рядом уникальных свойств, таких как низкая плотность, мягкость и низкая температура плавления. Именно благодаря этим свойствам щелочные металлы находят широкое применение в различных отраслях промышленности.
Опрос по щелочным металлам в химии для 9 класса направлен на проверку знаний учащихся о свойствах этих важных элементов, их реактивности, а также на понимание их роли в различных химических реакциях. В ходе опроса ученикам предлагается решить задачи, выполнить эксперименты и ответить на вопросы, которые помогут им закрепить полученные знания и развить навыки анализа и логического мышления.
История открытия щелочных металлов

Щелочные металлы – это группа элементов, включающая литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). История открытия щелочных металлов насчитывает несколько веков.
Первым щелочным металлом, который был открыт, был калий. Этот металл был открыт в 1807 году английским химиком и физиком Гумфри Дэви. Дэви проводил электролиз бромида калия и получил новое вещество, которое назвал калием. Открытие калия стало первым шагом в понимании щелочных металлов.
Другие щелочные металлы были открыты позже. В 1807 году Гумфри Дэви также открыл натрий путем электролиза соды. К этому времени, химики уже начали подозревать, что натрий и калий являются частью одной группы элементов. В 1814 году Йохан Арфведсон, шведский химик, открыл литий, который был найден в минерале петалит. Позднее, в 1860 году, были открыты рубидий и цезий, а в конце 19 века – франций.
Открытие щелочных металлов было важным вкладом в развитие химии. Эти металлы имеют ряд уникальных свойств и широко применяются в различных отраслях промышленности и науки. Щелочные металлы играют важную роль в процессах жизнеобеспечения органических систем и являются неотъемлемой частью нашей повседневной жизни.
Особенности химических свойств щелочных металлов
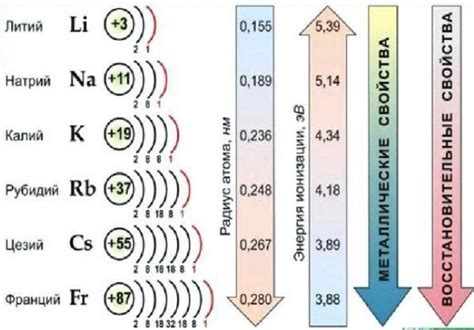
Щелочные металлы представляют собой группу химических элементов, включающую литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они обладают рядом уникальных химических свойств, которые делают их особенно интересными для изучения.
Во-первых, щелочные металлы являются сильными основаниями и активными металлами. Они реагируют с водой, образуя щелочные растворы и выделяя горючий водород. Также они легко реагируют с кислородом воздуха, образуя оксиды металлов.
Во-вторых, щелочные металлы обладают низкими значениями электроотрицательности и высокой активностью. Они легко отдают электроны и образуют положительные ионы. Благодаря этим свойствам, они являются хорошими проводниками электричества и тепла.
Кроме того, щелочные металлы образуют стабильные соединения с кислородом, образуя оксиды металлов. Эти соединения широко применяются в различных отраслях промышленности, включая производство стекла, ювелирные изделия и пиротехнику.
Щелочные металлы также обладают высокой реактивностью и способностью образовывать соли с другими элементами. Соли щелочных металлов обладают яркими цветами, что делает их привлекательными для использования в химических экспериментах и в производстве красителей.
Итак, особенности химических свойств щелочных металлов определяют их широкое применение в различных отраслях науки и промышленности. Изучение их свойств позволяет получать новые материалы и разрабатывать новые технологии.
Применение щелочных металлов в жизни

Натрий – один из щелочных металлов, широко применяемый в повседневной жизни. Натрий используется в пищевой промышленности для улучшения вкусовых качеств пищевых продуктов. Он также является составной частью соли и специй, которые добавляют в приготовление пищи. Благодаря своим свойствам натрий также применяется в осветительных приборах, энергетических батареях и как охлаждающая жидкость в некоторых технических системах.
Калий – еще один щелочной металл, неразрывно связанный с человеческим организмом. Калий является важным макроэлементом для адекватной работы сердечно-сосудистой и нервной систем, а также мышц. Калий используется в производстве удобрений для растений, что позволяет повысить уровень урожайности. Кроме того, калийное мыло изготавливается на основе гидроксида калия и широко используется в бытовой химии и косметической промышленности.
Литий – малораспространенный щелочный металл, но имеющий широкое применение в жизни. Литий-ионные батареи используются во многих портативных устройствах, таких как мобильные телефоны, ноутбуки и планшеты. Этот металл также используется в производстве лекарств для лечения биполярного аффективного расстройства и депрессии. Кроме того, литий широко применяется в производстве стекла и керамики, а также в ядерной энергетике.
Цезий – самый редкий и тяжелый щелочной металл. Он применяется в промышленности для создания атомных часов и точных измерительных приборов. Цезий также используется в производстве электронных устройств, особенно для создания чувствительных приборов, таких как фотодиоды и фотоэлектронные трубки. Кроме того, цезий-137 служит источником радиоактивности для медицинских и научных исследований.
Опасность использования щелочных металлов

Щелочные металлы – это группа химических элементов, которые характеризуются высокой реактивностью и способностью образовывать щелочные растворы. Их использование связано с определенными рисками и опасностями.
Первое и самое очевидное свойство щелочных металлов - их высокая реактивность. При контакте с воздухом они могут легко окисляться или реагировать с водой. Это может привести к возгоранию или взрыву в зависимости от условий. Поэтому при работе или хранении щелочных металлов необходимо соблюдать особую осторожность и использовать соответствующие меры безопасности.
Еще одна опасность, связанная с использованием щелочных металлов, – их высокая щелочность. Это означает, что они могут вызывать химические ожоги на коже и слизистых оболочках. При попадании на кожу или в глаза, они немедленно вызывают ощущение жжения и раздражение. В случае контакта необходимо мгновенно промыть место попадания водой и обратиться к медицинской помощи.
Также важно отметить, что способность щелочных металлов реагировать с водой может привести к образованию горючих водородных газов. Если использование щелочных металлов не контролируется и проводится в неправильных условиях, это может стать источником дополнительной опасности и возгорания.
В связи с вышеуказанными опасностями, использование щелочных металлов требует особых знаний и навыков в области безопасности. Поэтому рекомендуется использовать щелочные металлы только под надежным наблюдением и с соблюдением всех необходимых мер предосторожности. Необходимо работать с щелочными металлами только в хорошо проветриваемых помещениях, использовать защитные средства и соблюдать правила личной безопасности.
Эксперименты с щелочными металлами в химической лаборатории

Эксперименты с щелочными металлами являются важной частью химических исследований в лаборатории. Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, имеют широкий спектр применений, и их свойства и реактивность изучаются в химической науке.
Один из экспериментов, проводимых с щелочными металлами, - это их реакция с водой. Эта реакция происходит с выделением водорода и образованием гидроксидов щелочных металлов. Для проведения эксперимента требуется маленький кусочек щелочного металла, который помещается в колбу с водой. Результат реакции можно наблюдать по образованию пузырьков газа и изменению цвета раствора.
Другой интересный эксперимент - это реакция щелочных металлов с кислородом. Литий, например, горит на воздухе, образуя ярко-красное пламя. Это связано с тем, что щелочные металлы очень активно реагируют с кислородом, образуя оксиды. В эксперименте достаточно поместить маленький кусочек щелочного металла на петлю проволоки и поджечь его при помощи горелки.
Также можно провести эксперимент с растворением щелочных металлов в различных кислотах. Например, помещение натрия или калия в раствор соляной кислоты приведет к образованию соответствующих солей и выделению водорода. Для этого эксперимента необходимо добавить маленький кусочек щелочного металла в раствор кислоты и наблюдать реакцию.
Такие эксперименты позволяют более глубоко изучить свойства щелочных металлов и понять их химическую активность. Они также способствуют развитию навыков химического анализа и экспериментальных исследований учеников в химической лаборатории.
Практическое применение знаний о щелочных металлах

Знания о щелочных металлах имеют широкое практическое применение в различных областях нашей жизни. Например, натрий, один из щелочных металлов, широко используется в пищевой промышленности. Он является важным компонентом пищевых добавок, таких как поваренная соль, сода, пищевые ароматизаторы и регуляторы кислотности. Натрий также используется для консервирования пищевых продуктов и как основной ингредиент в изготовлении мыла и моющих средств.
Калий, еще один щелочный металл, находит применение в сельском хозяйстве. Калийные удобрения активно используются для повышения плодородия почвы и увеличения урожайности сельскохозяйственных культур. Калийные соединения также играют важную роль в медицине и фармацевтике. Они используются в производстве различных лекарственных препаратов для коррекции дефицита калия в организме и в лечении некоторых заболеваний.
Литий, третий щелочный металл, нашел применение в производстве литий-ионных аккумуляторов, которые используются в смартфонах, ноутбуках, электромобилях и других электронных устройствах. Литий-ионные аккумуляторы обладают высокими энергетическими характеристиками и длительным сроком службы, что делает их очень популярными.
В целом, знания о щелочных металлах являются неотъемлемой частью современной науки и технологий. Их применение простирается от пищевой промышленности до электроники, от фармацевтики до сельского хозяйства. Понимание свойств и особенностей этих металлов позволяет нам создавать новые технологии, повышать комфорт и эффективность нашей жизни, а также решать множество глобальных проблем в области экологии и энергетики.
Закрепление материала по щелочным металлам через тестирование

Для закрепления знаний по щелочным металлам и их свойствам, можно провести тестирование, которое поможет ученикам систематизировать полученную информацию и укрепить усвоенное.
Вопросы теста могут быть разнообразными и охватывать основные аспекты изучаемой темы. Например:
- Какие элементы относятся к группе щелочных металлов?
- Каковы основные свойства щелочных металлов?
- Какие соединения щелочных металлов широко используются в промышленности?
Для ответов на вопросы теста ученики могут использовать свои конспекты и учебники, что позволит им активно вспоминать и применять знания в практических задачах.
Кроме того, тестирование может проводиться в групповой форме, что способствует взаимодействию учеников друг с другом и обмену информацией, а также повышает мотивацию к изучению материала.
После прохождения тестирования можно провести обсуждение правильных и неправильных ответов, а также дать дополнительные объяснения и комментарии к затруднительным вопросам. Это поможет закрепить материал ещё сильнее и подготовит учеников к более сложным задачам и темам в области химии.
Вопрос-ответ

Для чего нужны щелочные металлы в химии?
Щелочные металлы играют важную роль в химии. Они используются в различных отраслях промышленности для производства щелочей, стекла, щелочных батарей и других веществ. Они также широко применяются в лабораторных условиях для проведения химических реакций и исследований.
Какие щелочные металлы существуют и чем они отличаются друг от друга?
Щелочные металлы включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они отличаются своими физическими и химическими свойствами. Например, литий - самый легкий щелочный металл, а франций - самый тяжелый. Также они имеют различные электрохимические свойства и реакционную способность.
Каково значение щелочных металлов для живых организмов?
Щелочные металлы имеют важное значение для живых организмов. Например, натрий и калий играют важную роль в регуляции водного баланса и функционирования нервной системы. Они также необходимы для работы мышц и сердечного ритма. Физиологические соли щелочных металлов часто добавляются в пищу и напитки, чтобы удовлетворить потребности организма в этих элементах.
