Коррозия - одно из основных явлений, которое негативно влияет на металлические конструкции и оборудование. Она может привести к разрушению материала и ухудшению его функциональных свойств. Взаимодействие различных металлов между собой играет важную роль в возможности возникновения коррозии. В зависимости от пар металлов, которые находятся в контакте, может возникать более или менее интенсивная коррозия.
Коррозия при взаимодействии металлов может быть вызвана различными факторами, такими как разность потенциалов, электролитическое взаимодействие, наличие кислорода и влаги. При наличии сильной разности потенциалов между двумя металлами, один из них будет служить анодом, а другой катодом. Анодный металл будет подвергаться активной коррозии, в то время как катодный металл будет защищать его от коррозии.
Некоторые комбинации металлов сильно снижают скорость коррозии благодаря эффекту, называемому "катодной защитой". Например, цинк и сталь создают гальваническую пару, в которой цинк служит катодом, защищающим сталь. Это применяется в гальванических анодных защитных системах, которые широко используются для защиты подводных частей судов и нефтяных платформ от коррозии.
Основные факторы влияния взаимодействия металлов на возможность коррозии

1. Разность потенциалов между металлами
Один из важных факторов, влияющих на возможность коррозии, - это разность потенциалов между металлами. Если встречаются два разных металла с разными значениями потенциалов, то может возникнуть электрохимическая реакция между ними, что приведет к коррозии. Такая реакция называется анодно-катодным взаимодействием.
2. Покрытия и защитные слои
Некоторые металлы имеют металлические или не металлические покрытия и защитные слои, которые могут защищать от коррозии. Например, антикоррозионные покрытия, такие как краска или гальваническое покрытие, помогают сохранить металлы от контакта с влагой и кислородом, что предотвращает коррозию.
3. Окружающая среда
Коррозия металлов зависит от состава и свойств окружающей среды. Например, контакт с хлоридами, солевыми растворами или кислотами может вызвать коррозию. Также влажность, температура и наличие различных загрязнений в окружающей среде могут повлиять на процесс коррозии металла.
4. Гальваническая пара
Когда два металла контактируют друг с другом в присутствии электролита, возможно образование гальванической пары. В таком случае, один металл может стать анодом, а другой катодом. Это может привести к коррозии анода. Примером такого взаимодействия является образование ржавчины на поверхности железа при контакте с алюминием.
5. Напряжение и механические напряжения
Механическое напряжение, такое как трение или давление, может влиять на возможность коррозии. Если металл находится под механическим напряжением, то вероятность коррозии может увеличиться. Также напряжение между разными частями металлической конструкции может вызвать коррозию в местах с наибольшей разностью потенциалов.
Химическое взаимодействие металлов

Химическое взаимодействие металлов является важным аспектом при изучении их свойств и поведения в различных средах. Оно определяет возможность образования соединений с другими элементами и соединениями, что может повлиять на их коррозионную стойкость.
Одной из основных форм химического взаимодействия металлов является окисление, которое происходит при контакте металла с кислородом в воздухе или с другими оксидирующими агентами. В результате окисления металл может образовывать оксид, который может защитить его от дальнейшей коррозии или, наоборот, ускорить процесс разрушения.
Кроме того, металлы могут реагировать с различными кислотами, основами и солями, образуя новые соединения. Например, некоторые металлы могут образовывать растворимые соли, которые могут вызывать коррозию при контакте с водой или другими растворами.
Химическое взаимодействие металлов также может происходить при контакте двух разных металлов. В этом случае может происходить гальваническая коррозия, когда один металл будет служить анодом, а другой – катодом. Это может возникать при контакте различных металлических компонентов в строительстве, в автомобильной промышленности или при использовании различных металлических инструментов.
Химическое взаимодействие металлов играет важную роль в понимании и предотвращении коррозии. Изучение свойств различных металлов, их взаимодействия с окружающей средой и друг с другом позволяет разработать эффективные методы защиты от коррозии и продлить срок службы металлических конструкций и изделий.
Электрохимическое взаимодействие металлов
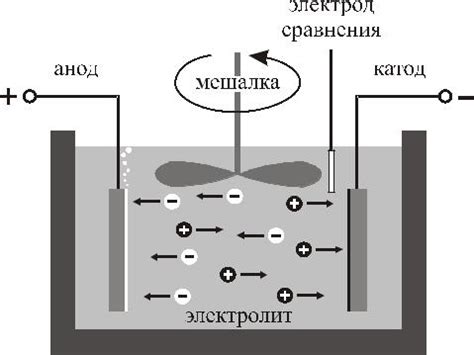
Электрохимическое взаимодействие металлов является важным фактором, определяющим возможность коррозии. Коррозия – это процесс разрушения металла под воздействием среды, вызванный электрохимическими реакциями.
Когда два или более различных металла находятся в контакте друг с другом в присутствии электролита, возникает гальваническая пара или гальванический элемент. В такой системе один металл оказывается более активным (анодом), а другой менее активный (катодом).
При этом анод – металл, который окисляется и передает электроны в электролит, а катод – металл, который восстанавливается и принимает электроны. Процессы окисления и восстановления связаны с передачей электрического тока, который приводит к коррозии анода и защите катода.
Такая пара металлов, где один будет служить анодом, а другой – катодом, создает условия для электрохимической коррозии. Разность потенциалов между этими металлами становится двигателем коррозионных процессов.
Понимание электрохимического взаимодействия металлов позволяет разрабатывать методы защиты от коррозии и выбирать сочетания материалов, которые будут обладать меньшей склонностью к электрохимической коррозии. Это крайне важно для повышения долговечности и надежности различных металлических конструкций и изделий в условиях эксплуатации.
Важность выбора правильной комбинации металлов

При выборе материалов для металлических конструкций или изделий необходимо учитывать их взаимное влияние на процесс коррозии. Коррозия является серьезной проблемой, которая может привести к ухудшению внешнего вида, снижению прочности и долговечности изделия. Поэтому, для того чтобы предотвратить или минимизировать процесс коррозии, важно выбирать правильную комбинацию металлов.
Разные металлы имеют различные электрохимические свойства, что влияет на вероятность возникновения коррозии при их взаимодействии. Некоторые металлы могут быть электрически более активными, тогда как другие - менее активными. При их сочетании может возникнуть электрохимическая пара, что способствует образованию гальванической коррозии.
Однако, существуют также такие комбинации металлов, которые могут обеспечивать дополнительную защиту от коррозии. Например, некоторые металлы, такие как цинк или алюминий, могут служить анодами, защищая другие металлы от коррозии. Это принцип гальванической защиты, который успешно применяется в различных отраслях промышленности.
Важно также учитывать условия эксплуатации изделия при выборе комбинации металлов. Некоторые металлы могут быть более устойчивы к определенным воздействиям, например, кислотам или солям. Поэтому, при проектировании и создании металлических конструкций необходимо учитывать все эти факторы, чтобы обеспечить долговечность и надежность изделия.
Таким образом, выбор правильной комбинации металлов является важным фактором в обеспечении защиты от коррозии. Необходимо учитывать электрохимические свойства металлов, принципы гальванической защиты и условия эксплуатации, чтобы обеспечить долговечность и надежность металлических конструкций или изделий.
Методы предотвращения коррозии при взаимодействии металлов

Коррозия - это процесс разрушения металлов под воздействием окружающей среды, вызванный их химическими реакциями с влагой, газами или другими веществами. Взаимодействие разных металлов может усилить коррозионные процессы и ускорить разрушение материала.
Одним из методов предотвращения взаимодействия металлов и последующей коррозии является использование анодной защиты. Этот метод основан на создании гальванической пары между металлами. При наличии анода из более реактивного металла, который будет активно окисляться, анодный металл будет защищен от коррозии. Этот метод широко применяется в морских условиях, где металлические конструкции подвержены агрессивным солевым растворам.
Другим эффективным методом предотвращения коррозии является использование покрытий и защитных покрытий на металлах. С помощью покрытий можно создать барьер между окружающей средой и металлом, что предотвратит взаимодействие и, соответственно, коррозию. Покрытия могут быть нанесены путем окрашивания, электрохимического осаждения или гальванического покрытия.
Для предотвращения коррозии металлов при их взаимодействии также применяются коррозионно-стойкие сплавы и материалы. Коррозионно-стойкие сплавы содержат особые добавки, которые придают им устойчивость к коррозии. Это позволяет использовать такие сплавы для изготовления конструкций, работающих в агрессивных условиях, например, в химической промышленности или морской среде.
Выбор метода предотвращения коррозии при взаимодействии металлов зависит от условий эксплуатации, типа металлов и требований к конструкции. Комбинация различных методов может обеспечить более эффективную защиту от коррозии и продлить срок службы металлических изделий.
Вопрос-ответ

Как взаимодействие разных металлов влияет на возможность коррозии?
Взаимодействие разных металлов может привести к электрохимической коррозии. Если два разных металла находятся в контакте в присутствии электролита (например, влажной среды), возникает гальваническая пара, которая приводит к активации одного из металлов. Более активный металл будет выделять электроны и подвергаться коррозии, в то время как менее активный металл будет защищен. Это называется анодно-катодным принципом и влияет на скорость коррозии.
Какие металлы лучше всего сочетаются и не вызывают коррозии?
Лучше всего сочетаются металлы, которые находятся близко друг к другу в ряду электрохимического потенциала, то есть имеют малую разницу в активности. Например, медь и алюминий сочетаются хорошо, поскольку они близки по активности и не вызывают гальванической коррозии. Сочетание разных металлов сильно зависит от конкретной среды, в которой они находятся, поэтому всегда важно проводить испытания и тестирование в конкретных условиях.
Как можно предотвратить коррозию при взаимодействии разных металлов?
Существуют различные способы предотвращения коррозии при взаимодействии разных металлов. Один из них - использование промежуточных слоев или покрытий. Например, между двумя разными металлами можно поместить слой неактивного металла или нанести на один из металлов защитное покрытие. Это помогает предотвратить прямой контакт металлов и снижает вероятность гальванической коррозии. Другой способ - использование специальных растворов или покрытий, которые уравновешивают разницу в электрохимическом потенциале между металлами. Важно также учитывать условия эксплуатации и окружающую среду, чтобы выбрать наиболее эффективные методы предотвращения коррозии.
