Метод определения эквивалента металла по объему выделившегося водорода – это один из простейших и наиболее распространенных методов определения эквивалентной массы металла. Основная идея метода заключается в том, что взаимодействие металла с кислородом приводит к образованию водорода, объем которого пропорционален количеству взаимодействовавшего металла. Таким образом, путем измерения объема выделившегося водорода можно определить эквивалентную массу металла.
Данный метод основывается на основных принципах химической реакции между металлом и кислородом, а именно на реакции образования гидроксидов металлов. Все металлы, кроме алюминия, содержатся в сыром состоянии в виде гидроксидов или солей, растворимых в воде. Под действием металла, растворяющегося в химическом путем воду, происходит образование водорода и соответствующего гидроксида металла.
Для проведения данного опыта требуется специальный аппарат, включающий в себя мерную бюретку с водой, сосуд с раствором кислоты и пробирку с металлом.
Эквивалент металла и его определение

Эквивалент металла - это показатель, который определяет количество металла, способного выделяться из раствора при взаимодействии с кислотой или электролитом. Этот метод широко используется для определения содержания металлов в различных материалах, таких как сплавы, руды или металлические изделия.
Определение эквивалента металла основывается на свойствах реакции металла с кислородом воды. При этой реакции выделяется водородный газ, объем которого напрямую зависит от количества металла. Для определения эквивалента металла применяют методом водородной дегазации, при котором металл помещается в раствор с избытком кислорода и выделяющийся водород собирается и измеряется.
Для определения эквивалента металла используются различные методы, включая гравиметрический, электрохимический и инструментальный анализ. Гравиметрический метод основан на измерении массы выделившегося металла, электрохимический метод - на измерении электрического тока, протекающего через раствор, а инструментальный метод - на применении специальных приборов, таких как спектрофотометры или атомно-абсорбционные спектрометры.
Определение эквивалента металла имеет широкое практическое применение в различных областях, включая металлургию, химию, геологию и электроэнергетику. Этот метод позволяет точно и надежно определить содержание металлов в различных материалах, что является важным для контроля качества и улучшения производственных процессов.
Объем выделившегося водорода в качестве определителя

Метод определения эквивалента металла по объему выделившегося водорода является одним из классических методов аналитической химии. Он основан на принципе реакции металла с кислотой, при которой выделяется водород.
Объем выделившегося водорода является важным определителем, так как его количество прямо пропорционально количеству металла, прореагировавшего с кислотой. Это позволяет определить эквивалент металла, то есть его массу, эквивалентную массе водорода.
Для проведения опыта по определению эквивалента металла по объему выделившегося водорода необходимо взвесить металл и поместить его в реакционную колбу, затем добавить кислоту. Под действием кислоты металл исчезает, а вместо него образуется пузырьки водорода, которые выделяются. Объем выделившегося водорода затем измеряется и используется для расчета эквивалента металла.
Метод определения эквивалента металла по объему выделившегося водорода широко применяется в аналитической химии для определения эквивалента различных металлов. Он позволяет получить точные результаты и является относительно простым и доступным методом анализа.
Основные этапы метода

1. Подготовка образца металла: В данном методе используется металлический образец, который должен быть предварительно очищен от загрязнений и оксидных пленок. Это делается с помощью механической обработки и химического травления.
2. Подготовка раствора: Для проведения эксперимента приготавливается раствор, содержащий кислоту и индикатор. Кислота обычно является сильным оксидантом, например, серной кислотой.
3. Иммерсия образца: Подготовленный образец металла помещается в приготовленный раствор и на него наносится точечное напускание мощным током для активации выделения водорода.
4. Измерение объема выделившегося водорода: Выделенный водород собирается в специальный сосуд, где его объем затем измеряется. Для этого может быть использован бюретный метод или газообразные манипуляторы.
5. Расчет эквивалента металла: По измеренному объему выделившегося водорода рассчитывается эквивалент металла, который выражается в граммах водорода, выделяющихся при электролизе одного грамма металла.
Все эти этапы позволяют определить эквивалент металла по объему выделившегося водорода и использовать его в дальнейших расчетах и исследованиях.
Реакция металла с кислотой

Реакция металла с кислотой - это химическая реакция, в результате которой металл взаимодействует с кислотой, образуя соль и выделяясь газ. Эта реакция является одним из способов определения эквивалента металла по объему выделившегося водорода.
При взаимодействии металлов с кислотами образуется ион водорода H+, который восстанавливается до молекулярного состояния и выделяется в виде газа. При этом металл вступает в реакцию с кислотой, окисляясь и образуя соль. Реактивность металла определяется его электрохимическим потенциалом и способностью вступать в реакцию с кислотой.
Реакция металлов с кислотами может быть представлена в виде уравнения химической реакции:
Металл + Кислота → Соль + Водород
Некоторые металлы, такие как натрий или калий, реагируют с кислотами очень активно, образуя сильно щелочные растворы соляных солей. Другие металлы, такие как медь или серебро, реагируют с кислотами значительно медленнее и выделяются водород в меньших объемах.
Использование реакции металла с кислотой для определения эквивалента металла по объему выделившегося водорода является одним из классических методов анализа. Он позволяет определить степень взаимодействия металла с кислотой и сравнить реактивность различных металлов.
Определение объема выделившегося водорода
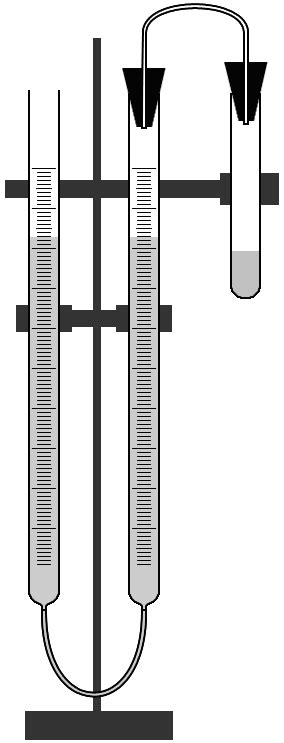
Определение объема выделившегося водорода представляет собой важный метод анализа, широко применяемый в различных областях науки и промышленности.
Для проведения данного определения необходимо иметь образец металла, с которым будет взаимодействовать кислота, а также кислоту, содержащую водород. Образец металла помещается в кислоту, в результате чего происходит химическая реакция, в ходе которой выделяется водород.
Объем выделившегося водорода можно определить с помощью специальных устройств, например, с помощью газового смесителя и спиртового горелка. При взаимодействии водорода с кислородом (наличие которого можно обеспечить с помощью подачи чистого кислорода) происходит воспламенение смеси, и по горящему фитилю можно определить объем выделившегося водорода.
Определение объема выделившегося водорода имеет широкое применение, например, для определения содержания водорода в различных материалах, включая металлы. Этот метод также используется в химических лабораториях для определения концентрации растворов и других химических веществ.
Точность определения объема выделившегося водорода зависит от точности проведения эксперимента и качества используемых реагентов. Поэтому важно соблюдать все условия и рекомендации, чтобы получить надежные результаты.
Применение метода в практике

Метод определения эквивалента металла по объему выделившегося водорода широко используется в практике различных отраслей промышленности. Он позволяет определить подлинность и качество металлических изделий, а также проводить контроль их производства.
Одной из основных областей применения этого метода является металлургическая промышленность. С его помощью можно определить эквивалент по объему выделившегося водорода различных сплавов, что позволяет проводить контроль химического состава материала. Этот метод также применяется для определения примесей и дефектов в металле.
Другой сферой применения метода является производство судов и авиационных конструкций. Определение эквивалента металла по объему выделившегося водорода позволяет контролировать качество сварных швов и металлических соединений, что является важным условием безопасности и надежности таких конструкций.
Также данный метод нашел свое применение в производстве электроники и приборостроении. Он используется для контроля качества металлических деталей, которые являются основными компонентами различных устройств и систем. С помощью этого метода можно выявить недостатки и дефекты материалов, что позволяет повысить надежность и долговечность электронных устройств.
Таким образом, метод определения эквивалента металла по объему выделившегося водорода нашел широкое применение в практике различных отраслей промышленности. Он является эффективным инструментом контроля качества и подлинности металлических изделий, а также позволяет выявить недостатки и дефекты материалов, что способствует повышению безопасности и надежности различных конструкций и устройств.
Контроль качества металлов

Одним из важных аспектов в производстве металлов является контроль их качества. Контроль качества необходим для проверки соответствия получаемых изделий требованиям стандартов и спецификаций. Он позволяет убедиться, что металлы обладают необходимыми механическими и физическими свойствами, а также сохраняют свою надежность и долговечность.
Контроль качества металлов может включать различные этапы, включающие проверку химического состава, механических свойств, прочности, твердости и др. Одним из распространенных методов контроля является метод определения эквивалента металла по объему выделившегося водорода. Этот метод позволяет оценить металлический материал на пористость, микротрещины и другие дефекты, которые могут негативно сказываться на его качестве и прочности.
Для проведения контроля качества металлов необходимо использовать специальные методы и оборудование. В лабораторных условиях проводятся испытания образцов металлов на различные показатели, а затем полученные результаты сравниваются с требованиями стандартов и спецификаций. Такой подход позволяет выявить и исправить возможные недостатки в качестве металлов, а также улучшить процесс их производства.
Контроль качества металлов является неотъемлемой частью производства и позволяет уверенно использовать данные материалы в различных отраслях промышленности, включая автомобильное производство, строительство, машиностроение и другие. Благодаря контролю качества, металлы могут быть использованы для создания безопасных и надежных изделий, что в свою очередь повышает их конкурентоспособность и удовлетворяет потребности клиентов.
Определение содержания металла в сплаве

Определение содержания металла в сплаве является важным этапом в процессе контроля качества материалов. Для этого используется метод определения эквивалента металла по объему выделившегося водорода. Этот метод основан на том, что металлы способны реагировать с водородом и образовывать газовые пузырьки.
Процедура определения содержания металла начинается с погружения образца сплава в кислую среду, содержащую водород. В результате химической реакции, металл начинает растворяться, выделяя при этом водородный газ. Чем больше металла содержится в сплаве, тем больше газовых пузырьков образуется.
Для определения содержания металла используется мерная лабораторная установка, которая позволяет измерить объем выделившегося водорода. После измерения объема газа, производится расчет эквивалента металла, по формуле, которая учитывает физико-химические свойства металла и особенности реакции взаимодействия с водородом.
Точность определения содержания металла в сплаве зависит от многих факторов, включая точность измерений объема газа, правильность подготовки образца, степень очистки от примесей и других веществ. Поэтому, для достижения точных результатов, необходимо соблюдать все требования и процедуры метода определения эквивалента металла по объему выделившегося водорода.
Возможности и ограничения метода
Метод определения эквивалента металла по объему выделившегося водорода является одним из наиболее распространенных и точных методов определения эквивалента металла. Он основан на химической реакции, при которой металлическая пластина погружается в специальный раствор и выделяется водород.
Одним из преимуществ этого метода является его высокая точность и надежность результатов. При правильной методике проведения эксперимента можно получить результаты, которые близки к реальным значениям эквивалента металла. Метод не требует сложной аппаратуры и может быть применен в лабораторных условиях.
Однако, метод также имеет некоторые ограничения. Во-первых, для проведения эксперимента требуется некоторое время, так как реакция между металлической пластиной и раствором происходит не мгновенно. Во-вторых, метод не является универсальным и может быть применен только для определенных металлов, которые способны выделять водород при взаимодействии с раствором.
Также стоит отметить, что метод определения эквивалента металла по объему выделившегося водорода может быть подвержен ошибкам. Неправильное выполнение методики или использование некачественных реагентов может привести к искажению результатов. Поэтому для получения достоверных данных необходимо строго соблюдать все условия и требования методики.
В целом, метод определения эквивалента металла по объему выделившегося водорода является эффективным и точным инструментом для определения эквивалента металла. При правильном использовании он позволяет получить надежные результаты, которые могут быть использованы в различных научных и промышленных областях.
Влияние примесей на результаты

В процессе определения эквивалента металла по объему выделившегося водорода может возникать проблема влияния различных примесей на получаемые результаты. Одним из основных факторов, оказывающих влияние на точность определения, является наличие примесей в исходном образце металла.
Примеси в металлах могут приводить к изменению скорости реакции с водородом, что в свою очередь приводит к искажению расчетов эквивалента металла. Некоторые примеси могут ускорять реакцию, тогда как другие - замедлять ее или даже препятствовать полной реакции между металлом и водородом.
Одним из способов учета влияния примесей является проведение контрольных испытаний на образцах с различными концентрациями примесей. Такой подход позволяет установить зависимость между концентрацией примесей и получаемыми результатами. На основании этих данных можно скорректировать расчеты эквивалента металла, учитывая влияние примесей.
Для более точных результатов необходимо также учитывать влияние других факторов, таких как температура, давление и концентрация реагентов. Они также могут оказывать значительное влияние на скорость реакции и объем выделившегося водорода. Поэтому важно проводить опыты в контролируемых условиях и учитывать все возможные факторы, которые могут влиять на результаты определения эквивалента металла.
Вопрос-ответ

Какой метод используется для определения эквивалента металла по объему выделившегося водорода?
Для определения эквивалента металла по объему выделившегося водорода используется метод вольтамперометрии.
Как происходит процесс выделения водорода?
Процесс выделения водорода происходит путем электролиза водного раствора соляной кислоты или других кислотных электролитов.
Каким образом определяется эквивалент металла по объему выделившегося водорода?
Для определения эквивалента металла по объему выделившегося водорода используется знание закона Фарадея, согласно которому масса вещества, осажденного или растворяющегося на электроде, пропорциональна затраченному при этом заряду.
