Оксиды щелочных металлов представляют собой неорганические соединения, состоящие из кислорода и металлического катиона щелочного металла. Щелочные металлы включают в себя такие элементы, как литий, натрий, калий, рубидий и цезий. Оксиды щелочных металлов обладают рядом уникальных свойств, которые делают их полезными в различных областях науки и технологии.
Одно из основных свойств оксидов щелочных металлов - это их щелочность. Это связано с тем, что оксиды щелочных металлов растворяются в воде, образуя гидроксиды, которые характеризуются высокой щелочностью. Гидроксиды щелочных металлов находят широкое применение в производстве щелочей и прочих продуктов химической промышленности.
Оксиды щелочных металлов также обладают высокой термической стабильностью. Они обычно имеют высокую температуру плавления и выдерживают термические нагрузки. Это делает их полезными в процессах, требующих высоких температур, таких как производство стекла, керамики и металлургия.
Необходимо отметить, что названия оксидов щелочных металлов имеют свою систему обозначений, основанную на ионных зарядах. Например, оксид лития обозначается Li2O, а оксид калия - K2O.
Оксиды щелочных металлов также широко применяются в качестве катализаторов, электролитов и полупроводников. Они обладают хорошей электрической проводимостью и могут служить материалами для создания суперконденсаторов и батарей высокой мощности.
Кроме того, некоторые оксиды щелочных металлов обладают фотолюминесцентными свойствами и могут использоваться в материалах для создания запоминающих устройств и дисплеев. Они также применяются в фармацевтической и косметической промышленности, а также в производстве огнеупорных материалов.
Оксиды щелочных металлов: основная информация

Оксиды щелочных металлов являются химическими соединениями, состоящими из кислорода и металлического элемента щелочной группы периодической системы. Эти соединения обладают рядом важных свойств и широко применяются в различных областях науки и промышленности.
Одной из основных характеристик оксидов щелочных металлов является их щелочность. Это связано с тем, что при взаимодействии с водой они образуют гидроксиды, которые проявляют щелочные свойства. Например, оксид натрия (Na2O) реагирует с водой, образуя гидроксид натрия (NaOH), который имеет щелочную природу и широко используется в производстве стекла, моющих средств и других продуктов.
Оксиды щелочных металлов также обладают высокой теплопроводностью и термической стабильностью. Это делает их полезными материалами для различных технических применений, включая производство керамики, стекловолокна и огнеупорных материалов. Благодаря своей высокой температурной стабильности, оксиды щелочных металлов также используются в качестве катализаторов, абсорбентов и активных компонентов в электрохимических устройствах.
Кроме того, некоторые оксиды щелочных металлов имеют важные оптические свойства. Например, оксид лития (Li2O) используется в производстве стекол с высокой прозрачностью в ультрафиолетовом диапазоне. Okсид калия (K2O) применяется в производстве оптических стекол с особыми оптическими свойствами.
Итак, оксиды щелочных металлов обладают разнообразными и важными свойствами, что делает их неотъемлемыми компонентами в различных отраслях промышленности и научных исследованиях.
Щелочные металлы: что это такое?
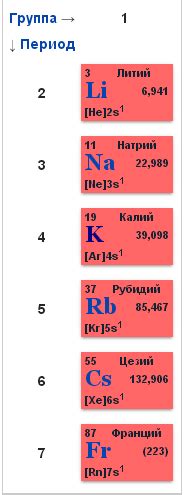
Щелочные металлы – это элементы периодической системы, которые относятся к 1 группе. К ним относятся литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
Щелочные металлы имеют металлический блеск и химически активны. Они хорошо проводят тепло и электричество, обладают низкой плотностью и низкой температурой плавления. Кроме того, щелочные металлы обладают низкой энергией ионизации, что делает их хорошими реагентами для различных химических реакций.
Щелочные металлы образуют оксиды, которые взаимодействуют с водой, образуя гидроксиды. Также они образуют соли, которые широко используются в различных областях науки и промышленности.
Химические свойства щелочных металлов объясняются их электронной структурой. У них одно электронное оболочка, которая легко отдается или принимается. Именно это делает их такими реактивными и способными к образованию разнообразных химических соединений.
Что такое оксиды щелочных металлов?

Оксиды щелочных металлов – это соединения, образующиеся при реакции щелочных металлов с кислородом. Они представляют собой неорганические соединения, состоящие из атома металла и атомов кислорода.
Оксиды щелочных металлов обладают рядом характеристических свойств. Во-первых, они обычно представляют собой твердые вещества, хотя некоторые из них могут быть жидкими при высокой температуре. Во-вторых, оксиды щелочных металлов обладают щелочными свойствами, то есть они реагируют с кислотами, образуя соли и воду.
Примеры оксидов щелочных металлов:
- Оксид лития (Li2O)
- Оксид натрия (Na2O)
- Оксид калия (K2O)
- Оксид рубидия (Rb2O)
- Оксид цезия (Cs2O)
Оксиды щелочных металлов широко используются в промышленности и научных исследованиях. Они используются в производстве стекла, керамики, щелочных абразивов и катализаторов.
Названия и свойства оксидов щелочных металлов

Оксиды щелочных металлов - это соединения, образуемые кислородом и щелочными металлами. Они имеют важное значение в химии и промышленности. Названия оксидов щелочных металлов образуются путем добавления к слову "оксид" названия конкретного металла. Например, оксид натрия, оксид калия, оксид лития и т.д.
Оксиды щелочных металлов обладают рядом особых свойств. Во-первых, они являются простыми веществами и представляют собой кристаллические соединения. Во-вторых, они обладают высокой степенью растворимости в воде, что делает их легко доступными для использования. Кроме того, оксиды щелочных металлов обладают щелочными свойствами и способны образовывать основания при реакции с водой.
Оксиды щелочных металлов также обладают высокой электропроводностью. Это объясняется наличием свободных электронов в кристаллической решетке, что позволяет проводить электрический ток. Благодаря этой особенности оксиды щелочных металлов широко используются в электротехнике и электролите для аккумуляторных батарей.
Кроме того, оксиды щелочных металлов часто применяются в качестве катализаторов в различных химических реакциях. Они обладают высокой активностью и способностью ускорять химические процессы. Это делает оксиды щелочных металлов важным компонентом в производстве различных промышленных продуктов и материалов.
Применение оксидов щелочных металлов

Оксиды щелочных металлов - это химические соединения, состоящие из атомов щелочных металлов и кислорода. Их широко применяют в различных областях науки и промышленности.
Одно из основных применений оксидов щелочных металлов - в производстве стекла. Их добавляют в стеклянную массу, чтобы изменить ее свойства. Например, оксид натрия (Na2O) делает стекло более прозрачным, а оксид калия (K2O) придает ему высокую термостабильность.
Оксиды щелочных металлов также находят применение в производстве мыла и моющих средств. Эти вещества имеют щелочную среду и содержат ионы щелочных металлов, которые обладают моющими свойствами. Их присутствие способствует удалять жир и грязь с поверхности.
Еще одним важным применением оксидов щелочных металлов является использование их в качестве катализаторов химических реакций. Они способны активировать реагенты и ускорять химические превращения. Например, оксид калия используется в процессе превращения сахарозы в фруктозу и глюкозу.
Неотъемлемой частью электроники являются полупроводники. Оксиды щелочных металлов, такие как оксид лития (Li2O) и оксид натрия (Na2O), находят применение в производстве полупроводниковых материалов. Они используются, например, в процессе изготовления полевых транзисторов.
Таким образом, оксиды щелочных металлов являются важными соединениями, которые находят широкое применение в различных отраслях промышленности. Они используются в стекольной, химической и электронной промышленности, а также в производстве мыла. Важно отметить, что каждый оксид щелочного металла обладает свойствами, которые позволяют использовать их в конкретных областях применения.
Вопрос-ответ

Какие основные свойства оксидов щелочных металлов?
Оксиды щелочных металлов обладают рядом общих свойств. Во-первых, они являются щелочными оксидами и растворяются в воде, образуя щелочные растворы. Во-вторых, они обладают высокой теплоемкостью и теплопроводностью. В-третьих, они образуют мощные щелочные растворы, которые легко реагируют с кислотами.
Какие виды оксидов щелочных металлов существуют?
Существует несколько видов оксидов щелочных металлов. Например, оксид натрия (Na2O), оксид калия (K2O), оксид лития (Li2O) и оксид рубидия (Rb2O). Каждый из них имеет свои особенности и применяется в различных областях промышленности и науки.
Каким способом можно получить оксиды щелочных металлов?
Оксиды щелочных металлов могут быть получены различными способами. Например, одним из способов является нагревание соответствующего металла в присутствии кислорода. Другим способом является обработка соответствующего гидроксида с помощью сильной соли. Кроме того, оксиды щелочных металлов могут быть получены и другими химическими реакциями.
Какие применения имеют оксиды щелочных металлов в промышленности?
Оксиды щелочных металлов имеют широкий спектр применений в промышленности. Например, оксид натрия используется для производства стекла, мыла и моющих средств. Оксид калия применяется в производстве удобрений и стекла. Оксид лития используется в производстве литиевых аккумуляторов и красителей. Оксид рубидия применяется в научных исследованиях и производстве электроники.
