Оксид щелочноземельного металла – это химическое соединение, состоящее из кислорода и щелочноземельного металла. Щелочноземельные металлы включают в себя бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Оксиды этих металлов обладают рядом уникальных свойств и широко используются в различных отраслях промышленности и науки.
Основные свойства оксидов щелочноземельных металлов включают высокую термическую и химическую стабильность, хорошую электропроводность, высокую твердость и химическую инертность. Эти свойства делают оксиды щелочноземельных металлов полезными в различных областях, включая производство стекла, керамики, электродов и катализаторов.
Оксиды щелочноземельных металлов также обладают реактивностью и способностью образовывать соли с различными кислотами. Например, оксид кальция (CaO), известный также как известь, реагирует с водой, образуя гидроксид кальция (Ca(OH)2) и выделяя большое количество тепла. Эта реакция, известная как гашение извести, широко используется в строительной и химической промышленности.
Химическая реактивность оксидов щелочноземельных металлов может быть усилена добавлением активных элементов, таких как алюминий (Al) или кремний (Si). Полученные смеси оксидов и алюмината или силиката щелочноземельных металлов обладают еще более высокой реактивностью и часто применяются в производстве огнеупорных материалов, эмалей и других специальных продуктов.
В заключение, оксиды щелочноземельных металлов являются важными химическими соединениями, которые обладают уникальными свойствами и широко используются в промышленности и науке. Их высокая стабильность, хорошая электропроводность и химическая инертность делают их незаменимыми в различных областях, а реактивность и способность образовывать соли позволяют использовать их в химических процессах и синтезе различных материалов.
Происхождение оксидов щелочноземельных металлов
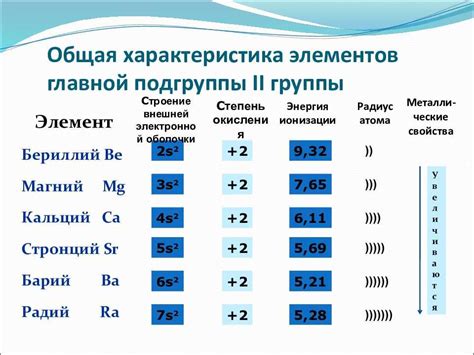
Оксиды щелочноземельных металлов являются химическими соединениями, состоящими из атомов щелочноземельных металлов и кислорода. Они образуются в результате реакции металлов с кислородом при высоких температурах, что делает их важными продуктами геологических и промышленных процессов.
Оксиды щелочноземельных металлов широко распространены в природе. Например, оксид кальция (CaO), известный также как известняк, является одним из основных компонентов известняковых пород. Он образуется при сгорании известкового камня в присутствии кислорода.
Другим примером может служить оксид магния (MgO), который образуется при нагреве магния. Это соединение также встречается в природе в виде минерала периклаза. Оксид магния широко используется в промышленности, например, в производстве огнеупорных материалов и в процессе сжигания угля для снижения выброса вредных веществ.
Оксиды щелочноземельных металлов обладают рядом уникальных свойств, которые делают их полезными в различных областях. Они обладают высокой теплоемкостью, высокой температурной стойкостью и химической инертностью. Кроме того, они являются хорошими проводниками электричества и тепла.
В заключение, оксиды щелочноземельных металлов имеют важное значение в геологии, промышленности и науке. Их происхождение связано с реакцией металлов с кислородом при высоких температурах, и они обладают рядом уникальных свойств, которые делают их полезными в различных областях. Изучение и применение этих соединений продолжает быть актуальной задачей для научных исследований и технологического развития.
Оксиды щелочноземельных металлов в природе

Оксиды щелочноземельных металлов широко распространены в природе и встречаются в виде минералов или рудных пород. Эти оксиды образуются в результате химических реакций между щелочноземельными металлами и кислородом, происходящих при высоких температурах или в результате окисления минералов и пород содержащих эти металлы.
Для щелочноземельных металлов, таких как магний, кальций, стронций и барий, основными оксидами являются соответственно оксид магния (MgO), оксид кальция (CaO), оксид стронция (SrO) и оксид бария (BaO). Эти оксиды выступают важными компонентами горных пород и минералов, таких как доломит, известняк и барит.
Оксиды щелочноземельных металлов обладают рядом химических и физических свойств, которые делают их полезными в различных областях. Например, оксид кальция (известка) широко используется в строительстве, для производства цемента и грунтовок, а также в производстве стекла и керамики. Оксид магния (магнезия) находит применение в производстве огнеупорных материалов, литников и электрических изоляторов, а также используется как компонент в лекарствах и пищевых добавках.
Всякий раз, когда мы встречаемся с минералами и рудами, содержащими щелочноземельные металлы, мы сталкиваемся и с их оксидами. Изучение свойств и реактивности оксидов щелочноземельных металлов позволяет нам лучше понять природу окружающего нас мира и эффективнее использовать эти материалы в различных областях нашей повседневной жизни.
Искусственное получение оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов являются важными химическими соединениями, которые широко применяются в различных областях. Они могут быть получены искусственно путем реакции металла с кислородом или его соединениями.
Получение оксидов щелочноземельных металлов начинается с выбора исходных материалов, которые обычно являются чистыми металлами или их соединениями. Затем происходит проведение реакций с использованием кислорода, воды или других оксидантов.
Реакция металла с кислородом может быть проведена путем нагревания или контакта с кислородом при определенных условиях. Результатом такой реакции является образование оксида щелочноземельного металла и выделение тепла.
Также оксиды щелочноземельных металлов можно получить путем реакции металла с водой или ее соединениями. Например, реакция цинка с водой приводит к образованию оксида цинка и выделению водорода.
Оксиды щелочноземельных металлов имеют важные свойства и реактивность, благодаря которым они находят применение в различных отраслях науки и техники. Искусственное получение этих соединений позволяет контролировать их состав и чистоту, что является важным фактором для их использования в различных приложениях.
Свойства оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов обладают рядом характерных свойств, которые обуславливаются особенностями атомной структуры и химической активностью этих элементов.
Во-первых, оксиды щелочноземельных металлов обычно образуются в результате реакции металлов с кислородом. Они представляют собой соединения, включающие кислородный атом и металлический катион. Такие соединения имеют сильно основные свойства, их растворы образуют гидроксиды и соли оснований, выпадающие в виде осадка.
Во-вторых, оксиды щелочноземельных металлов обладают высокой термической стабильностью. Они обычно имеют высокую температуру плавления и кипения, что связано с сильными электростатическими силами, действующими между атомами вещества.
Кроме того, оксиды щелочноземельных металлов обычно обладают кристаллической структурой, в которой атомы упорядочены по определенным правилам. Это обеспечивает им определенные физические и химические свойства.
Оксиды щелочноземельных металлов являются важными сырьевыми компонентами в химической, строительной и металлургической промышленности. Они используются в производстве стекла, керамики, цемента, а также как катализаторы и абразивные материалы. Благодаря своим уникальным свойствам, оксиды щелочноземельных металлов находят широкое применение в различных областях науки и техники.
Физические свойства оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов, таких как оксид кальция (CaO), оксид магния (MgO) и оксид бария (BaO), обладают рядом характерных физических свойств.
Во-первых, эти оксиды обычно являются белыми кристаллическими веществами, которые обладают высокой твердостью и точкой плавления. Оксид кальция имеет плотную кубическую структуру, тогда как оксиды магния и бария образуют кристаллы согласно гексагональной и кубической симметрии соответственно.
Во-вторых, оксиды щелочноземельных металлов обладают низкой летучестью и плохо растворимы в воде. Эти соединения обычно плохо проявляют реакцию с кислородом воздуха, что предотвращает их окисление в обычных условиях.
Кроме того, оксиды щелочноземельных металлов могут быть использованы в качестве катализаторов, например оксид кальция широко применяется в процессе синтеза аммиака. Эти соединения также могут иметь свойства щелочи, реагируя с кислотами и образуя соли.
Интересно, что оксиды щелочноземельных металлов могут образовывать полиэлектроны при взаимодействии с некоторыми полиионами, что позволяет использовать эти соединения в проводящих материалах.
Химические свойства оксидов щелочноземельных металлов

Оксиды щелочноземельных металлов представляют собой соединения металлов с кислородом. Они обладают рядом химических свойств, которые определяют их реактивность и применение в различных областях.
Первым химическим свойством, характерным для оксидов щелочноземельных металлов, является их основность. Они способны образовывать щелочные растворы при взаимодействии с водой. Это свойство основности объясняется высокой алкаличностью металлов, из которых они состоят.
Вторым химическим свойством оксидов щелочноземельных металлов является их способность взаимодействовать с кислотами. Они образуют соли при реакции с кислотами, что позволяет использовать их в процессах нейтрализации кислотных растворов.
Третье свойство оксидов щелочноземельных металлов – это их амфотерность. Они могут проявлять свойства и оснований, и кислоты в зависимости от условий реакции. Это дает им возможность реагировать как с кислотами, так и с основаниями.
Кроме того, оксиды щелочноземельных металлов обладают высокой термической стабильностью, что позволяет использовать их в качестве материалов для высокотемпературных процессов и катализаторов.
Изучение химических свойств оксидов щелочноземельных металлов является важным для понимания их роли в химических реакциях и разработке новых материалов с определенными свойствами.
Вопрос-ответ

Что такое оксид щелочноземельного металла?
Оксид щелочноземельного металла – это химическое соединение, образующееся в результате взаимодействия щелочноземельного металла с кислородом. Он обладает свойствами основания и используется в различных сферах промышленности.
Какие свойства имеет оксид щелочноземельного металла?
Оксид щелочноземельного металла имеет следующие свойства: высокую термическую и электрическую проводимость, химическую активность, основный характер реакции с водой, кислотами и кислородом, а также способность образовывать соли с кислотами.
Какие реакции возможны с участием оксида щелочноземельного металла?
Оксид щелочноземельного металла может реагировать с водой, образуя соответствующие гидроксиды. Он также реагирует с кислотами, образуя соли, и с кислородом, образуя пероксиды. Кроме того, оксид щелочноземельного металла может проявлять амфотерные свойства и реагировать как с кислотами, так и с щелочами.
Где может использоваться оксид щелочноземельного металла?
Оксид щелочноземельного металла находит применение в различных областях промышленности. Например, его используют для производства различных видов стекла, керамики и электроники. Оксиды щелочноземельных металлов также широко используются в производстве глиняных изделий и строительных материалов.
