Оксиды - это химические соединения, которые образуются при соединении металлов с кислородом. Металлы, будучи самыми активными химическими элементами, могут реагировать с кислородом воздуха или воды и образовывать различные оксиды.
Оксиды имеют особую роль в химии и промышленности. Они широко используются в производстве различных материалов, таких как керамика, стекло и металлы. Кроме того, они играют важную роль в органической химии и фармацевтике.
Оксиды металлов могут иметь различные структуры и свойства. Некоторые оксиды, такие как оксид магния (MgO) и оксид алюминия (Al2O3), являются твердыми, нерастворимыми веществами, которые обладают высокой температурной стойкостью. Другие оксиды, такие как оксид натрия (Na2O) и оксид калия (K2O), являются щелочными и могут образовывать растворы в воде.
Образование оксидов является важным процессом в химической реакции между металлами и кислородом. Оксиды могут иметь различные физические и химические свойства, и их использование в различных отраслях промышленности делает их важными соединениями для десятков тысяч производственных процессов.
Определение оксида

Оксид - это химическое соединение, состоящее из атомов металла и атомов кислорода. Оксиды образуются, когда металлы соединяются с кислородом при полном или частичном окислении.
Оксиды широко распространены в природе и встречаются в различных формах, например, оксид железа, оксид цинка, оксид алюминия и так далее. В органической химии оксиды также могут быть включены в состав биологически активных веществ и лекарственных препаратов.
Оксиды могут обладать различными свойствами, в зависимости от металла и кислорода, из которых они состоят. Некоторые оксиды являются кислотными оксидами, которые могут реагировать с водой и образовывать кислоты. Другие оксиды могут быть основными, т.е. обладать щелочными свойствами. Есть также оксиды, которые не проявляют характеристик ни кислоты, ни основания, и называются нейтральными оксидами.
Оксиды широко используются в промышленности, в том числе в производстве стекла, керамики, металлургии и получении металлов из их руд. Они также играют важную роль в природных процессах, например, оксиды железа отвечают за образование ржавчины на металлах.
Отличительные свойства оксидов

Оксиды являются классом химических соединений, которые образуются при взаимодействии металлов с кислородом. Они отличаются рядом свойств, которые делают их уникальными и полезными в различных областях.
Во-первых, оксиды обладают высокой термической стабильностью. Это означает, что эти соединения могут выдерживать высокие температуры без разложения или изменения своей структуры. Из-за этого оксиды широко используются в металлургической промышленности для получения и очистки металлов.
Во-вторых, оксиды характеризуются высокой электропроводностью. Под воздействием электрического поля, оксиды способны передавать электроны и образовывать электрический ток. Именно поэтому оксиды металлов часто используются в проводниках, а также в разработке электронных компонентов.
Кроме того, оксиды обычно обладают высокой степенью инертности. Это означает, что они не образуют реакций с другими химическими веществами и не подвержены коррозии или окислению. Поэтому оксиды широко используются в качестве защитных покрытий для металлических поверхностей.
Некоторые оксиды обладают также специфическими свойствами, которые делают их полезными в определенных областях. Например, оксид кремния является основным компонентом стекла и керамики. Оксид алюминия широко применяется в производстве алюминиевых сплавов и строительных материалов.
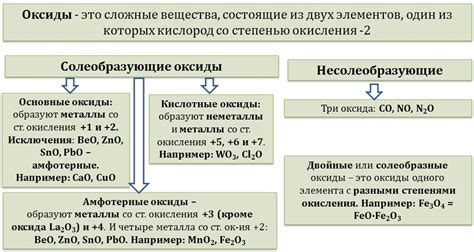
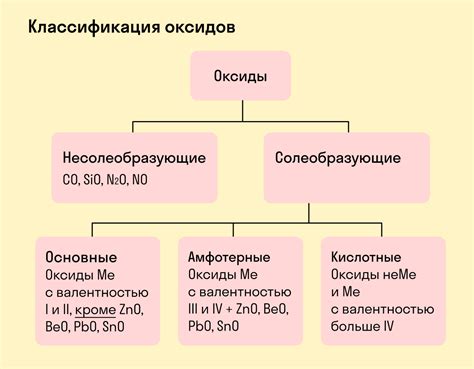
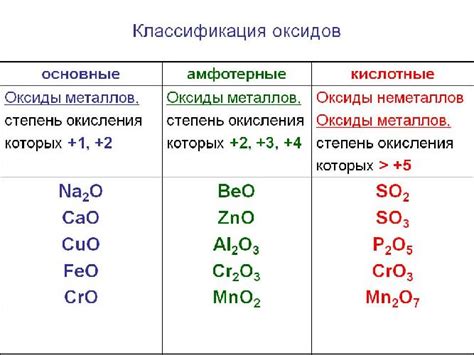
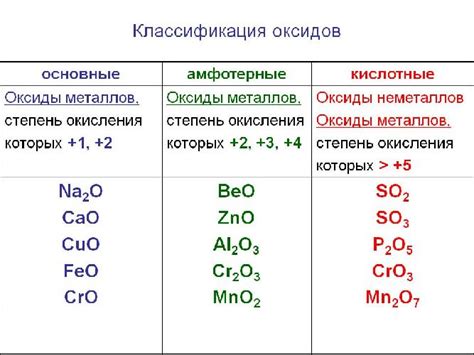
Виды оксидов:
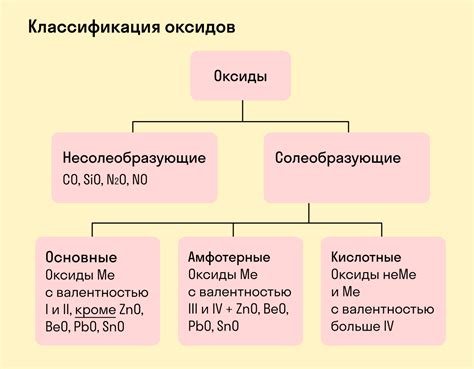
Оксиды - это соединения металлов с кислородом. В зависимости от структуры и химических свойств, оксиды делятся на разные виды.
1. Оксиды щелочных металлов: такие оксиды образуют щелочные металлы (например, натрий, калий). Они обладают щелочными свойствами и растворяются в воде, образуя гидроксид. Например, оксид натрия (Na2O) образуется при сжигании натрия в кислороде.
2. Оксиды щелочноземельных металлов: такие оксиды образуют щелочноземельные металлы (например, магний, кальций). Они также обладают алкалинными свойствами, но растворяются в воде не так легко, как оксиды щелочных металлов. Например, оксид магния (MgO) образуется при сжигании магния в кислороде.
3. Оксиды переходных металлов: такие оксиды образуют переходные металлы (например, железо, медь). Они имеют разнообразные свойства и могут образовываться в разных степенях окисления. Например, оксид железа (Fe2O3), известный как ржавчина, образуется при окислении железа в кислороде.
4. Оксиды полупроводников: такие оксиды образуют полупроводниковые материалы (например, кремний, германий). Они имеют специфические электронные свойства и широко применяются в электронике и солнечных батареях. Например, оксид кремния (SiO2), известный как кварц, является одним из наиболее распространенных оксидов полупроводников.
Все эти виды оксидов имеют разные химические и физические свойства и находят широкое применение в различных областях науки и технологии.
Процесс образования оксидов

Оксиды – это соединения, которые образуются при взаимодействии металлов с кислородом. Процесс образования оксидов может происходить при нагревании металла на воздухе или при его соприкосновении с водой или кислотами.
Когда металл вступает в реакцию с кислородом, происходит окисление – процесс, при котором атомы металла теряют электроны и образуют положительно заряженные ионы. Кислород, в свою очередь, получает электроны и образует отрицательно заряженные ионы. Образование оксидов – это результат такой химической реакции.
Оксиды металлов имеют различные свойства, в зависимости от типа металла и условий их образования. Некоторые оксиды могут быть твердыми веществами, другие – газами или жидкостями. Некоторые оксиды обладают кислотными свойствами и растворяются в воде, другие – щелочными и реагируют с кислотами.
Например, образование оксида железа (Fe2O3) при окислении железа воздухом приводит к образованию ржавчины на поверхности металла. Другой пример – образование оксида алюминия (Al2O3) при нагревании алюминия в присутствии кислорода. Также можно упомянуть об оксиде меди (CuO), который образуется при воздействии кислорода на медь во влажной среде.
Образование оксидов является одним из важных процессов, которые происходят в химических реакциях с участием металлов. Эти соединения имеют широкое применение в различных отраслях промышленности, а также в нашей повседневной жизни.
Применение оксидов
Оксиды широко применяются в различных отраслях промышленности и науке благодаря своим полезным свойствам и разнообразным химическим реакциям, в которых они участвуют.
Одним из наиболее распространенных применений оксидов является использование их в качестве катализаторов в химических процессах. Оксиды металлов, такие как оксид железа или оксид цинка, способны ускорять скорость химической реакции, улучшать ее эффективность и повышать выход продукта. Они находят применение в производстве пластмасс, лекарств, удобрений и других продуктов.
Оксиды также используются в процессе обработки металлов. Например, оксид алюминия широко применяется как абразивный материал в полировке и обработке поверхностей. Оксид циркония используется в изготовлении высокотемпературных керамических материалов, таких как нити для ламп накаливания или терморезисторы.
Оксиды также применяются в производстве стекла и электроники. Оксид кремния (кремнезем) является основным компонентом стекла и используется в производстве окон, посуды, оптических линз и других изделий. Оксиды металлов, такие как оксиды меди или оксид цинка, используются в электронике для создания полупроводниковых материалов и проводников.
Кроме того, оксиды металлов применяются в качестве красителей и пигментов в косметической и текстильной промышленности. Оксиды железа, оксиды титана и другие оксиды добавляются в косметические средства и краски для создания различных оттенков и эффектов.
Таким образом, оксиды играют важную роль в нашей жизни, находя применение во многих отраслях промышленности и науки благодаря своим уникальным свойствам и способностям.
Связь оксидов с окружающей средой

Оксиды - это химические соединения, образующиеся при взаимодействии металлов с кислородом. В природе оксиды металлов широко распространены и имеют различные физические и химические свойства. Связь оксидов с окружающей средой играет важную роль во многих процессах, в том числе в пищевой, медицинской и промышленной отраслях.
Оксиды металлов могут проявлять кислотные или щелочные свойства. Некоторые оксиды растворяются в воде, образуя щелочные или кислотные растворы, которые влияют на кислотно-щелочное равновесие окружающей среды. Такие оксиды могут играть важную роль в процессах защиты окружающей среды, например, в промышленных очистительных инсталляциях или в очистке сточных вод.
Другие оксиды металлов могут быть ядовитыми или иметь антимикробные свойства. Например, оксид цинка обладает противовоспалительными и антисептическими свойствами, поэтому он широко используется в фармацевтике и косметике. Также некоторые оксиды металлов, такие как оксиды свинца или меди, могут быть ядовитыми и вызывать серьезные отравления, поэтому их использование требует особой осторожности и контроля.
Связь оксидов с окружающей средой может быть также связана с физическими свойствами оксидов, такими как кондуктивность, термическая стабильность или магнитные свойства. Например, некоторые оксиды металлов могут быть использованы в электрических проводниках или магнитных материалах. Изучение свойств и взаимодействия оксидов с окружающей средой позволяет разрабатывать новые материалы с улучшенными свойствами и применениями в различных областях.
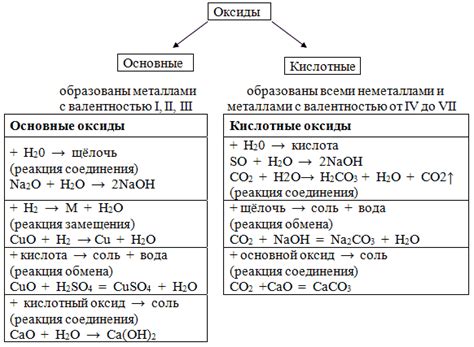
Взаимодействие оксидов с водой

Оксиды – это соединения металлов с кислородом. Они образуются при окислительных реакциях, когда металл вступает в контакт с кислородом. Многие металлы образуют оксиды, и эти соединения могут взаимодействовать с водой.
Взаимодействие оксидов с водой может происходить различными способами. Например, некоторые оксиды реагируют с водой, образуя основания. В результате такой реакции образуются гидроксиды металлов, которые растворяются в воде и образуют гидроксидные ионы.
Другие оксиды могут реагировать с водой, образуя кислоты. Такие реакции происходят, если металл в оксиде имеет высокую степень окисления. При взаимодействии с водой образуются кислотные ионы, которые растворяются в воде и делают ее кислой.
Некоторые оксиды металлов не реагируют с водой и могут быть использованы в различных промышленных процессах, например, для получения строительных материалов или при производстве электроники.
Взаимодействие оксидов с водой имеет важное значение в химических процессах и промышленности. Понимание этих реакций позволяет улучшить производственные процессы и разработать новые материалы с нужными свойствами.
Влияние оксидов на здоровье человека

Оксиды, образованные металлами, могут иметь различное влияние на здоровье человека в зависимости от своих химических свойств и концентрации в окружающей среде. Некоторые оксиды являются токсичными и могут вызывать различные заболевания и проблемы с дыхательной системой.
Например, оксиды некоторых металлов, таких как свинец, медь, цинк и алюминий, могут вызывать отравление организма при попадании их в организм через пищу, воду или воздух. Оксиды свинца могут накапливаться в организме и вызывать серьезные проблемы с нервной системой и почками.
Другие оксиды, такие как оксиды железа и алюминия, могут накапливаться в легких и вызывать астму, бронхит и другие заболевания органов дыхательной системы. Оксиды железа также могут вызывать изменения в составе крови и повышенное рискование развития сердечно-сосудистых заболеваний.
Однако, не все оксиды имеют отрицательное влияние на здоровье человека. Некоторые оксиды могут использоваться в медицине для лечения определенных заболеваний. Например, оксид цинка используется для лечения солнечных ожогов и различных кожных проблем. Оксид магния широко применяется в медицине как антиацидный препарат для лечения изжоги и желудочных язв.
В целом, влияние оксидов на здоровье человека зависит от их типа, концентрации и способа попадания в организм. Поэтому важно контролировать уровень оксидов в окружающей среде и принимать меры для минимизации их токсического воздействия на организм.
Вопрос-ответ

Какие металлы образуют оксиды?
Практически все металлы образуют оксиды. Оксиды металлов могут быть различных типов в зависимости от комбинации металла и кислорода.
В чем заключается значение образования оксидов металлами?
Образование оксидов металлами имеет большое значение, так как оксиды играют важную роль в химических реакциях и имеют различные свойства, которые могут быть полезными в разных отраслях промышленности.
Какие свойства имеют оксиды металлов?
Свойства оксидов металлов зависят от типа металла и комбинации с кислородом. Некоторые оксиды металлов являются кислотными, другие - основными, а некоторые - нейтральными. Также свойства оксидов могут включать проводимость электричества, магнитные свойства и другие.
Какие металлы образуют особенно активные оксиды?
Некоторые металлы, такие как натрий, калий и кальций, образуют особенно активные оксиды, которые быстро реагируют с водой и образуют щелочные растворы. Это может быть опасно и требует особого внимания при работе с такими металлами и их оксидами.
Какие оксиды используются в промышленности?
Оксиды металлов используются в промышленности для различных целей, таких как производство стекла, керамики, красок, электродов и других изделий. Они также могут использоваться в качестве катализаторов и добавок в различных процессах.