Оксиды металлов – это соединения металлов с кислородом, которые широко используются в промышленности и научных исследованиях. В реакциях оксидов металлов с водой, кислотами или основаниями часто наблюдаются основные свойства этих соединений. Но существует лишь предположение о том, что оксиды металлов проявляют только основные свойства, в то время как они также могут проявлять и кислотные свойства. Этот вопрос стал особенно актуальным в последние годы и вызвал интерес у многих исследователей и химиков.
Научные эксперименты исследователей в области химии и материаловедения привели к некоторым интересным результатам. Несколько исследований показали, что некоторые оксиды металлов могут проявлять и кислотные свойства, и это может быть объяснено структурой и электронными свойствами соединений. Например, исследования проведенные с использованием рентгеноэлектронного спектроскопа свидетельствуют о наличии кислотных свойств в оксидах металлов.
Исследования также подтверждают, что свойства оксидов металлов могут зависеть от их состава, структуры и методов получения.
Также следует отметить, что кислотные свойства оксидов металлов могут проявляться лишь при определенных условиях, таких как наличие вспомогательных соединений или катализаторов. Кроме того, физико-химические свойства оксидов металлов могут сильно варьировать в зависимости от температуры, давления и окружающей среды.
Таким образом, можно сделать вывод, что предположение о том, что оксиды металлов проявляют только основные свойства – это скорее миф, чем реальность. Свойства оксидов металлов могут быть разнообразными и зависят от многих факторов. Хотя основные свойства оксидов металлов действительно часто встречаются, кислотные свойства также могут быть проявлены в некоторых случаях.
Оксиды металлов и их свойства
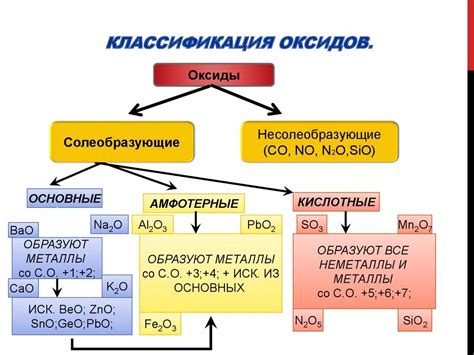
Оксиды металлов - это химические соединения, состоящие из металлического элемента и кислорода. Они обладают разнообразными физическими и химическими свойствами.
Во-первых, оксиды металлов проявляют основные свойства, что означает их способность образовывать гидроксиды при взаимодействии с водой. Это свойство связано с наличием ионов металла в структуре оксида.
Во-вторых, многие оксиды металлов проявляют амфотерные свойства. Это значит, что они могут проявлять и кислотные, и основные свойства в зависимости от условий взаимодействия. Например, оксид алюминия (Al2O3) может образовывать соли как с кислотными, так и с основными окислами.
Кроме того, оксиды металлов обладают различными цветовыми свойствами. Например, оксид железа (Fe2O3) имеет красный цвет, оксид меди (CuO) - черный, оксид цинка (ZnO) - белый.
Оксиды металлов широко применяются в различных отраслях науки и промышленности, например, в производстве стекла, керамики, электроники. Их свойства делают их важными компонентами при создании материалов с определенными функциональными свойствами.
Оксиды металлов как основные соединения
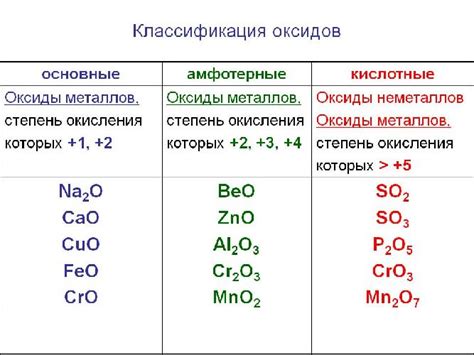
Оксиды металлов являются одними из самых распространенных и важных соединений в химии. Они образуются в результате реакции металла с кислородом. Особым свойством этих соединений является их способность проявлять только основные свойства.
Одной из основных характеристик оксидов металлов является их способность реагировать с кислотами, образуя соли. Это объясняется наличием щелочных свойств в структуре оксидов. Например, оксид кальция (CaO) реагирует с соляной кислотой (HCl), образуя хлорид кальция (CaCl2) и воду (H2O).
Кроме того, оксиды металлов обладают высокой электроотрицательностью, что позволяет им проявлять основные свойства при взаимодействии с кислотами. Например, оксид натрия (Na2O) реагирует с серной кислотой (H2SO4), образуя сульфат натрия (Na2SO4) и воду (H2O).
Также следует отметить, что оксиды металлов обладают основными свойствами при взаимодействии с водой. В результате реакции оксид металла и вода образуется гидроксид металла. Например, оксид калия (K2O) реагирует с водой (H2O), образуя гидроксид калия (KOH).
Таким образом, оксиды металлов являются основными соединениями, которые проявляют только основные свойства при взаимодействии с кислотами и водой. Они играют важную роль в различных процессах, включая производство сплавов, стекла, керамики и других материалов.
Основные свойства оксидов металлов
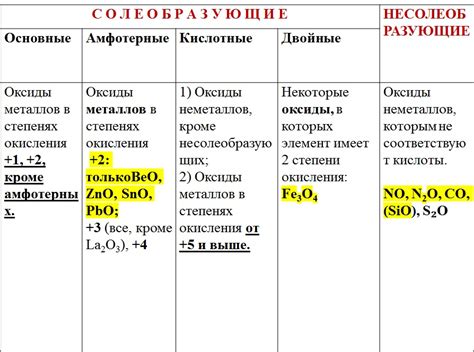
Оксиды металлов являются неорганическими соединениями, состоящими из металлического и кислородного элементов. Они проявляют ряд основных свойств, которые отличают их от других классов соединений.
Первое основное свойство оксидов металлов - их способность проявлять щелочные свойства. При реакции с водой они образуют гидроксиды металлов, которые в свою очередь обладают щелочными свойствами. Например, оксид натрия (Na2O) реагирует с водой, образуя гидроксид натрия (NaOH), который широко используется в химической промышленности.
Второе основное свойство оксидов металлов - их способность реагировать с кислородом. Оксиды металлов могут окисляться при взаимодействии с кислородом, образуя оксиды более высокой степени окисления. Например, оксид меди (II) (CuO) может окисляться до оксида меди (I) (Cu2O) при взаимодействии с кислородом.
Третье основное свойство оксидов металлов - их способность образовывать соли. При взаимодействии с кислотами оксиды металлов образуют соли - соединения, состоящие из катиона металла и аниона кислоты. Например, оксид цинка (ZnO) реагирует с соляной кислотой, образуя хлорид цинка (ZnCl2).
В целом, оксиды металлов проявляют только основные свойства и редко демонстрируют кислотные или нейтральные свойства. Их реактивность и способность образовывать различные соединения делают их важными компонентами в различных промышленных процессах и химических реакциях.
Возможности оксидов металлов расширяются за пределами основных свойств
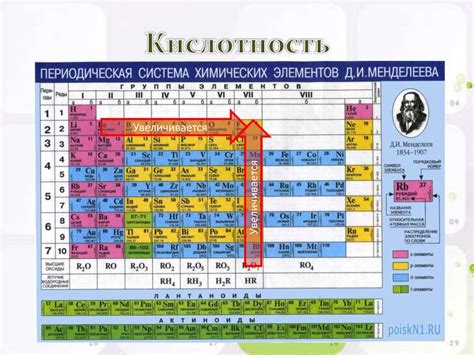
Однако оксиды металлов не ограничиваются только проявлением основных свойств. Они также могут обладать другими характеристиками, которые могут быть полезными в различных областях.
Некоторые оксиды металлов имеют ферромагнитные свойства, что делает их применимыми в магнитных материалах, таких как железные оксиды для изготовления катушек индуктивности и магнитных датчиков.
Оксиды металлов также могут обладать полупроводниковыми свойствами, что делает их ключевыми компонентами в электронных устройствах и полупроводниковой промышленности. Например, оксиды кремния широко используются в производстве солнечных панелей и интегральных схем.
Другой важной характеристикой, которой обладают некоторые оксиды металлов, является их светооптическое поведение. Например, оксиды титана и цинка используются в производстве оптических линз, покрытий для стекол и фотокатализаторов.
Можно сказать, что оксиды металлов проявляют не только основные свойства, но и имеют ряд других полезных характеристик, которые сделали их важными материалами в различных отраслях промышленности и науки.
Исследования и доказательства

Оксиды металлов – это химические соединения, которые образуются при соединении металла с кислородом. Исторически, оксиды металлов считались основными соединениями, проявляющими только основные свойства. Однако, последние исследования и эксперименты позволяют утверждать, что такое утверждение является недостаточно обоснованным.
Некоторые исследования показали, что оксиды металлов могут проявлять и кислотные свойства. Например, оксид алюминия (Al2O3) обладает свойствами кислоты при взаимодействии с основаниями. Это подтверждается изменением pH раствора после добавления оксида алюминия. Также было доказано, что оксиды металлов могут растворяться в кислотах, образуя соли металла и воду.
Другие исследования свидетельствуют о том, что оксиды металлов могут проявлять и амфотерные свойства, то есть способность как проявлять свойства кислоты, так и основания. Например, оксид цинка (ZnO) взаимодействует как с кислотами, так и с основаниями, образуя соли и воду. Такое поведение оксидов металлов объясняется различной степенью полярности связи металл-кислород.
Подводя итог, можно сделать вывод, что оксиды металлов не проявляют только основные свойства, но и кислотные, а иногда и амфотерные. Исследования и доказательства указывают на неоднозначность и многообразие свойств оксидов металлов, которые зависят от различных факторов, включая условия реакции и химический состав вещества.
Вопрос-ответ

Какие свойства оксидов металлов можно отнести к основным?
Основные свойства оксидов металлов включают их способность к реакции с кислотами, образованию щелочных растворов, а также их щелочность и способность образовывать ионы гидроксида в водных растворах.
Могут ли оксиды металлов проявлять и кислотные свойства?
Нет, оксиды металлов обычно не обладают кислотными свойствами. Они проявляют только основные свойства, такие как реакция с кислотами и образование щелочных растворов.
Какова природа основных свойств оксидов металлов?
Основные свойства оксидов металлов обусловлены их способностью образовывать ионы гидроксида в водных растворах. Это происходит за счет того, что металл в оксиде передает электроны кислороду, образуя ионы гидроксида. Таким образом, оксиды металлов обладают щелочными свойствами и могут реагировать с кислотами, образуя соли и воду.
