Окалина - это осадок, который образуется в процессе производства металла и содержит различные вещества, включая мелкие частицы металла, органические вещества, шлаки и другое.
Исследование реактивности окалины с различными веществами является важным для понимания и оптимизации процессов переработки металла. Окалина может обладать как положительными, так и отрицательными свойствами в зависимости от ее состава и условий окружающей среды.
Одной из важных характеристик реактивности окалины является ее способность растворяться в различных реагентах. Например, окалина может быть растворима в кислотах, щелочах или других химических соединениях. Это свойство позволяет использовать окалину для получения ценных веществ или для очистки от отходов.
Однако окалина также может проявлять негативную реакцию при контакте с некоторыми веществами. Например, некоторые компоненты окалины могут быть токсичными или вызывать коррозию металла. Поэтому изучение реактивности окалины с различными веществами является важным для безопасного и эффективного использования ее в производстве.
Исследование реактивности окалины с различными веществами является сложным заданием, требующим использования различных методов анализа и экспериментов. Важно выявить как положительные, так и отрицательные свойства окалины, чтобы успешно решать задачи обработки и переработки металла. Благодаря этим исследованиям можно разрабатывать новые методы очистки, повышать эффективность производства и снижать влияние на окружающую среду.
Реактивность окалина с кислотами

Окалина, или окисленные осадки, встречается в природе в виде твёрдых осадков, образующихся при окислении различных минералов. Известно, что окалина может проявлять реактивность с различными веществами, включая кислоты.
Взаимодействие окалины с кислотами может протекать по-разному в зависимости от свойств и концентрации кислоты, а также химического состава окалины. Некоторые кислоты, например, соляная кислота или серная кислота, могут вызвать разложение окалины с выделением газовых продуктов.
Окалина также может быть растворена в некоторых кислотах при достаточной концентрации и времени воздействия. В этом случае происходит химическое взаимодействие между окалиной и кислотой, в результате которого окалина растворяется или претерпевает изменения своей структуры.
Следует отметить, что некоторые кислоты могут оказывать очаговое действие на окалину, образуя блестящие или окрашенные пятна на ее поверхности. Это может быть связано с окислительными или восстановительными свойствами кислоты и ее взаимодействием с составляющими окалины.
В целом, реактивность окалины с кислотами является сложным и многофакторным процессом, который требует дополнительных исследований для полного понимания. Однако известно, что такое взаимодействие может приводить к изменениям в структуре и свойствах окалины, а также влиять на окружающую среду.
Особенности реакции

Реакция окалины с различными веществами обладает своими уникальными особенностями. При контакте с кислотами, например, наблюдается сильное выделение пузырей и образование пены. Данное явление связано с химическим взаимодействием между кислотными и оксидными компонентами окалины, что приводит к освобождению двуокиси углерода.
Реакция окалины с щелочами также имеет свои особенности. В данном случае наблюдается повышенная активность и выделение тепла. При взаимодействии щелочных и оксидных компонентов окалины происходит образование солей и воды. Часто подобная реакция сопровождается изменением цвета окалины, что связано с образованием новых химических соединений.
Взаимодействие окалины с металлами также характеризуется своей спецификой. Реакция между окалиной и металлами приводит к образованию относительно стабильных оксидов, которые могут образовывать пленки на поверхности металлов. Это может привести к защите металла от дальнейшей коррозии, однако иногда такие оксидные пленки могут быть нестабильными и приводить к активной коррозии.
Таким образом, реактивность окалины с различными веществами обнаруживает свои особенности в зависимости от природы вещества и условий их взаимодействия. Понимание этих особенностей позволяет более точно прогнозировать результаты реакции и использовать окалину в различных технологических процессах.
Реактивность окалина с щелочами

Окалина – это осадок, который образуется при горении угля или других органических веществ в присутствии кислорода. Он состоит из несгоревших остатков углерода и других минеральных примесей. Окалина обладает высокой реактивностью и может взаимодействовать с различными веществами, включая щелочи.
Щелочи – это вещества, которые обладают щелочными свойствами, то есть они образуют гидроксиды щелочных металлов (например, гидроксид натрия или гидроксид калия) при реакции с водой. Реактивность окалины с щелочами зависит от их концентрации и физико-химических свойств веществ.
При взаимодействии окалины с щелочами происходит образование растворимых солей и выделение газа. Например, при добавлении окалины в раствор гидроксида натрия (щелочной раствор) происходит образование осадка и выделение пузырьков газа.
Реактивность окалины с щелочами может быть использована в различных областях, например, в производстве щелочных металлов или при очистке сточных вод. Кроме того, это важное явление, которое может быть изучено и использовано в химическом образовании для демонстрации различных реакций.
Процесс взаимодействия
Реакция окисления и восстановления является основным процессом взаимодействия окалины с различными веществами. В зависимости от химического состава и свойств вещества, окалина может проявлять разную реактивность.
Окалина активно реагирует с металлами, образуя оксиды, гидроксиды или соли. Во время взаимодействия с металлами происходит образование окислов и выделение водорода. Например, при взаимодействии окалины с железом образуется окись железа и выделяется водородный газ.
Сильным окислителем является кислород, который в больших количествах присутствует в окислительных процессах с окалиной. Окалина реагирует с кислородом, образуя промежуточные оксиды. Например, при окислении окалиной гидрогена образуется окись водорода (H2O2).
Также окалина может взаимодействовать с органическими веществами, образуя различные соединения. Например, взаимодействие окалины с алканами приводит к образованию алканола и воды. В случае взаимодействия с карбонатами или гидрокарбонатами, окалина образует соли.
Определение реактивности окалины с различными веществами позволяет оценить возможность использования окалины в различных химических процессах, например, в производстве лекарственных препаратов или косметических средств.
Реактивность окалины с солями
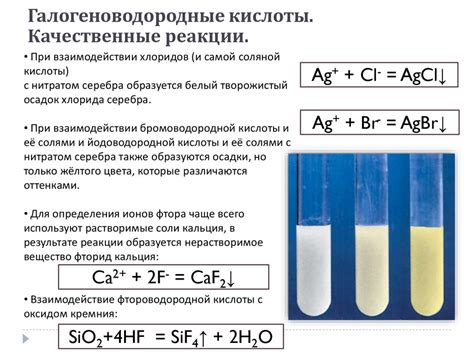
Окалина, или окись железа (III), является химическим соединением, которое обладает высокой реактивностью. Когда она взаимодействует с солями, происходят различные химические реакции.
Солями можно назвать различные химические соединения, в которых металл замещен на положительный ион. Например, сульфат железа (II) (FeSO4), хлорид железа (III) (FeCl3) или нитрат железа (III) (Fe(NO3)3). Все эти соли могут вступать во взаимодействие с окалиной, что приводит к образованию различных продуктов.
При взаимодействии окалины с солями происходит окислительно-восстановительная реакция. Молекулы окалины окисляются, теряя электроны, а ионы металла в соли восстанавливаются, получая электроны от окалины.
Реактивность окалины с солями может зависеть от концентрации и типа соли. Например, сульфат железа (II) и окалина взаимодействуют более интенсивно, по сравнению с хлоридом железа (III). Это связано с различием в структуре и свойствах этих соединений.
Таблица ниже показывает некоторые реакции окалины с солями:
| Соль | Реакция |
|---|---|
| Сульфат железа (II) | FeSO4 + 3Fe2O3 → 4Fe3O4 + SO2 |
| Хлорид железа (III) | FeCl3 + 3Fe2O3 → 4Fe3O4 + 3Cl2 |
| Нитрат железа (III) | Fe(NO3)3 + 6Fe2O3 → 7Fe3O4 + 3NO |
Образование осадка

Осадок образуется в результате реакции между окалиной и различными веществами, которые могут находиться в окружающей среде или быть добавлены специально. Реактивность окалина зависит от ее химического состава и может проявляться при контакте с кислотами, щелочами, солями и другими веществами.
В процессе реакции, молекулы окалины взаимодействуют с молекулами вещества, что приводит к изменению их структуры и образованию новых соединений. Эти новые соединения могут иметь осадочную форму и выделяться в виде мельчайших частиц, которые оседают на поверхности окалины или растворяются в ней.
Образование осадка может происходить как в результате химической реакции, так и при физическом взаимодействии веществ. Например, растворенные в воде соли могут связываться с окалиной в результате обменных реакций или образования сложных соединений с образованием мелких кристаллов или аморфных осадков.
Также, осадок может образовываться в результате диффузии веществ из окружающей среды или внутри самой окалины. Например, воздушная влага может производить конденсацию на поверхности окалины, образуя тонкий слой жидкости или мельчайшие капельки, которые затем могут осаждаться на поверхности вещества.
Образование осадка является одним из многих процессов, которые могут происходить при взаимодействии окалины с различными веществами. Этот процесс может иметь различные последствия и результаты, которые зависят от условий их взаимодействия и свойств самих веществ. Изучение этих процессов важно для понимания химической природы окалины и ее взаимодействия с окружающей средой.
Реактивность окалина с металлами

Окалин, представляющий собой твердый продукт окислительной реакции, может вступать в различного рода взаимодействия с металлами. Реактивность окалина с металлами зависит от их химических свойств и потенциала окисления.
Самыми реакционноспособными металлами в отношении окалина являются щелочные и щелочноземельные металлы. Они могут реагировать с окалином не только в водной среде, но и при нагревании. В результате таких реакций образуется искра, характерная для протекания реакции окисления металла.
Более инертные металлы, такие как серебро или платина, взаимодействуют с окалином меньше активно. Вследствие этого такие реакции проходят медленно и не выделяют значительного количества тепла и света.
Однако, реактивность окалина с металлами может быть усилена за счет различных факторов, таких как повышение температуры окружающей среды или добавление катализатора. Иногда могут происходить и более сложные реакции, например, образование металлических оксидов при взаимодействии окалина с металлами.
Вопрос-ответ

Что такое окалина?
Окалина - это шлак, примесь в необработанных материалах, таких как руда или уголь. Это вещество, которое остается после того, как руда или уголь прогреваются для получения полезных металлов или топлива.
Какая реактивность окалины с различными веществами?
Окалина имеет различную реактивность с различными веществами. Например, она может быть реактивной с водой, образуя газы или пену, или может реагировать с кислотами и основаниями. Различные вещества могут вызывать различные химические реакции с окалиной.
