Оксиды и металлы – важные компоненты высокотехнологичных процессов и материалов. Взаимодействие между оксидами и металлами может привести к различным результатам, в зависимости от особенностей химической реакции. Возможны окисление, образование сплавов или соединений, а также изменение свойств оксидов и металлов. В этой статье будут рассмотрены несколько примеров взаимодействия оксидов и металлов и их возможные последствия.
Одним из типичных примеров взаимодействия оксидов и металлов является окисление металла кислородом воздуха. При этом у металла отбираются электроны, что приводит к образованию соответствующего металлического оксида. Например, железо при окислении образует оксид железа (Fe2O3), который мы называем ржавчиной. Ржавчина имеет красно-коричневый цвет и характерный запах,а также может привести к разрушению металла. Однако ржавчина обладает также защитными свойствами, предотвращая дальнейшую коррозию металла.
Другим интересным примером взаимодействия оксидов и металлов является образование сплавов. Сплав – это материал, состоящий из двух и более металлов, которые смешиваются в расплавленном состоянии и затвердевают вместе. Так, сплав меди и цинка образует латунь, которая обладает прочностью, хорошей гибкостью и прекрасно поддается обработке. Также можно получить сплавы, добавляя к металлу другие вещества, например, никель или хром, для придания специальных свойств. Важно отметить, что химические свойства сплава могут быть отличными от отдельных металлов, что делает их полезными во многих отраслях промышленности и повседневной жизни.
Оксиды и металлы: взаимодействие и результаты
Оксиды и металлы - это два вещества, которые могут вступать во взаимодействие друг с другом. Результатом такого взаимодействия может быть образование соли и воды.
Взаимодействие оксида с металлом зависит от их свойств и химической активности. Некоторые оксиды могут реагировать с металлами и образовывать соли, при этом оксид сам может изменять свою окраску или физические свойства.
Одним из примеров такого взаимодействия является реакция меди с оксидом серы. При этом образуется сульфат меди и выделяется сероводород. Реакция протекает следующим образом:
2Cu + O₂ ⟶ 2CuO
CuO + H₂S ⟶ CuSO₄ + H₂O
Также возможно взаимодействие оксида с металлом, при котором образуется соль и обратимое окислительно-восстановительное взаимодействие. Например, взаимодействие оксида железа с алюминием:
Fe₂O₃ + 2Al ⟶ 2Fe + Al₂O₃
Это реакция, при которой оксид железа восстанавливается, алюминий окисляется, и образуется соль - оксид алюминия.
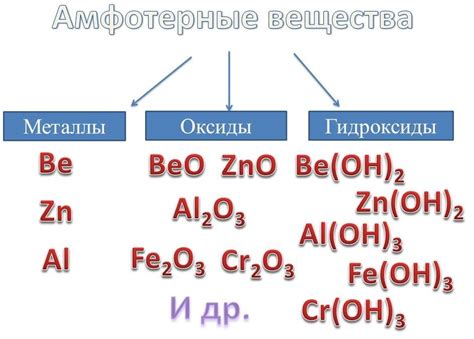
Интересно, что некоторые оксиды металлов обладают амфотерными свойствами, то есть могут реагировать как с кислотами, так и с щелочами. Примером такого оксида является оксид цинка:
ZnO + 2HCl ⟶ ZnCl₂ + H₂O
ZnO + 2KOH ⟶ K₂ZnO₂ + H₂O
Таким образом, взаимодействие оксида и металла может привести к образованию соли и воды, окислительно-восстановительному взаимодействию или амфотерному реагированию.
Оксиды и металлы: что это такое?
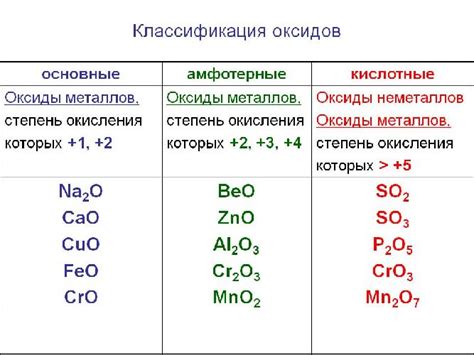
Оксиды - это соединения, состоящие из кислорода и другого химического элемента. Кислород может соединяться с различными металлами и неметаллами, образуя разнообразные оксиды. Оксиды играют важную роль в нашей жизни и в химической промышленности, так как они применяются в различных процессах и производствах.
С другой стороны, металлы являются одной из основных групп химических элементов. Они обладают характерными свойствами, такими как блеск, проводимость электричества и тепла, пластичность и т.д. Металлы являются важными материалами в различных отраслях промышленности, конструкции и техники.
Взаимодействие оксида и металла вызывает реакции, в результате которых образуются новые вещества. Например, оксид цинка взаимодействует с алюминием, образуя алюминат цинка и выделяя кислород. Подобные химические реакции могут происходить при различных условиях, и они имеют важное значение в химической и физической науке, а также в промышленности и технологиях.
Оксиды: свойства и структура
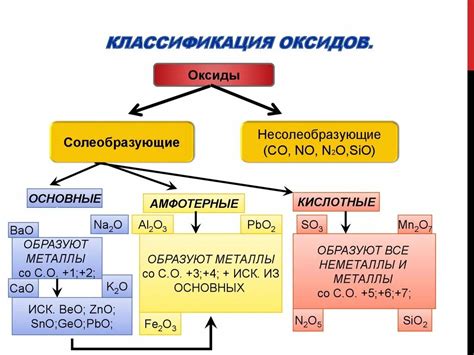
Оксиды представляют собой химические соединения, состоящие из атомов кислорода и других элементов. Они имеют широкое применение в различных областях науки и технологий.
Структура оксидов может быть различной и зависит от типа элементов, входящих в соединение. Некоторые оксиды представляют собой ионные кристаллические решетки, где атомы кислорода окружены ионами других элементов. Другие оксиды могут иметь молекулярную структуру, где атомы кислорода связаны с другими атомами через ковалентные связи.
Свойства оксидов также зависят от элементов, входящих в состав соединения. Некоторые оксиды могут быть кислотными и образовывать кислотные растворы при контакте с водой. Другие оксиды, напротив, могут быть щелочными и образовывать щелочные растворы. Еще есть оксиды, которые не образуют кислоты или щелочи, но способны реагировать с другими веществами.
Некоторые оксиды имеют высокую степень термической и электрической проводимости, что делает их важными в области электроники и энергетики. Другие оксиды могут обладать магнитными свойствами или быть полупроводниками. Изучение свойств и структуры оксидов имеет большое значение для разработки новых материалов и технологий.
Металлы: характеристики и особенности

Металлы - это класс материалов, обладающих определенными характеристиками, которые обуславливают их большую популярность в различных отраслях промышленности. Одной из основных особенностей металлов является их высокая тепло- и электропроводность, что делает их незаменимыми в производстве электроники и электроприборов.
Кроме того, металлы отличаются высокой прочностью и устойчивостью к механическим воздействиям, что делает их очень привлекательными для строительства различных конструкций и машин. Они также обладают способностью быть легко подвергнутыми обработке, что делает возможным создание сложных форм и конструкций.
Металлы имеют разнообразные свойства, которые обуславливают их различное использование. Например, алюминий является легким металлом с высокой коррозионной устойчивостью, благодаря чему он широко применяется в авиастроении и производстве упаковочных материалов. Сталь, являющаяся сплавом железа и углерода, обладает высокой прочностью и применяется в строительстве, машиностроении и производстве оружия.
Для классификации металлов используют также их химические свойства. Например, щелочные металлы, такие как литий, натрий и калий, обладают высокой реактивностью и способностью образовывать ионные соединения. Алкалиноземельные металлы, такие как магний и кальций, также обладают высокой реактивностью, но менее выраженной, чем ущелочных металлов.
Металлы играют важную роль в жизни человека и современной индустрии. Их уникальные характеристики и особенности позволяют использовать их в самых разных областях, существенно облегчая и улучшая нашу жизнь.
Химические реакции между оксидами и металлами

Химические реакции между оксидами и металлами представляют собой процессы образования или разложения оксидов в присутствии металлических элементов. Они играют важную роль в различных сферах нашей жизни, таких как промышленность, энергетика и жизнеобеспечение.
Одной из наиболее распространенных химических реакций между оксидами и металлами является реакция восстановления, при которой металл вступает во взаимодействие с оксидом, передавая ему электроны и превращая его в металл. Эта реакция особенно активна при высоких температурах, когда структура оксида разрушается и формируется соответствующий металл.
Другой важной реакцией является окислительно-восстановительная реакция, при которой металл окисляется, а оксид восстанавливается. В результате этой реакции происходит изменение окислительного состояния атомов металла. Она играет решающую роль в превращении металлов в стойкие оксидные формы, которые могут быть использованы в различных отраслях промышленности, например, в производстве стекла или керамики.
Реакции между оксидами и металлами часто протекают в присутствии кислорода, который является неотъемлемой частью оксидов. Кислород обладает сильными окислительными свойствами, поэтому металлы могут быть подвержены окислению в его присутствии. В свою очередь, оксиды металлов могут служить источником кислорода при взаимодействии с другими веществами.
Взаимодействие оксидов и металлов является сложным процессом, который зависит от множества факторов, таких как химические свойства веществ, условия окружающей среды и температура. Изучение этих реакций и их свойств позволяет нам лучше понять их роль в мире химии и улучшить технологии, основанные на использовании оксидов и металлов.
Взаимодействие оксидов и металлов: примеры и исследования

Взаимодействие оксидов и металлов представляет собой важный процесс, который часто изучается в химических исследованиях. Оксиды, как вещества, содержащие кислород, могут реагировать с металлами, образуя новые соединения и изменяя свои химические свойства.
Примером такого взаимодействия может служить реакция оксида железа (III) с алюминием. При нагревании этих веществ в твердом состоянии происходит экзотермическое взаимодействие, которое сопровождается выделением тепла и образованием нового соединения - алюминия оксида железа. Эта реакция имеет место и во время ржавления металлов, когда оксиды железа взаимодействуют с металлической поверхностью, приводя к ее коррозии.
Исследования взаимодействия оксидов и металлов включают как лабораторные эксперименты, так и теоретические расчеты. Ученые изучают кинетику этих реакций, анализируют структуру полученных соединений и ищут способы контроля и оптимизации данных процессов. Такие исследования имеют практическое значение, поскольку позволяют разрабатывать новые материалы, повышать стабильность металлических конструкций и улучшать свойства оксидных покрытий на металлических поверхностях.
Одним из интересных результатов исследований взаимодействия оксидов и металлов является использование альфа-титанового оксида в электрохимических аккумуляторах. Этот материал обладает высокой электропроводимостью и стабильностью, что делает его отличным анодом для литий-ионных батарей. Такие исследования и примеры взаимодействия оксидов и металлов продолжают вносить вклад в развитие науки и технологий, открывая новые возможности для применения этих соединений в различных областях.
Результаты взаимодействия оксидов и металлов: что происходит?
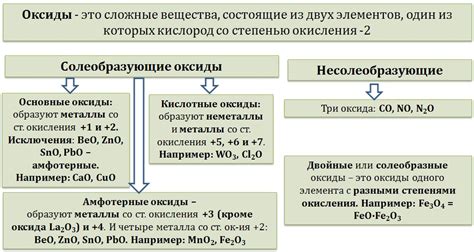
Оксиды и металлы являются основными компонентами химических реакций, которые происходят в природе и в промышленности. При взаимодействии оксидов и металлов происходят различные химические и физические изменения, которые приводят к образованию новых веществ и свойств.
Одним из результатов взаимодействия оксидов и металлов является образование новых соединений - солей. В зависимости от химической реакции и условий, при которых она происходит, могут образовываться различные виды солей. Например, взаимодействие оксида натрия и меди приводит к образованию соли куприта – Cu2O.
Кроме образования солей, взаимодействие оксидов и металлов может приводить к изменению состава и свойств металла. Например, при оксидации железной руды в присутствии кислорода образуется оксид железа - Fe2O3, который является основным компонентом ржавчины. Это пример процесса, который может негативно влиять на металл, приводя к его коррозии и разрушению.
Результаты взаимодействия оксидов и металлов также могут проявляться в виде изменений внешнего вида и свойств материалов. Например, при декоративном покрытии металла оксидами меди и железа можно получить различные оттенки и эффекты цветности, что применяется в производстве ювелирных изделий и художественной обработке металла.
В целом, результаты взаимодействия оксидов и металлов зависят от множества факторов - начиная от химической природы оксида и металла, заканчивая условиями реакции и присутствием катализаторов. Понимание этих процессов позволяет применять оксиды и металлы в различных областях науки и технологий для получения новых материалов с нужными свойствами и характеристиками.
Влияние оксидов на свойства металлов
Оксиды имеют существенное влияние на свойства металлов, влияя на их коррозионную стойкость, механические свойства и термическую стабильность.
Присутствие оксидной пленки на поверхности металла играет важную роль в защите от коррозии. Оксидные пленки предотвращают контакт металла с воздухом и водой, создавая барьер, который предотвращает окисление металла. Некоторые оксидные пленки, такие как оксид алюминия на поверхности алюминия, обладают свойством самозакрываться, что обеспечивает еще большую защиту металла.
Оксиды могут также влиять на механические свойства металлов, изменяя их твердость, прочность и усталостную стойкость. Например, добавление оксидов в сплавы может улучшить их механические свойства, увеличивая прочность и твердость. Оксиды также могут служить смазками, уменьшая трение между поверхностями металла и обеспечивая легкое движение.
Термическая стабильность металлов может быть повышена благодаря воздействию оксидов. Оксиды могут образовывать стабильные соединения с металлами, устойчивые к высоким температурам. Например, оксид циркония различных форм взаимодействует с металлами и сплавами, образуя термостойкие соединения, которые могут использоваться в высокотемпературных приложениях, таких как аэрокосмическая промышленность и энергетика.
Практическое применение взаимодействия оксидов и металлов

1. Производство сплавов. Оксиды металлов широко используются в промышленности для производства сплавов. Взаимодействие оксидов и металлов позволяет улучшить механические и химические свойства материалов. Например, добавление оксида алюминия к меди создает сплав, который обладает повышенной прочностью и коррозионной стойкостью.
2. Производство керамики. Оксиды металлов используются при изготовлении керамических изделий. Например, оксид циркония позволяет создать керамические протезы, которые обладают высокой прочностью, стойкостью к износу и биологической совместимостью.
3. Катализаторы. Оксиды металлов применяются в качестве катализаторов в различных процессах. Например, оксид железа используется в катализаторах для синтеза аммиака, который является основным компонентом удобрений. Катализаторы на основе оксидов металлов позволяют ускорить химические реакции и снизить энергозатраты на производство.
4. Электроника. Оксиды металлов применяются в производстве электронных компонентов. Например, оксид цинка используется в производстве транзисторов и светодиодов. Взаимодействие оксида цинка с другими материалами позволяет создать полупроводниковые материалы с определенными электрическими свойствами.
5. Краски и покрытия. Оксиды металлов применяются в производстве красок и покрытий. Например, оксид железа используется для получения коричневого и красного пигментов. Взаимодействие оксидов металлов с различными добавками позволяет создавать разнообразные цвета и эффекты покрытий.
6. Очистка воды. Оксиды металлов используются в процессе очистки воды от загрязнений. Например, оксид алюминия применяется в процессе коагуляции для удаления взвешенных частиц из воды. Взаимодействие оксидов металлов с загрязнениями позволяет образовать осадок, который можно легко удалить.
7. Производство стекла. Оксиды металлов используются в процессе производства стекла для придания ему особых свойств. Например, оксид свинца повышает прозрачность стекла, а оксид бора повышает его термостабильность. Взаимодействие оксидов металлов со стекловидными компонентами позволяет получать различные типы стекла с нужными свойствами.
Вопрос-ответ

Какие бывают оксиды?
Оксиды - это химические соединения металлов с кислородом. Их можно классифицировать по наличию одного или нескольких видов атомов металла и кислорода в соединении.
Как происходит взаимодействие оксида и металла?
При взаимодействии оксида и металла обычно происходит реакция окисления металла, при которой металл отдает электроны кислороду. В результате образуется соединение металла с кислородом, а также может образоваться тепло или свет.
Что происходит, если металл реагирует с воздухом?
Если металл реагирует с кислородом в воздухе, то образуется оксид металла. Например, железо при окислении в воздухе образует ржавчину - оксид железа (III). Реакция с кислородом в воздухе может привести к разрушению металлических предметов и коррозии.
Каковы применения оксидов металлов?
Оксиды металлов имеют широкий спектр применений. Например, оксид меди используется в производстве керамики и стекла, оксид железа используется в производстве красок и магнитов, оксид цинка используется в косметике и лекарственных препаратах.
