Оксид металла вода - это вещества, образующиеся в результате реакции металла с водой или паром воды. Эти соединения являются одними из наиболее распространенных и важных классов химических соединений. Вода в реакции с металлами может действовать как окислитель или восстановитель в зависимости от условий.
Свойства оксидов металла воды включают в себя их способность растворяться в воде и образовывать щелочные растворы. Оксиды металла воды также обладают различной степенью активности, что может зависеть от типа металла и его электрохимического потенциала. Кроме того, оксиды металла воды обычно обладают характерными физическими свойствами, такими как цвет, плотность и температура плавления.
Важно отметить, что оксиды металла воды могут играть важную роль в различных химических процессах и применяться в разных отраслях промышленности. Они могут использоваться в качестве катализаторов, пигментов, абразивов и многих других веществ. Кроме того, некоторые оксиды металла воды обладают антисептическими свойствами и могут использоваться в медицине для лечения различных инфекций и заболеваний.
Оксид металла вода: определение и классификация

Оксид металла вода – это химическое соединение, образующееся при реакции металла с кислородом в присутствии влаги или воды. Они широко распространены в природе и являются основными компонентами минералов и руд.
Оксиды металлов воды можно классифицировать по следующим критериям:
- Различие по химическому составу: оксиды металлов воды могут быть одноосновными (содержат одну молекулу кислорода) и многоосновными (содержат несколько молекул кислорода).
- Различие по степени окисления металла: в соединениях с низкой степенью окисления металл имеет более положительный окислительный потенциал, в то время как в оксидах с высокой степенью окисления металл имеет более отрицательный окислительный потенциал.
- Различие по структуре: оксиды металлов воды могут быть аморфными (без определенного кристаллического строения) или кристаллическими (с определенной кристаллической решеткой).
Оксиды металлов воды имеют различные свойства и могут использоваться в различных областях, включая производство металлургических материалов, катализаторов, аккумуляторов и электродов.
Оксид металла вода: роль в химических реакциях
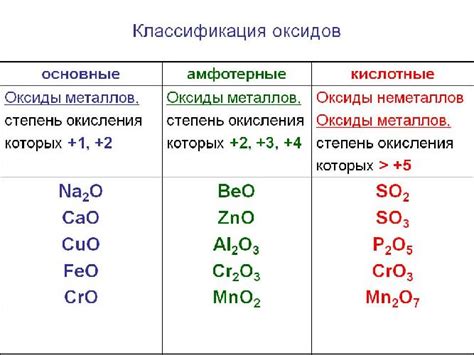
Оксиды металлов с водой могут реагировать, образуя кислоты или щелочи, в зависимости от своих свойств. Эта реакция имеет важное значение в различных химических процессах.
Когда оксид металла взаимодействует с водой, происходит гидратация молекулы, в результате чего образуются кислоты или основания. Эта реакция называется гидратацией оксида. При гидратации оксида металла вода диссоциирует и образует ионы гидроксида и катионы металла.
Гидратация оксида металла вода играет важную роль в процессе образования кислот и щелочей. Кислоты образуются, когда оксид металла диссоциирует в воде, а щелочи формируются при диссоциации гидроксидов металлов. Гидратация оксида также может включать образование и других органических соединений.
Гидратация оксида металла вода также влияет на pH-значение водных растворов. Кислотные растворы имеют nизкое pH (меньше 7), основные растворы имеют высокое pH (больше 7), а нейтральные растворы имеют pH около 7. При гидратации оксида металла вода происходит изменение pH-значения раствора в сторону кислоты или щелочи.
Гидратация оксида металла вода играет важную роль во многих промышленных и технологических процессах. Например, гидратация оксидов металлов является основой для получения многих химических соединений, используемых в производстве лекарств, красителей, пищевых добавок и других продуктов. Также гидратация оксидов металлов вода применяется в процессах очистки воды и водоподготовки в различных отраслях промышленности.
Оксид металла вода: свойства и структура
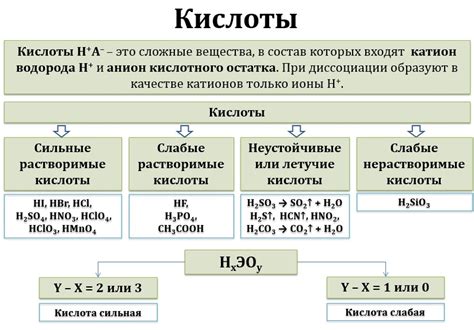
Оксид металла вода – это соединение, в состав которого входят металл и кислород. Одним из наиболее известных и распространенных оксидов металла воды является оксид железа II (FeO). Он образуется при реакции металла железа с кислородом из воды или воздуха.
Оксиды металла воды обладают рядом химических и физических свойств. Они часто обладают хорошей проводимостью электрического тока и являются химически активными соединениями. Их свойства зависят от типа и состояния металла, а также от условий среды, в которой они находятся.
Структура оксида металла воды включает в себя металлическую сетку, в которой оксидные и водородные ионы располагаются. Эта структура обеспечивает устойчивость соединения и его способность взаимодействовать с другими веществами.
Оксиды металла воды широко применяются в различных отраслях промышленности и науки. Например, оксид железа II используется в производстве стекла и керамики, а оксид алюминия – в производстве алмазных и инструментов. Кроме того, оксиды металла воды являются важными катализаторами в химических реакциях.
Свойства оксида металла воды могут быть изменены путем добавления различных примесей или взаимодействием с другими веществами. Это позволяет использовать оксиды металла воды для создания материалов с заданными свойствами и функциональностью.
Оксид металла вода: применение в промышленности

Оксиды металла воды широко используются в различных отраслях промышленности благодаря своим уникальным свойствам и химическим реакциям.
Одно из основных применений оксидов металла воды – производство керамики и стекла. Оксиды металла добавляются в сырьевую смесь, которая после обработки при высокой температуре превращается в прочный и прозрачный материал. Керамика и стекло с применением оксидов металла обладают высокой степенью прочности и устойчивостью к воздействию влаги и агрессивных сред.
Оксиды металла воды также используются в качестве катализаторов в различных химических процессах. Благодаря своим специфическим физико-химическим свойствам, они ускоряют химические реакции и повышают их эффективность. Такие катализаторы широко применяются в производстве пластмасс, лаков, красителей, удобрений и многих других химических продуктов.
Еще одним важным применением оксидов металла воды является их использование в электронной и электротехнической промышленности. Оксиды металла используются в производстве полупроводниковых материалов, суперконденсаторов, а также в производстве электролитических конденсаторов. Кроме того, оксиды металла воды применяются в качестве диэлектриков, анодов и катодов в различных электролитических ячейках и батареях.
Итак, оксиды металла воды имеют широкое применение в промышленности благодаря своим уникальным свойствам и химическим реакциям. Они используются в производстве керамики и стекла, в различных химических процессах в качестве катализаторов, а также в электронной и электротехнической промышленности.
Оксид металла вода: влияние на окружающую среду

Оксиды металлов, взаимодействуя с водой, могут оказывать как положительное, так и отрицательное влияние на окружающую среду.
Во-первых, некоторые оксиды металлов растворяются в воде с образованием кислот. Это может привести к изменению pH воды и нарушению ее химического и экологического баланса. Например, оксид серы взаимодействует с водой, образуя серную кислоту, которая является основной причиной кислотных дождей. Кислотные дожди вредны для окружающей среды, так как они негативно влияют на почву, водные экосистемы и живые организмы.
Во-вторых, некоторые оксиды металлов взаимодействуют с водой, образуя щелочные растворы. Например, оксид кальция реагирует с водой, образуя гидроксид кальция – вещество с щелочной реакцией. Такие щелочные растворы могут приводить к повышению pH воды и негативно влиять на ее экологическое состояние, особенно в акваториях с низкими значениями pH.
Оксиды металлов также могут быть токсичными для водных организмов. К примеру, оксиды железа и меди в определенных концентрациях являются ядовитыми для микроорганизмов и рыб. Это может приводить к нарушению биологического равновесия в водных экосистемах.
В целом, оксиды металлов взаимодействующие с водой могут оказывать существенное влияние на окружающую среду, поэтому необходимо проявлять осторожность при их использовании и утилизации, чтобы минимизировать негативные последствия.
Оксид металла вода: перспективы исследований
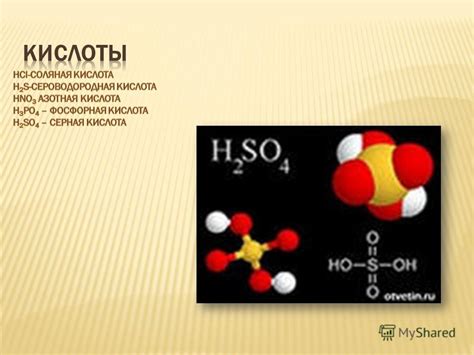
Оксид металла вода - это особый вид химического соединения, который образуется в результате взаимодействия металлического элемента с водой. Изучение свойств оксидов металлов воды в настоящее время представляет большой научный интерес.
Перспективы исследования оксидов металлов воды связаны с их возможным использованием в различных областях, включая энергетику, катализ и нанотехнологии. Благодаря своим уникальным свойствам, оксиды металлов воды могут стать эффективными катализаторами в различных химических реакциях.
Одним из направлений исследований является разработка новых методов синтеза оксидов металлов воды с контролируемыми свойствами. Это открывает возможности для создания новых материалов с улучшенными каталитическими и фотохимическими свойствами.
Исследование оксидов металлов воды также имеет большое значение для разработки новых энергетических технологий. Возможность использования оксидов металлов воды в солнечных батареях и системах водородного хранения может значительно повысить эффективность и устойчивость энергетических систем.
Таким образом, исследование оксидов металлов воды представляет собой актуальную и перспективную научную задачу, открытия в этой области могут привести к созданию новых материалов и технологий, которые будут иметь важное практическое значение.
Вопрос-ответ

Что такое оксид металла?
Оксид металла - это химичесное соединение, состоящее из металла и кислорода. Все металлы могут формировать оксиды, которые обладают различными свойствами и применяются в разных отраслях промышленности.
Какие свойства обладают оксиды металлов?
Оксиды металлов обладают различными свойствами в зависимости от типа металла и степени окисления. Они могут быть кислотными, щелочными или амфотерными. Некоторые оксиды металлов обладают электропроводностью и используются в качестве полупроводников. Оксиды металлов также могут обладать свойствами катализаторов и применяться в разных реакциях.
Какова роль оксидов металлов в природе?
Оксиды металлов играют важную роль в природе. Например, оксиды железа способствуют образованию ржавчины на металлических поверхностях, оксид алюминия является основным компонентом глины, а оксид кремния - главным компонентом песчаника. Оксиды металлов также широко распространены в минералах и играют важную роль в геохимических процессах.
