Оксид азота – вещество, которое обладает рядом интересных свойств. Многие ученые долгое время спорили о его химической природе. Некоторые считали оксид азота неметаллом, в то время как другие настаивали на его металлическом характере. Вплоть до сегодняшнего дня ведутся исследования, чтобы разрешить эту химическую загадку.
Оксид азота, обозначаемый формулой NO, состоит из одного атома азота и одного атома кислорода. Это газообразное вещество, которое обладает резким запахом и служит одним из ключевых компонентов атмосферного воздуха. Однако его химические свойства оказываются неоднозначными, что создает основание для дискуссий о его классификации.
Одни ученые считают оксид азота неметаллом, их аргументы основаны на его нековкой и недеформируемой структуре, а также отсутствии металлического блеска и характерного для металлов проводимости электричества и тепла. Однако другое мнение заключается в том, что оксид азота может быть металлом, так как он способен образовывать соли с кислотами и проявлять в реакциях свойства типичных металлов, например, способность образовывать ионы с положительной зарядом.
Существование споров о природе оксида азота демонстрирует сложность классификации химических соединений и проблемы, связанные с границами между неметаллами и металлами. И хотя на сегодняшний день не существует определенного ответа на этот вопрос, дальнейшие исследования и эксперименты позволят нам расширить наши знания и лучше понять природу оксида азота.
Оксид азота и его природа

Оксид азота – это химическое соединение, состоящее из атомов азота и кислорода. В его молекуле присутствуют два атома азота и один атом кислорода. Оксид азота имеет формулу NO.
Данное соединение обладает интересными свойствами и широко используется в различных областях. Оксид азота является одним из ключевых компонентов атмосферы Земли и играет важную роль в процессах, происходящих в атмосфере.
Оксид азота встречается как в природной среде, так и создается в результате физических и химических процессов. Он образуется в результате горения, воздействия молнии, а также в результате бактериального разложения органического вещества в почве и воде.
Одним из важных свойств оксида азота является его возможность взаимодействия с другими веществами. Это позволяет ему играть важную роль во многих химических реакциях и процессах в природе. Например, оксид азота играет ключевую роль в реакции воздействия на атмосферные соединения, которые влияют на формирование и разрушение озона в стратосфере.
- Оксид азота также широко используется в различных отраслях промышленности. Он применяется в производстве удобрений, в процессе очистки газов от загрязнений и в процессе синтеза органических соединений.
- Оксид азота имеет важное значение в медицине. Он используется в качестве медицинского газа для борьбы с инфекциями, снижения болевых ощущений и расширения дыхательных путей.
Таким образом, оксид азота представляет собой важное химическое соединение, которое играет значительную роль в различных процессах в природе и в области технологий. Его уникальные свойства делают его полезным во многих отраслях и помогают нам понять и контролировать некоторые природные процессы.
Неметалл в химическом составе
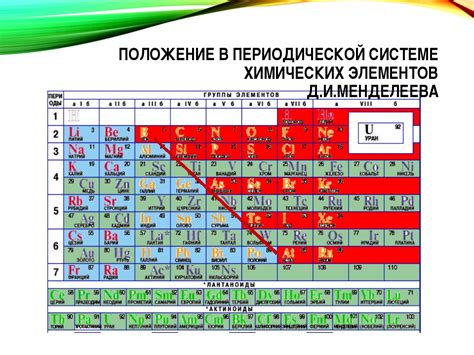
Оксид азота является неметаллом в своем химическом составе. Это соединение, состоящее из атомов кислорода и азота. Кислород и азот - это химические элементы, которые обычно классифицируются как неметаллы в периодической системе элементов.
Оксид азота имеет различные формы, такие как диоксид азота (NO2) и оксид азота (NO). Эти соединения образуются при реакции азота с кислородом в атмосфере или в промышленных процессах.
Оксид азота обладает некоторыми характеристиками неметаллов. Он обычно обладает непроводящими свойствами, не образует ионные связи и имеет низкую температуру плавления и кипения.
Однако, оксид азота также обладает характеристиками металлов. Он способен образовывать положительные и отрицательные ионы и может вступать в реакции с различными веществами. Эти свойства делают его важным в химической промышленности и в атмосферных процессах.
Реакции и свойства оксида азота

Оксид азота, также известный как азотная свинцовка (NO), является бесцветным газом с характерным запахом. Он обладает рядом уникальных свойств и способен взаимодействовать с другими веществами, образуя различные соединения.
Реакции оксида азота зависят от условий, в которых они происходят. При нормальных условиях оксид азота не реагирует с водой и воздухом, но при повышенных температурах может образовываться азотистая кислота (HNO3), которая является сильным окислителем.
Оксид азота также реагирует с металлами, образуя нитраты. Например, при взаимодействии с железом (Fe) образуется нитрат железа (Fe(NO3)2), а с калием (K) - нитрат калия (KNO3).
Оксид азота также может взаимодействовать с аммиаком (NH3) и образовывать аммонийный нитрат (NH4NO3), который широко используется в производстве удобрений и взрывчатых веществ.
В реакциях оксида азота образуются окислительно-восстановительные соединения, поскольку он может вступать как в окислительные, так и в восстановительные реакции. Например, оксид азота может участвовать в реакциях окисления металлов или восстановления других соединений.
Свойства оксида азота делают его важным веществом во многих промышленных процессах. Он используется в производстве кислорода, удобрений и взрывчатых веществ, а также в медицине для лечения различных заболеваний.
Применение в промышленности и медицине

Оксид азота, также известный как NO, имеет широкое применение в промышленности и медицине благодаря своим уникальным свойствам и действию на организм.
В промышленности оксид азота используется в качестве важного компонента в процессе производства азотной кислоты, которая в свою очередь используется для производства различных химических продуктов, таких как удобрения, пластик и взрывчатые вещества.
Кроме того, оксид азота играет важную роль в медицине. Врачи используют его для расширения сосудов и снижения кровяного давления у пациентов с артериальной гипертензией или сердечно-сосудистыми заболеваниями. Он также используется для облегчения дыхания у пациентов с астмой и хронической обструктивной болезнью легких.
Кроме того, оксид азота играет роль нейромедиатора в нервной системе и участвует в различных биологических процессах, таких как иммунная реакция и сексуальная функция. Он применяется в виде медикаментозных препаратов для лечения эректильной дисфункции у мужчин.
Главным образом, оксид азота находит свое применение как важное вещество в промышленности и медицине, благодаря своим уникальным свойствам и способности влиять на организм человека. Его использование является неотъемлемой частью многих отраслей и помогает улучшить качество жизни людей.
Взаимодействие оксида азота с окружающей средой

Оксид азота, химическая формула которого NO, взаимодействует с окружающей средой, вызывая различные последствия. Этот газ является одним из главных загрязнителей атмосферы и влияет на здоровье человека и экологическую ситуацию в целом.
Взаимодействие оксида азота с воздухом приводит к образованию атмосферного азотного диоксида (NO2). Присутствие этого вещества в воздухе негативно влияет на дыхательную систему человека и может вызывать астму, бронхит и другие заболевания. Нарушается также экологический баланс, так как NO2 является одним из главных компонентов смога.
Однако, окисление оксида азота в атмосфере также может приводить к образованию атмосферного азотной кислоты (HNO3). Это является причиной кислотных дождей, которые оказывают разрушительное воздействие на почву, растения и водные экосистемы. Загрязнение водных бассейнов кислотными дождями может привести к гибели рыб и другой водной фауны.
Взаимодействие оксида азота с влагой в атмосфере приводит к образованию азотных кислот, таких как азотная кислота и нитроусные кислоты. Эти соединения являются основными компонентами естественных и искусственных удобрений и оказывают положительное воздействие на растительный рост. В то же время, избыточное использование таких удобрений может привести к загрязнению почвы и грунтовых вод азотными соединениями.
Таким образом, взаимодействие оксида азота с окружающей средой оказывает как положительное, так и отрицательное воздействие. Уменьшение выбросов оксида азота в атмосферу и использование экологически чистых методов его переработки являются важными задачами для защиты окружающей среды и обеспечения экологической устойчивости.
Вопрос-ответ

Какие свойства обуславливают классификацию оксида азота как неметалла?
Оксид азота (NO) обладает неметаллическими свойствами, так как не образует ионные связи с другими элементами. Кроме того, оксид азота является газом при комнатной температуре и давлении, что также свидетельствует о его неметаллическом характере.
Что такое оксид азота и каково его значение в природе?
Оксид азота (NO) является неметаллическим соединением азота и кислорода. Он возникает в атмосфере в результате комбинации азота и кислорода при высоких температурах, например, при горении топлива. Оксид азота является одним из компонентов смога и кислотных дождей, и его избыток в атмосфере может оказывать вредное воздействие на окружающую среду и здоровье человека.
В чем заключается неметаллический характер оксида азота?
Неметаллический характер оксида азота обусловлен его химическими свойствами. Он не образует ионные связи с другими элементами, а образует ковалентные связи, в которых электроны общие между атомами азота и кислорода. Кроме того, оксид азота является газом при комнатной температуре и давлении, что также свидетельствует о его неметаллическом характере.
