Металлы - важная группа элементов, которые находят широкое применение в различных отраслях промышленности. Они обладают высокой проводимостью электричества и тепла, а также имеют прочность и долговечность. Однако, металлические конструкции могут подвергаться окислению, что может привести к их повреждению и разрушению. Для предотвращения окисления металлов применяются окислители, которые помогают защитить их от неблагоприятных воздействий окружающей среды.
Окислители металлов – это вещества, способные принять электроны от металла, при этом сами претерпевая восстановление. Они обладают высокой окислительной активностью и могут взаимодействовать с различными металлами, образуя комплексы и соли. В зависимости от своих свойств и химического состава, окислители металлов классифицируются на неорганические и органические. Неорганические окислители металлов обычно представляют собой кислоты, галогениды и оксиды, такие как хлориды, нитраты, пероксиды, азиды и прочие. Органические окислители, в свою очередь, содержат в своем составе органические соединения, такие как спирты, альдегиды, кетоны и другие органические функциональные группы.
Применение окислителей металлов позволяет не только предотвратить окисление самого металла, но и защитить его от коррозии и разрушения. Окислители металлов также могут использоваться для создания красивых и эстетических покрытий на металлической поверхности, таких как оксидные и патинированные покрытия. Однако, при использовании окислителей металлов необходимо учитывать их химические свойства и взаимодействие с конкретным металлом, чтобы избежать нежелательных последствий.
Вещества, окисляющие металлы: разновидности и применение

Окислители металлов — это вещества, которые способны отдавать электроны в химической реакции с металлами. Они являются активными реагентами и находят широкое применение в различных отраслях промышленности и научных исследованиях.
Одним из наиболее известных окислителей металлов является кислород. Он широко применяется в металлургической промышленности для образования оксидов металлов. Кислород также используется при горении металлов, что позволяет контролировать реакцию.
Еще одним важным окислителем металлов является хлор. Он активно используется в процессе хлорирования металлов, что позволяет изменить их свойства. Хлорирование позволяет улучшить стойкость к коррозии и повысить прочность металлов, делая их более применимыми в различных отраслях промышленности.
Различные соли тяжелых металлов, например, хлориды, являются эффективными окислителями для большинства драгоценных металлов. Они находят применение в гальваническом производстве, при создании покрытий и в других процессах, где требуется окисление металлов.
Кроме того, вещества, содержащие перекись водорода (водородные перекиси), также являются окислителями металлов. Они широко используются в аналитической химии и лабораторных исследованиях для определения концентрации металлов и их примесей.
Выводя различные металлы из активной зоны окружающей среды в окисленное состояние, окислители металлов играют важную роль в современных технологиях и науке. Их применение позволяет улучшить свойства металлов, получить новые соединения и обеспечить стабильность и безопасность в процессе производства.
Другое название окислителей металлов
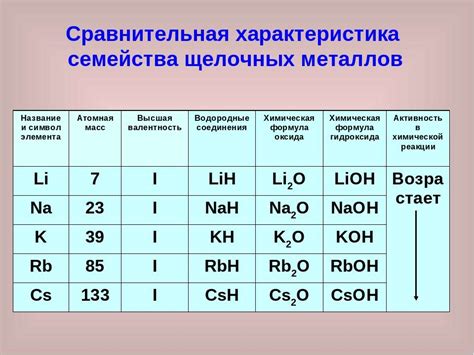
Окислители металлов также могут быть названы восстановителями или окислителями. Они играют важную роль в различных химических процессах, в том числе в окислительно-восстановительных реакциях. Восстановители вещества позволяют передавать электроны окислителю, при этом сами окисляются, а окислитель, наоборот, принимает электроны и при этом сам восстанавливается.
Другим названием для окислителей металлов может быть "электроактивные вещества". В этих веществах атомы металла имеют высокую степень окисления и способны передавать электроны другим веществам. Примером такого окислителя может быть кислород, который широко применяется в окислительных реакциях, например, при сгорании.
В окислителях металлов, помимо кислорода, можно сказать про озон, нитраты, перманганаты. Озон обладает высокой окислительной активностью и активно используется в химической промышленности. Нитраты и перманганаты также широко применяются в качестве окислителей, в том числе в аналитической химии.
Таким образом, помимо основных названий окислителей металлов, существует и другие термины, которые используются для обозначения этих веществ, в том числе "восстановители" и "электроактивные вещества". Это зависит от контекста и конкретной области применения окислителя.
Какие свойства имеют окислители металлов?
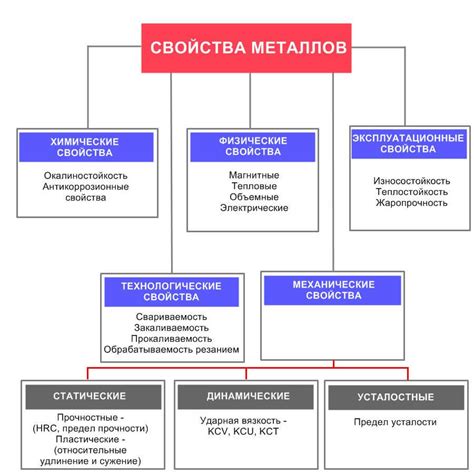
Окислители металлов - вещества, обладающие способностью окислять металлы, т.е. превращать их в соединения с более высокой степенью окисления. Они играют важную роль во многих процессах, таких как коррозия, реакции с кислородом и прочие окислительно-восстановительные реакции.
Некоторые свойства окислителей металлов:
- Высокая активность: Окислители металлов обладают большой электроотрицательностью, что позволяет им быть сильными окислителями. Они легко привлекают электроны от металлов, позволяя последним окислиться.
- Твердое состояние: Многие окислители металлов являются твердыми веществами с определенными кристаллическими структурами. Это обуславливает их способность вступать в реакции с поверхностями металлов.
- Высокая электроотрицательность: Окислители металлов обычно имеют высокую электроотрицательность, что позволяет им привлекать электроны от металлов и выполнить процесс окисления.
- Коррозионная активность: Окислители металлов могут быть активными в присутствии влаги, что может вызывать коррозию металлических поверхностей. Например, кислород воздуха или вода могут служить окислителями для различных металлов.
Важно помнить, что свойства окислителей металлов могут сильно различаться в зависимости от конкретного окислителя и металла, с которым они взаимодействуют. Поэтому при работе с окислителями металлов необходимо быть предельно внимательным и следовать соответствующим инструкциям и мерам безопасности.
Примеры окислителей металлов
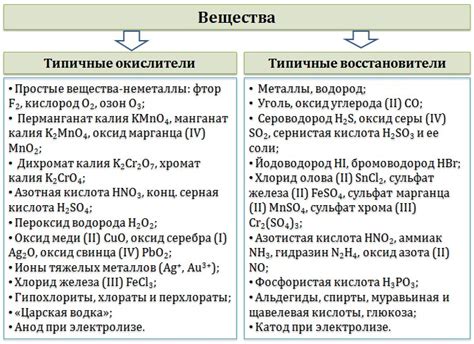
Окислители металлов - это вещества, способные принять электроны от металлов, вызывая их окисление. Некоторые из наиболее распространенных окислителей металлов находятся в нашей повседневной жизни и используются в различных областях. Вот несколько примеров:
- Кислород (O2) - Один из самых распространенных окислителей металлов. Кислород взаимодействует с металлической поверхностью, приводя к процессу окисления, который может привести к образованию ржавчины.
- Хлор (Cl2) - Также является сильным окислителем металлов. Хлор может реагировать с различными металлами, вызывая их окисление и образование соединений, таких как хлориды.
- Пероксиды (H2O2, Na2O2) - Эти вещества также могут быть использованы в качестве окислителей металлов. Например, пероксид водорода может реагировать с железом, вызывая его окисление и образование ржавчины.
- Хлорные кислоты (HClO3, HClO4) - Они являются очень сильными окислителями и могут реагировать с различными металлами, вызывая их окисление и образование ионов металла.
Это лишь некоторые примеры окислителей металлов, которые мы неоднократно встречаем в повседневной жизни. Различные окислители могут быть использованы в разных областях, включая химическую промышленность, металлургию, электроэнергетику и даже в бытовых товарах, таких как моющие средства и косметические продукты.
Окислители металлов в промышленности

В промышленности широко применяются различные окислители металлов, которые играют важную роль в процессах производства и преобразования материалов. Они позволяют ускорить химические реакции, повышить эффективность производства и получить желаемый результат.
Одним из наиболее распространенных окислителей металлов в промышленности является кислород. Кислород широко применяется в металлургии, где используется для окисления различных металлов, таких как железо, алюминий и медь. Окисление металла позволяет получить окись металла или его окисленные соединения, которые затем используются в процессах дальнейшей обработки.
Еще одним важным окислителем металлов является хлор. Хлор используется в промышленности для окисления железа и других металлов. Окись железа, полученная в результате реакции с хлором, может быть использована в процессе получения стали или других металлических сплавов.
Кроме того, в промышленности широко применяется пероксид водорода. Пероксид водорода используется как окислитель металлов при обработке поверхностей различных изделий. Он обладает высокой эффективностью и может быть использован для обработки металлических деталей, а также для удаления окалины.
Введение окислителей металлов в промышленное производство является неотъемлемой частью современных технологий. Они позволяют ускорить процессы производства, улучшить качество продукции и снизить затраты. Окислители металлов играют важную роль в различных отраслях промышленности, от металлургии до обработки поверхностей и создания новых материалов.
Помимо окислителей металлов: другие вещества, способные окислять металлы

Окислители металлов - это вещества, которые способны выделять кислород и передавать его на металлы, вызывая их окисление. Такие вещества широко применяются в различных отраслях промышленности и научных исследованиях. Однако помимо окислителей металлов, существуют и другие вещества, которые также могут проявлять окислительные свойства по отношению к металлам.
Хлориды - это класс соединений, которые содержат в своей составе ион хлора. Некоторые хлориды, такие как хлорид натрия или хлорид алюминия, способны служить окислителями металлов. Они могут реагировать с металлами, выделять кислород и вызывать окисление металлической поверхности. Например, хлорид натрия может быть использован в электролизе для окисления алюминия.
Пероксиды - это класс соединений, содержащих в своей молекуле группу пероксид (-O-O-). Некоторые пероксиды, такие как водородный пероксид (водик), способны служить окислителями металлов. Они могут реагировать с металлами, отдавая кислород и вызывая окисление металлической поверхности. Например, водородный пероксид может использоваться для окисления железа или меди.
Озон - это разновидность кислорода, состоящая из трех атомов (O3). Озон является очень активным окислителем и может реагировать с многими веществами, включая металлы. Он способен вызвать окисление металлической поверхности и образование оксидов металлов. В результате таких реакций металлический предмет может изменить свою цветность или поверхностные свойства.
Аммиак - это химическое соединение, которое широко используется в промышленности. В некоторых случаях аммиак может выступать в качестве окислителя металлов. Он может активно реагировать с определенными металлами, такими как железо или никель, образуя соединения, содержащие аммиак. Такие реакции могут вызывать окисление металла и изменение его свойств.
Влияние окислителей металлов на окружающую среду

Окислители металлов играют существенную роль не только в процессах производства, но и в окружающей среде. Взаимодействие окислителей металлов с окружающей средой может привести к серьезным последствиям, включая загрязнение воды, почвы и атмосферы, а также угрозу для здоровья людей и животных.
Окислители металлов, попадая в окружающую среду, могут вызывать окисление органических веществ и образование токсичных соединений. Также они могут приводить к изменению температуры, рН-уровня и электропроводности водных и почвенных сред, что негативно сказывается на жизни и развитии микроорганизмов, растений и животных.
Более того, некоторые окислители металлов могут быть ядовитыми для человека и вызывать различные заболевания, включая проблемы с дыхательной системой, печенью и почками. Поэтому контроль и ограничение выброса окислителей металлов в окружающую среду является одной из главных задач в современной экологии и промышленности.
Для снижения негативного влияния окислителей металлов на окружающую среду могут применяться различные меры. Контроль и очистка выбросов, использование более безопасных и экологически чистых окислителей, а также разработка и внедрение новых технологий обработки и утилизации отходов могут помочь минимизировать эффекты негативного воздействия на окружающую среду и обеспечить устойчивое развитие промышленности и общества в целом.
Вопрос-ответ

Какие окислители металлов существуют?
Существует множество окислителей металлов. Некоторые из них включают хлор, бром, пероксид водорода, хлоридно-бромистые смеси, цианистый натрий и другие.
Для чего используются окислители металлов?
Окислители металлов используются в различных отраслях промышленности, например, в процессах гальванизации, при производстве химических соединений, при очистке воды и в других технологических процессах. Они также могут использоваться в лабораториях для различных химических реакций и исследований.
Как выбрать правильный окислитель для нужного процесса?
Выбор правильного окислителя для нужного процесса зависит от нескольких факторов, таких как тип металла, который необходимо окислить, окружающие условия (температура, давление и т.д.), требуемая степень окисления и другие. Что бы выбрать подходящий окислитель, рекомендуется обратиться к специалистам в данной области или консультантам, которые смогут предоставить рекомендации на основе ваших специфических требований.
