Серная кислота, также известная как сульфатная кислота, является одним из важнейших химических соединений, которые могут взаимодействовать с металлами. Эта кислота имеет формулу H2SO4 и образуется путем окисления сероводорода. Серная кислота является сильным кислотным окислителем, и поэтому ее реактивность с металлами может быть довольно высокой.
Одним из общих свойств серной кислоты с металлами является их растворимость. Большинство металлов могут растворяться в серной кислоте при образовании солей, известных как сульфаты. Растворимость металлов в серной кислоте зависит от их активности и степени окисления.
Серная кислота также может быть использована в качестве окислителя при реакциях с металлами. Например, она может окислять металлический водород до воды. Это может быть полезно в различных промышленных процессах, таких как производство водорода.
Серная кислота также может реагировать с металлическими оксидами и гидроксидами, образуя соответствующие соли. Однако стоит отметить, что не все металлы реагируют с серной кислотой одинаково. Некоторые металлы могут проявлять поведение, характерное для щелочей, при взаимодействии с серной кислотой.
В целом, взаимодействие серной кислоты с металлами является сложным процессом, и его результат может зависеть от ряда факторов, включая физические и химические свойства металла, его степень окисления и концентрацию серной кислоты. Изучение этих свойств позволяет не только лучше понять химические взаимодействия, но и найти применение серной кислоте в различных областях, включая промышленность и науку.
Основные свойства серной кислоты
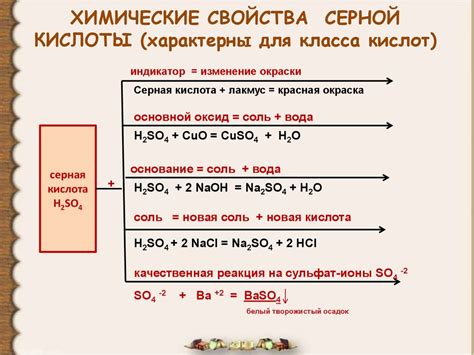
1. Кислотность: Серная кислота является сильной кислотой, что означает, что она легко отдает протоны в водном растворе. В результате образуется ион водородная серная кислота (H2SO4), который может реагировать с различными соединениями и образовывать соли.
2. Окислительные свойства: Серная кислота обладает окислительными свойствами и может взаимодействовать с многими веществами, в том числе с некоторыми металлами. При этом она сама может действовать как окислитель, отдавая кислород и принимая электроны.
3. Деструктивное действие: Серная кислота обладает сильным деструктивным действием. Она может разлагать органические вещества, такие как древесину, сахара, белки и другие, при этом образуя различные продукты.
4. Образование солей: Взаимодействуя со многими металлами, серная кислота образует соли. При этом ион водородной серной кислоты H2SO4 может замещаться ионом металла, образуя соответствующий соль.
5. Концентрация: Серная кислота может присутствовать в разных концентрациях, от разбавленных растворов до концентрированной серной кислоты. Зависимо от концентрации, она может проявлять различную химическую активность и иметь разные физические свойства.
6. Важное применение: Серная кислота широко используется в промышленности, включая производство удобрений, пределывание текстильных волокон, очистку металлов и др. Ее применение связано с ее кислотными, окислительными и деструктивными свойствами.
Взаимодействие с металлами
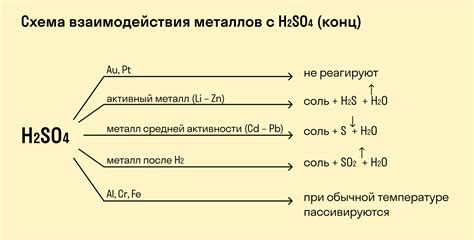
Серная кислота обладает высокой реакционной способностью с металлами. Взаимодействие с металлами происходит путем образования солей серной кислоты. Соли серной кислоты, или сульфаты, являются широко распространенным классом химических соединений.
Взаимодействие металлов с серной кислотой можно наблюдать на примере реакции с цинком. В результате этой реакции образуется сульфат цинка и выделяется молекулярный водород. Реакция проходит с выделением тепла и довольно быстро.
Кроме цинка, реакцию с серной кислотой способны претерпевать и другие металлы, такие как железо, медь и алюминий. При этом некоторые металлы, например медь, реагируют с серной кислотой гораздо медленнее, и для развития реакции может потребоваться нагревание смеси.
Реакция металлов с серной кислотой может протекать как в жидкой, так и в газообразной фазе. При этом, в газообразной фазе реакция между металлами и серной кислотой приводит к образованию сернистого газа. Этот газ обладает характерным запахом и является ядовитым.
Вопрос-ответ

Какие свойства серной кислоты делают её реактивным соединением с металлами?
Серная кислота обладает высокой кислотностью и окислительными свойствами, что позволяет ей активно реагировать с металлами. Кислый характер серной кислоты обусловлен наличием в ее структуре кислородных атомов, способных принимать электроны от металла, образуя ионы сернатой кислоты. Также серная кислота является сильным окислителем, способным окислять металлы и образовывать с ними соответствующие сульфаты.
Какие особенности реакции серной кислоты с металлами можно выделить?
Реакция серной кислоты с металлами протекает с образованием сульфатов металлов и выделением сероводорода. Это позволяет использовать реакцию серной кислоты с металлами для получения сероводорода в промышленных масштабах. Реакция обычно проходит достаточно быстро и сопровождается выделением тепла. Взаимодействие серной кислоты с металлом может приводить к коррозии металлических поверхностей.
Какие факторы влияют на скорость реакции серной кислоты с металлами?
Скорость реакции серной кислоты с металлами зависит от нескольких факторов, таких как концентрация кислоты, температура, площадь поверхности металла и наличие катализаторов. Повышение концентрации серной кислоты и повышение температуры обычно ускоряют реакцию. Увеличение площади поверхности металла также может способствовать более быстрой реакции. Наличие катализаторов может увеличить скорость реакции и снизить температуру, необходимую для ее протекания.
