Электролиз является одним из основных методов получения металлов. Благодаря этому процессу можно разделять и очищать различные компоненты, а также извлекать металлы из их минеральных руд. Процесс электролиза основывается на применении электрического тока для вызывания химических реакций и переноса зарядов через электролит.
Один из наиболее распространенных способов получения металлов электролизом является гальваническое осаждение. В этом процессе металлы осаждается на поверхности электрода из раствора, содержащего соответствующие ионы металла. Этот метод используется в различных отраслях, таких как производство ювелирных изделий, электронная промышленность и многие другие.
Электролиз также широко используется в процессе производства алюминия. Этот металл получают из боксита, который содержит оксид алюминия. Процесс электролиза включает в себя использование электродов из углеродных материалов, которые погружены в раствор электролита. Под действием электрического тока оксид алюминия распадается на металлический алюминий и кислород.
Металлы электролиз: общие способы получения металлов и электролиз

Металлы являются важным компонентом современной промышленности. Их широко используют в различных отраслях, начиная от строительства и машиностроения до электроники и автомобильного производства. Существует несколько способов получения металлов, один из которых - это электролиз.
Электролиз представляет собой процесс разложения вещества под действием постоянного электрического тока. В процессе электролиза происходит трансформация ионов металла из положительного полюса - анода, на отрицательный полюс электрода - катод. Таким образом, металлы получаются в результате редукции ионов на катоде.
Одним из ключевых условий успешного электролиза является выбор подходящей электролитической среды. В зависимости от химических свойств металла, для электролиза могут использоваться различные соли, кислотные или щелочные огнетушители. Также для обеспечения эффективного электролиза необходимы определенные условия, такие как температура, концентрация и скорость потока электролита.
Преимущества электролиза в получении металлов включают высокую чистоту и качество полученного продукта. Также, электролиз является процессом, который может быть легко контролируемым и масштабируемым. Однако, электролиз требует значительных энергетических затрат, что может быть недостатком для его применения в некоторых случаях.
Способы получения металлов
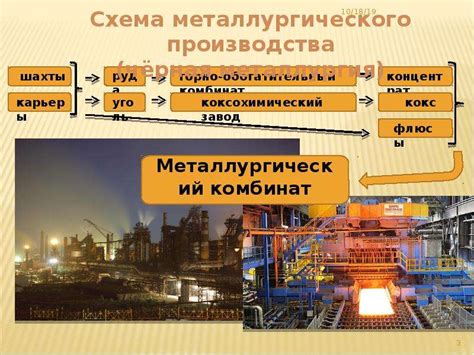
Металлы являются одним из основных видов материалов, используемых в различных отраслях промышленности. Для получения металлов существуют различные способы, которые зависят от их свойств, особенностей добычи и обработки.
Одним из основных способов получения металлов является добыча из природных руд. Этот метод используется для получения таких металлов, как железо, алюминий, свинец, цинк и другие. Для этого проводится дробление руды, ее обогащение и последующая переработка с использованием различных химических процессов.
Важным способом получения металлов является также электролиз, который применяется для получения ряда металлов, в том числе алюминия, меди, никеля и других. Электролиз основан на использовании электрической энергии для разделения соединений металлов на ионы и их последующего осаждения на электроды.
Другим способом получения металлов является плавка, которая применяется для преобразования металлических руд или сплавов в жидкое состояние при высоких температурах. Плавка позволяет получать такие металлы, как золото, серебро, медь и другие.
Также существует способ получения металлов с помощью химической реакции, например, через взаимодействие металлических солей с веществами, которые способны осаждать металлы. Этот метод позволяет получать металлы высокой чистоты и широко используется в производстве электроники и других отраслях.
Металлы и их физические свойства
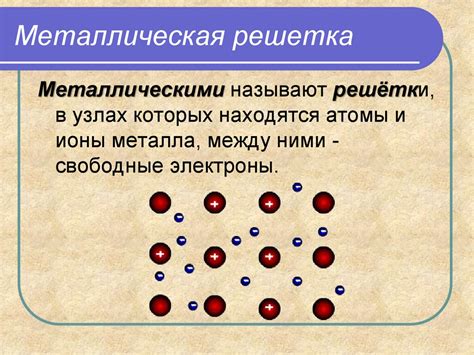
Металлы - это класс материалов, обладающих определенными физическими свойствами. Одной из основных характеристик металлов является их электропроводность. Металлы обладают большим количеством свободных электронов, которые легко двигаются по материалу, позволяя электрическому току свободно проходить через металлическую проводниковую сеть.
Другим важным свойством металлов является их теплопроводность. Металлы способны эффективно передавать тепло, что делает их идеальными материалами для использования в теплотехнических системах и приборах.
Металлы также обладают механической прочностью и жесткостью. Они способны выдерживать большие нагрузки и оставаться устойчивыми при деформациях. Это делает металлы незаменимыми материалами для строительных конструкций, автомобильных деталей и других механических устройств.
Интересной особенностью металлов является их способность формировать сплавы. Металлы могут сочетаться с другими металлами, образуя материалы с новыми свойствами. Сплавы широко используются в различных отраслях, включая машиностроение, химическую промышленность и электротехнику.
Электролиз в химических процессах
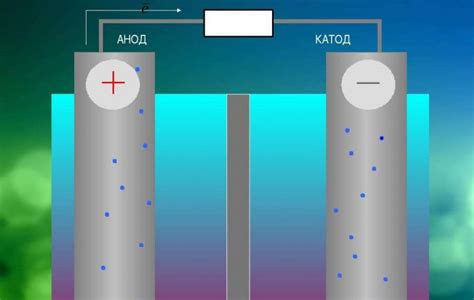
Электролиз – это процесс разложения веществ с использованием электрического тока. Он является основным методом получения многих металлов и химических веществ. В химических процессах электролиз используется для синтеза различных соединений, очистки растворов от примесей и извлечения полезных продуктов.
В процессе электролиза используются два электрода: катод и анод. Катод – это отрицательно заряженный электрод, на который переносятся положительно заряженные ионы, а анод – это положительно заряженный электрод, на который переносятся отрицательно заряженные ионы. Под действием электрического тока происходит окисление или восстановление вещества в растворе на электродах.
Электролиз в химических процессах широко применяется в различных отраслях промышленности. Например, в процессе хлорирования с помощью электролиза получают хлор и щелочь. Также электролиз используется для получения алюминия, меди, цинка и других металлов. Кроме того, он применяется в синтезе органических соединений, электрохимическом выделении металлов из руд и растворов, а также в процессе очистки воды и сточных вод от загрязнений.
При электролизе важными параметрами являются электрический ток, время действия тока, концентрация раствора и свойства электродов. Они оказывают влияние на эффективность процесса, скорость образования продукта, качество получаемых веществ и экономическую эффективность.
Применение электролиза в промышленности
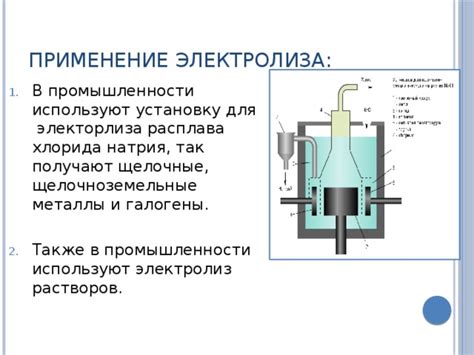
Электролиз является важным процессом, который широко применяется в различных отраслях промышленности. В процессе электролиза металлы получают путем разложения их соединений с помощью электрического тока. Это позволяет получить высокочистые металлы для использования в различных промышленных процессах.
Одним из ключевых применений электролиза является получение алюминия. Алюминий является одним из самых распространенных металлов в мире и широко применяется в промышленности, особенно в производстве авиационных и автомобильных компонентов. Процесс электролиза позволяет получить высококачественный алюминий из бокситовых и глиноземистых руд.
Кроме алюминия, электролиз применяется для получения других металлов, таких как никель, цинк и медь. Например, в процессе электролиза из руды никеля можно получить высокочистый никель, который используется в производстве нержавеющей стали, аккумуляторов и многих других продуктов.
Электролиз также применяется в производстве хлора и щелочей. При электролизе солевых растворов получают хлор и единицы. Хлор применяется в производстве пластмасс, резин, одеял и дезинфицирующих средств, а щелочи используются в качестве промышленных химикатов и в процессе очистки воды.
Кроме того, электролиз используется для получения аккумуляторов, электрометаллургической и электрохимической обработки, а также в других процессах, связанных с производством и переработкой металлов. Таким образом, электролиз играет важную роль в промышленности и позволяет получить металлы высокой чистоты, что открывает широкие возможности для использования их в различных сферах.
Процесс электролиза в качестве примера

Электролиз – это процесс, в ходе которого разложение проводников электрического тока происходит под действием электрической энергии. Одним из примеров электролиза является получение металлов. Данный процесс основан на использовании электролитических реакций и позволяет получить металлы высокой чистоты.
В качестве электролита при электролизе металлов обычно используют соли, растворенные в воде или других растворителях. Электролиты содержат ионы металлов, которые перемещаются под действием электрического тока. Этот процесс называется электродвижением.
Во время электролиза в растворе происходит разделение на два электрода. Положительный электрод называется анодом, а отрицательный – катодом. На аноде происходит окисление, а на катоде – восстановление. Между анодом и катодом протекает электрический ток, который стимулирует протекание электролитической реакции.
В результате электролиза, на катоде получают чистый металл, а на аноде образуется соединение этого металла. Для каждого металла существует свой определенный способ электролиза, который зависит от его химических свойств. Электролиз позволяет получить металлы высокой степени очистки, что делает его часто используемым методом производства металлов.
Вопрос-ответ

Какие способы существуют для получения металлов?
Существуют различные способы получения металлов, включая экстракцию из руды, электролиз и термохимические методы. Каждый способ имеет свои особенности и применяется в зависимости от типа металла и условий процесса.
Что такое электролиз?
Электролиз - это процесс разложения вещества под действием электрического тока. В результате электролиза могут образовываться различные продукты, в том числе металлы.
Как происходит электролиз и какие реакции происходят?
Электролиз происходит в электролитической ячейке, состоящей из двух электродов - анода и катода, погруженных в электролит. При подаче электрического тока анод окисляется, а катод восстанавливается. В результате этих процессов происходит разложение раствора и образование металлического осадка на катоде.
Каким образом электролиз используется для получения металлов?
В процессе электролиза металлические ионы в растворе притягиваются к катоду под воздействием электрического тока и образуют металлический осадок. Таким образом, металлы можно получать из растворов, содержащих их ионы.
Какие примеры применения электролиза для получения металлов можно привести?
Один из примеров применения электролиза для получения металлов - это получение алюминия из руды бокситов. При этом катодом служит графитовый стержень, а анодом - алюминиевый оксид. Под воздействием электрического тока происходит разложение оксида и образование металлического алюминия на катоде.
