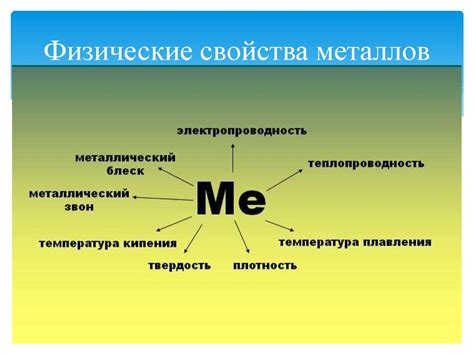
Металлы - это класс веществ, который обладает специфическими физическими и химическими свойствами. Одной из важнейших характеристик металлов является их способность образовывать металлическую связь, которая обусловливает особые физические свойства, такие как высокая теплопроводность и электропроводность, пластичность и деформируемость.
Металлическая связь проявляется в таких свойствах металлов, как проводимость электричества и тепла. Атомы металлов образуют кристаллическую решетку, где каждый атом окружен несколькими соседними атомами. Между атомами металлов имеются свободные электроны, которые способны свободно перемещаться по кристаллической решетке. Это обуславливает высокую электропроводность металлов, поскольку электроны могут легко передвигаться на большие расстояния без существенных потерь энергии.
Металлы также обладают высокой теплопроводностью благодаря металлической связи. При нагреве металла энергия передается от одних атомов к другим через свободные электроны, что позволяет энергии мгновенно распространяться по всему материалу. Именно поэтому металлы часто используются в технологии, где важна передача тепла, например, в изготовлении теплообменников и охладителей.
Металлическая химическая связь и ее роль

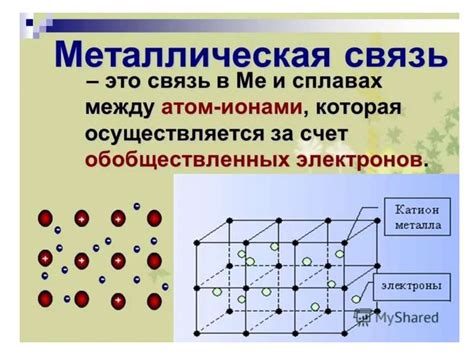
Металлическая химическая связь - это тип химической связи, характерный для металлов, в результате которой образуется кристаллическая решетка, состоящая из положительно заряженных ионов металла и свободных электронов.
Одной из основных характеристик металлической химической связи является свободное движение электронов между атомами металла. Это обуславливает такие физические свойства металлов, как высокая электропроводность и теплопроводность.
Металлы обладают металлическим блеском благодаря отражению света свободными электронами, а также пластичностью и проволочностью из-за способности электронов смещаться без препятствий в кристаллической решетке.
Металлическая химическая связь также влияет на плавление и кипение металлов. Благодаря слабости взаимодействия электронов с атомами металла в кристаллической решетке, металлы имеют низкую температуру плавления и кипения по сравнению с другими типами химических связей.
Роль металлической химической связи в природе и технологии трудно переоценить. Она определяет множество свойств металлов, что делает их необходимыми материалами для производства различных изделий и конструкций.
Структура металлов и ее связь с металлической химической связью
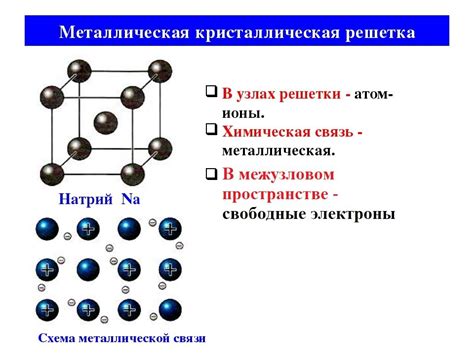
Металлы характеризуются особой структурой, которая обусловлена металлической химической связью, основой которой являются свободные электроны.
Структура металлов основана на кристаллической решетке, которая образуется в результате упорядоченного расположения атомов металла. Каждый атом в решетке имеет несколько ближайших соседей, к которым он привязан металлической связью.
Металлическая химическая связь характеризуется высокой подвижностью электронов в металле. Каждый атом в металле отдает один или несколько электронов для общего использования. Эти свободные электроны, называемые электронами проводимости, перемещаются по всей структуре металла, создавая электронный облако.
Структура металлов и их особенности, обусловленные металлической химической связью, придают металлам ряд характерных физических свойств. К таким свойствам относятся высокая электропроводность, хорошая теплопроводность, пластичность и хорошая изгибаемость.
Металлы также обладают выраженным металлическим блеском и способностью отражать свет. Это связано с тем, что свободные электроны в металле могут поглощать и переизлучать энергию света.
Проводимость и электрические свойства металлов
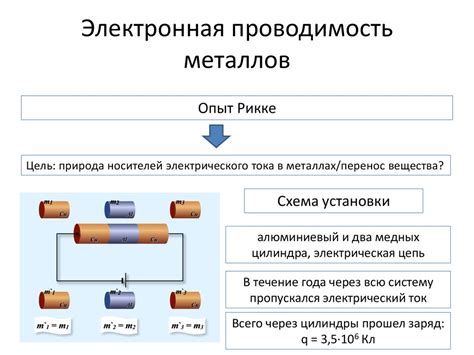
Проводимость - одно из основных электрических свойств металлов. Она характеризует способность материала передавать электрический ток. В отличие от неметаллических материалов, у металлов проводимость очень высокая.
Проводимость металлов обусловлена наличием свободных электронов, которые могут легко перемещаться по кристаллической решетке. Металлическая химическая связь характеризуется деликатным взаимодействием между атомами, что позволяет электронам двигаться без сопротивления, создавая электрический ток.
Следует отметить, что проводимость металлов сильно зависит от температуры и структуры кристаллической решетки. При понижении температуры, как правило, проводимость увеличивается, так как уменьшается число фононов - колебаний кристаллической решетки, что уменьшает вероятность рассеяния электронов.
Электрические свойства металлов также могут варьироваться в зависимости от примесей и процессов легирования. Например, присутствие определенных примесей может уменьшать проводимость металла, делая его полупроводником, или увеличивать его проводимость, делая его сверхпроводником.
Теплоотдача и термические свойства металлов
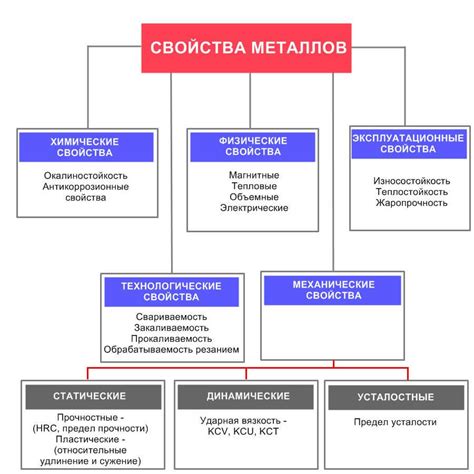
Теплоотдача - одно из важнейших свойств металлов, определяющее их способность передавать тепло. Металлы обладают высокой теплоотдачей благодаря наличию свободных электронов, которые могут легко перемещаться и переносить тепловую энергию.
Одним из физических свойств металлов, связанных с теплоотдачей, является их теплопроводность. Теплопроводность - это способность материала проводить тепло при тепловом движении электронов и атомов. Металлы обладают высокой теплопроводностью благодаря наличию свободных электронов, которые принимают участие в процессе теплопроводности.
Теплоемкость - это количество теплоты, необходимой для нагрева одной единицы массы материала на определенную температуру. Металлы обладают высокой теплоемкостью, что обусловлено большим количеством частиц, которые могут поглощать и хранить теплоту.
Одним из интересных явлений, связанных с теплоотдачей металлов, является их термическое расширение. В процессе нагрева металлы расширяются, а при охлаждении сужаются. Это связано с изменением температуры и колебаниями атомов в решетке металла.
Суммируя вышесказанное, можно сделать вывод, что металлы обладают высокой теплоотдачей, что делает их эффективными материалами для передачи и распределения тепла. Их высокая теплопроводность и теплоемкость способствуют эффективному передаче теплоты в различных процессах, а термическое расширение позволяет использовать металлы в различных конструкциях с учетом их изменений при изменении температуры.
Механические свойства и прочность металлов

Металлы обладают высокой прочностью благодаря особенностям их механических свойств. Главной характеристикой металлов является их прочность, которая определяет способность материала сопротивляться внешним нагрузкам без разрушения. Прочность металла зависит от его структуры, наличия дефектов, тепловой обработки и других факторов.
Металлы могут быть трех видов прочности: тяговой, сжатой и сдвигающейся. Тяговая прочность показывает, на какую силу металл способен сопротивляться растяжению. Сжатая прочность, в свою очередь, определяет способность металла сопротивляться сжатию. А прочность на сдвиг показывает, насколько материал устойчив к разрушению при действии сдвиговых нагрузок.
Прочность металлов обусловлена их металлической химической связью, которая обеспечивает высокую степень упорядоченности атомов в кристаллической решетке. Металлическая связь позволяет атомам легко сдвигаться друг относительно друга без разрушения связи, что делает металлы гибкими и деформируемыми материалами.
Основными факторами, влияющими на прочность металлов, являются кристаллическая структура и взаимное расположение атомов, а также деформация материала при воздействии нагрузки. Изменение структуры и состава металла может приводить к существенному изменению его механических свойств, включая прочность.
Важным параметром, характеризующим прочность металлов, является предел текучести. Предел текучести определяет максимальную деформацию материала без его разрушения. Материал, превысивший предел текучести, начинает образовывать трещины и отказываться. Поэтому предел текучести является важным показателем для оценки прочности и надежности металлических конструкций.
Коррозионная стойкость металлов
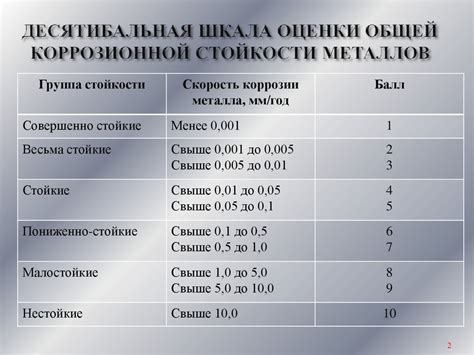
Коррозия - это процесс разрушения металлов под воздействием окружающей среды. Длительный контакт металла с водой, воздухом, кислотами, солями и другими химическими веществами может привести к его окислению и последующей деградации. Однако, металлы имеют разную стойкость к коррозии в зависимости от их химической связи.
Металлы, обладающие ионными связями, такие как натрий и калий, обычно обладают низкой коррозионной стойкостью. Ионные связи легко разрушаются под воздействием воды и кислот, что приводит к быстрому окислению и разрушению металла.
Металлы с ковалентной связью, такие как углерод или кремний, обычно имеют более высокую коррозионную стойкость. Ковалентная связь более прочна и устойчива к воздействию различных химических веществ, поэтому металлы такой структуры обычно менее подвержены коррозии.
Однако, наиболее стойкими к коррозии являются металлы с металлической связью, такие как алюминий, магний или железо. Металлическая связь обеспечивает высокую прочность и устойчивость металла к различным факторам окружающей среды. Более того, такие металлы часто покрывают тонкой пленкой оксида, которая служит дополнительной защитой от коррозии.
Для улучшения коррозионной стойкости металлов различные процессы обработки и покрытия могут быть использованы. Например, металлы могут быть покрыты защитными покрытиями, такими как хром или никель, которые образуют прочную и стойкую к коррозии пленку на поверхности. Также, металлы могут быть легированы другими элементами, чтобы улучшить их химическую стойкость к коррозии.
Влияние металлической химической связи на пластичность металлов
Металлическая химическая связь имеет значительное влияние на пластичность металлов, то есть их способность деформироваться без разрушения при воздействии внешних сил. Пластичность является одной из важнейших физических свойств металлов, определяющих их успех в промышленности.
Металлы обладают специфической структурой, состоящей из кристаллической решетки, в которой атомы металла занимают позиции узлов. Металлическая связь, образующаяся между этими атомами, характеризуется высокой энергией связи и особыми электронными свойствами.
Проявление пластичности металлов связано с особенностями металлической связи. В результате внешнего воздействия, например, при нагревании или деформации, атомы металла сдвигаются друг относительно друга, сохраняя при этом контакт и электронную связь. Это позволяет металлам обладать высокой пластичностью, то есть способностью формирования сложных деформаций без разрушения.
Металлическая связь придает металлам такие важные свойства, как проводимость электричества и тепла, а также возможность образования направленных кристаллов при охлаждении. Однако, она также оказывает некоторое влияние на другие свойства металлов, такие как твердость и пластичность. Изменение химической связи или структуры металла может привести к изменению его механических свойств и использованию в различных сферах человеческой деятельности.
Ферромагнетизм и физические свойства магнитных металлов
Ферромагнетизм - это явление, при котором некоторые металлы обладают способностью намагничиваться во внешнем магнитном поле и удерживать полученную намагниченность после прекращения воздействия поля. Магнитные металлы, такие как железо, никель, кобальт, обладают уникальными физическими свойствами, которые определяют их способность к ферромагнетизму.
Одной из важных характеристик магнитных металлов является их кристаллическая структура. Так, в железе и никеле присутствует кубическая решетка, в которой атомы металла располагаются в упорядоченном порядке. Это обеспечивает создание идеальных условий для образования магнитного момента и спиновой ориентации электронов.
В магнитных металлах сильно выражена взаимодействие между атомами, вызванное металлической химической связью. Это приводит к переходу электронов между атомами и формированию спиновых структур с выровненными магнитными моментами. Отличительной особенностью магнитных металлов является наличие доменной структуры, представляющей собой упорядоченное расположение областей с одинаковой направленностью магнитного момента.
Магнитные металлы обладают рядом физических свойств, связанных с их ферромагнетизмом. Например, они обладают высокой магнитной проницаемостью, что означает, что они хорошо пропускают магнитные линии силы. Кроме того, магнитные металлы обладают низкой коэрцитивной силой, то есть они легко намагничиваются и демагнитизируются.
Ферромагнетизм и физические свойства магнитных металлов играют важную роль в различных промышленных и технологических процессах. Эти материалы используются в производстве перманентных магнитов, электромагнитных устройств, электромагнитных усилителей и других устройств, где требуется использование магнитных свойств металлов.
Вопрос-ответ

Какая роль металлической химической связи в физических свойствах металлов?
Металлическая химическая связь играет ключевую роль в формировании физических свойств металлов. Она обеспечивает высокую электропроводность, теплопроводность и пластичность металлов.
Какие свойства металлов определяются металлической химической связью?
Металлическая химическая связь определяет такие свойства металлов, как высокая электропроводность, теплопроводность, пластичность и металлический блеск. Она также обуславливает способность металлов образовывать кристаллическую решетку с ионами положительного заряда, которая обладает высоким механическим прочтстом.
