Переходные металлы - это группа химических элементов, которая включает в себя элементы с атомными номерами от 21 до 30, от 39 до 48 и от 57 до 80. Основными представителями этой группы являются железо, медь, цинк, никель, хром и многие другие. Они получили свое название из-за своей способности образовывать комплексные соединения, в которых металл образует связь с лигандами - атомами, ионами или молекулами, окружающими металл и образующими структуру комплекса.
Комплексные соединения переходных металлов обладают множеством интересных свойств и находят широкое применение в различных областях, таких как катализ, медицина, электрохимия и технология материалов. Они могут иметь различные структуры и формы, их цвет может варьироваться от безцветного до ярко окрашенного.
Одной из основных характеристик переходных металлов и их комплексных соединений является возможность образования различных степеней окисления. Это означает, что переходные металлы могут образовывать ионы с разным количеством электронов, отданных или принятых металлом. Это свойство позволяет им образовывать различные соединения и участвовать в различных реакциях.
Исследование переходных металлов и их комплексных соединений имеет большую практическую значимость и является активной областью научных исследований. Понимание их основных характеристик и свойств может привести к разработке новых материалов и катализаторов, которые могут быть использованы для решения различных проблем и задач в химической промышленности и других областях науки и техники.
В этой статье мы рассмотрим основные характеристики переходных металлов и их комплексных соединений, а также их приложения и значимость в современном мире.
Переходные металлы: определение и классификация
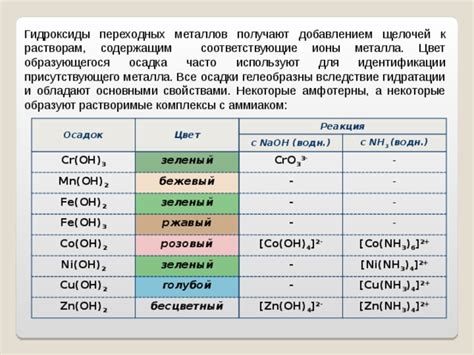
Переходные металлы - это элементы д-блока периодической системы химических элементов, которые обладают особенностями в строении своих атомных и электронных орбиталей. Они имеют неполный внешний электронный слой, что делает их активными в химических реакциях.
Переходные металлы подразделяются на несколько классов в зависимости от электронной конфигурации и химических свойств.
Первый класс переходных металлов включает элементы, у которых валентные электроны заполняют последовательно d-подуровни. К ним относятся титан, ванадий, хром, марганец, железо, кобальт и никель. Они обладают различными степенями окисления и могут образовывать стабильные соединения с разными анионами и молекулами.
Второй класс переходных металлов составляют элементы, у которых валентные электроны заполняют s- и d-орбитали. Это элементы из группы цинка, стронция, иттрия, циркония, ниобия, молибдена, технеция, рутения, родия, палладия, серебра и кадмия. Их соединения обладают специфическими свойствами и широко применяются в различных отраслях науки и техники.
Третий класс переходных металлов состоит из элементов, у которых валентные электроны заполняют s-, d- и f-орбитали. К этой группе относятся элементы из серии лантаноидов и актиноидов. Их соединения имеют особые магнитные и оптические свойства, а также находят применение в качестве катализаторов и активных веществ в различных химических преобразованиях.
Характеристики переходных металлов
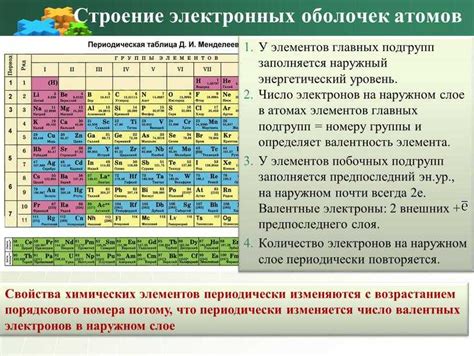
Переходные металлы - это элементы D-блока периодической системы химических элементов. Они обладают особыми характеристиками, которые делают их уникальными и полезными в различных областях науки и промышленности. Вот некоторые из основных характеристик переходных металлов:
- Валентность: Переходные металлы имеют различные степени окисления и способность образовывать соединения с различными валентностями. Это позволяет им образовывать разнообразные комплексы с другими атомами и ионами.
- Электронные конфигурации: Переходные металлы имеют неполностью заполненные D-подуровни, что делает их способными к образованию комплексов с лигандами. Это обусловлено наличием ненасыщенности в D-электронной оболочке.
- Катализаторы: Многие переходные металлы обладают каталитической активностью, что делает их ценными в промышленных процессах. Они могут ускорять химические реакции, участвовать в окислительно-восстановительных реакциях и снижать энергию активации реакций.
- Магнитные свойства: Некоторые переходные металлы обладают высокой магнитной восприимчивостью и стабильным магнитным поведением. Это делает их полезными в производстве магнитов и магнитных материалов.
- Растворимость: Многие переходные металлы образуют растворимые и стабильные комплексы с различными лигандами. Их растворимость в воде и других растворителях может зависеть от их валентности и др. химических частей.
Переходные металлы являются важными компонентами многих жизненно важных систем и процессов. Они широко применяются в качестве катализаторов, лекарств, цветных пигментов, магнитов, солнечных батарей и в других областях. Их уникальные характеристики позволяют им играть важную роль в химии и технологических процессах.
Особенности комплексных соединений переходных металлов

Переходные металлы обладают уникальными свойствами, которые делают их особенно интересными для образования комплексных соединений. Одной из основных характеристик этих соединений является наличие одной или нескольких координатных связей между переходными металлами и лигандами. Это позволяет комплексам образовывать разнообразные структуры и обладать различными физическими и химическими свойствами.
Комплексные соединения переходных металлов также отличаются от обычных соединений тем, что они часто обладают высокой степенью структурной организации. Внутри комплекса атомы переходного металла и лиганды располагаются в определенном порядке, образуя координационную сферу вокруг металла. Это обстоятельство позволяет комплексу проявлять свойства, которые не характерны для отдельных компонентов.
Одной из особенностей комплексов переходных металлов является их способность к изменению структуры и свойств в зависимости от окружающей среды. Влияние лигандов и условий реакции может привести к образованию соединений с различными степенями окисления, растворимостью, магнитными свойствами и т.д. Благодаря этому свойству комплексы переходных металлов широко применяются в различных областях, включая катализ и медицину.
Комплексные соединения переходных металлов могут иметь различные степени валентности, что позволяет им обмениваться электронами с окружающими молекулами. Это обстоятельство делает комплексы переходных металлов активными веществами в химических реакциях, таких как окислительно-восстановительные процессы, присоединение лигандов и т.д. Кроме того, переходные металлы могут образовывать комплексы с различными лигандами, что позволяет им вступать во взаимодействие со множеством различных соединений.
Строение комплексных соединений

Комплексные соединения — это химические соединения, в которых центральный атом, ион или молекула, называемые лигандами, образуют координационную сферу вокруг переходного металла. Строение комплексных соединений определяется взаимодействием лигандов и центрального атома, что приводит к образованию координационных связей.
Координационная сфера включает в себя центральный атом или ион, а также лиганды, которые связаны с центральным атомом через координационные связи. Лиганды могут быть анионы или нейтральные молекулы, содержащие одну или несколько атомных групп, обладающих неспаренными электронами.
Строение комплексных соединений может быть описано с помощью различных моделей и терминов. Например, модель октаэдра описывает комплексы, в которых центральный атом или ион образует координационную сферу из шести лигандов, расположенных вокруг него таким образом, чтобы образовывать октаэдр. Модель квадратной пирамиды описывает комплексы, в которых пять лигандов располагаются в плоскости, а шестой лиганд находится над этой плоскостью или под ней.
Строение комплексных соединений может иметь большое значение для их свойств и реакционной активности. Оно может влиять на взаимодействие со средой, способность к каталитической активности, оптические свойства и т.д. Изучение строения комплексных соединений является важным аспектом в области координационной химии и может помочь в понимании многих химических реакций и процессов, связанных с переходными металлами.
Свойства и реактивность комплексных соединений

Комплексные соединения переходных металлов обладают уникальными свойствами и высокой реактивностью. Они образуются путем образования координационных связей между переходными металлами и лигандами, которые могут быть анионами, нейтральными молекулами или катионами.
Важное свойство комплексных соединений - их способность изменять свою структуру и оптические свойства в зависимости от окружающей среды. Различные лиганды могут влиять на цвет и магнитные свойства соединения. Например, соединения переходных металлов с азотсодержащими лигандами обладают яркой окраской, тогда как соединения с карбонилами обычно являются безцветными.
Комплексные соединения также обладают высокой реактивностью и могут участвовать в различных химических реакциях. Они могут взаимодействовать с другими соединениями, образуя новые комплексы или происходя реорганизация координационной сферы металла. Кроме того, комплексы переходных металлов могут быть использованы в качестве катализаторов для различных химических превращений.
Свойства комплексных соединений могут быть использованы в различных областях, включая катализ, медицину, оптику и электронику. Они являются важными объектами исследования в сфере координационной химии и позволяют разрабатывать новые материалы и технологии.
Применение комплексных соединений

Комплексные соединения, получаемые из переходных металлов, находят широкое применение в различных областях науки и техники. Одной из важнейших областей применения является катализ.
Благодаря особой структуре и свойствам комплексных соединений, они могут быть эффективными катализаторами в химических реакциях. Катализаторы на основе комплексных соединений используются в производстве пластиков, фармацевтических продуктов, а также в процессах очистки воды и воздуха.
Другим важным направлением использования комплексных соединений является медицина. Некоторые комплексные соединения переходных металлов обладают антибактериальными свойствами и могут быть использованы в лекарственных препаратах для борьбы с инфекционными заболеваниями. Кроме того, комплексные соединения переходных металлов могут быть полезными в лечении рака и других заболеваний.
Комплексные соединения также используются в сенсорах и электронике. Например, некоторые комплексы переходных металлов способны менять цвет в зависимости от внешних условий, таких как температура или pH. Эти свойства можно использовать для создания сенсоров, которые могут измерять эти параметры и давать соответствующий сигнал. Кроме того, комплексные соединения переходных металлов могут быть использованы в электронике для создания новых материалов и устройств с улучшенными свойствами.
Вопрос-ответ

Какие элементы относятся к переходным металлам?
К переходным металлам относятся элементы д-блока периодной системы, начиная с титана (Z=22) и заканчивая ртутью (Z=80). Всего в переходных металлах 38 элементов.
Что такое комплексные соединения?
Комплексные соединения - это соединения, в которых координированный центр (переходный металл) образует благородный газ или внутримолекулярную связь с другими молекулами или ионами, называемыми лигандами. Комплексы могут иметь различные структуры и свойства.
Какие свойства переходных металлов делают их полезными в различных областях?
Переходные металлы обладают несколькими полезными свойствами, такими как высокая термическая и электрическая проводимость, магнитные свойства, катализаторные свойства и способность образовывать комплексные соединения. Благодаря этим свойствам, переходные металлы широко используются в различных областях, включая промышленность, электронику, катализ и медицину.
