Оксиды металлов – это соединения, состоящие из кислорода и металла. Они образуются в результате химической реакции между металлом и кислородом. Оксиды металлов имеют широкий спектр свойств и применений, что делает их важными и интересными объектами изучения в области химии и материаловедения.
Одной из основных характеристик оксидов металлов является их физическое состояние. Они могут быть как твердыми, так и газообразными веществами, в зависимости от конкретного металла и условий образования. Например, оксид алюминия, белый порошок, обладает высокой термической стабильностью и используется в производстве керамики, а оксид магния, известный как перекись магния, является газообразным веществом и широко применяется как катализатор в химической промышленности.
Еще одним важным свойством оксидов металлов является их химическая активность. Они могут реагировать с водой, кислотами и другими веществами, образуя новые соединения. Например, медный оксид может реагировать с серной кислотой, образуя сульфат меди, который широко используется в производстве гальванических элементов и красителей.
Применение оксидов металлов разнообразно и зависит от их конкретных свойств. Они используются в качестве катализаторов, пигментов, пропускных материалов, диэлектриков и многого другого. Например, оксид цинка применяется в качестве пигмента в красках, а оксид титана – в производстве солнечных батарей и косметических средств. Это лишь некоторые примеры использования оксидов металлов, которые подчеркивают их важность и актуальность в современной промышленности и науке.
Оксиды металлов: свойства и применение
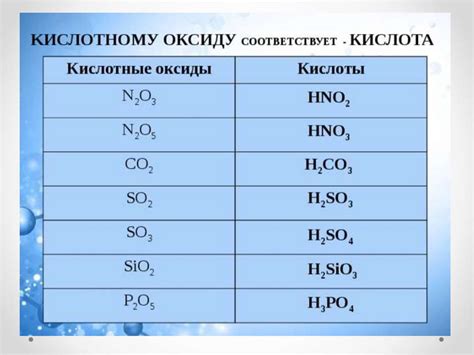
Оксиды металлов - это химические соединения, состоящие из металлического и кислородного атомов. Они обладают различными свойствами и имеют широкое применение в различных областях.
В зависимости от своих свойств, оксиды металлов могут быть кислотными или щелочными. Кислотные оксиды растворяются в воде и образуют кислые растворы, а щелочные оксиды образуют щелочные растворы.
Оксиды металлов широко используются в производстве различных материалов. К примеру, оксид кремния (SiO2), известный также как кварц, используется в производстве стекла и керамики. Оксид железа (Fe2O3), также известный как красный оксид железа или ржавчина, применяется в производстве красок, пигментов и косметических средств.
Некоторые оксиды металлов являются полупроводниками и используются в электронике и солнечных батареях. Например, оксид кадмия (CdO) применяется для создания тонких пленок в солнечных батареях, а оксид цинка (ZnO) используется в светодиодах и прозрачном электроде жидкокристаллических дисплеев.
Оксиды металлов также используются в катализе химических реакций. Например, оксид меди (CuO) используется в процессе газовой очистки и в производстве газа для сварки. Оксид кобальта (CoO) широко применяется в производстве катализаторов для реакций гидрогенирования и оксидирования.
Основные свойства оксидов металлов
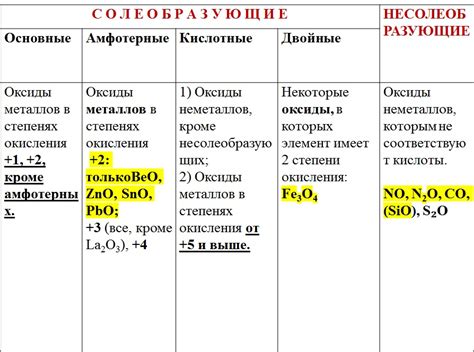
Оксиды металлов - это одна из самых распространенных и важных групп неорганических соединений. Они образуются при соединении металлов с кислородом. Одно из основных свойств оксидов металлов - их высокая степень устойчивости к действию различных химических реагентов.
Оксиды металлов характеризуются различными степенями окисления металла. Некоторые оксиды металлов обладают свойствами кислотных оксидов, способны растворяться в воде и образовывать кислотные растворы. Другие оксиды металлов являются основными оксидами, способными растворяться в воде и образовывать щелочные растворы. Есть также нейтральные оксиды, не проявляющие ни кислотных, ни основных свойств.
Оксиды металлов обладают высокой термической устойчивостью. Они обычно имеют высокую температуру плавления и кипения. Многие оксиды металлов используются в качестве катализаторов в различных химических процессах. Они также широко применяются в производстве керамики, эмали, стекла и других материалов.
Основные свойства оксидов металлов можно обобщить следующим образом:
- Высокая устойчивость к воздействию химических реагентов.
- Различные степени окисления металла.
- Кислотные, основные и нейтральные свойства.
- Высокая термическая устойчивость.
- Применение в качестве катализаторов и в производстве различных материалов.
Физические свойства оксидов металлов

Оксиды металлов обладают рядом физических свойств, которые определяют их поведение и применение в различных областях науки и промышленности.
Температурная зависимость: Оксиды металлов обычно имеют высокие точки плавления и кипения. Они являются твердыми веществами при комнатной температуре, но некоторые из них, как, например, оксид меди (II), оксид железа (III), плавятся при нагревании.
Цвет: Оксиды металлов могут иметь различные цвета, включая белый, черный, красный, желтый, синий и зеленый. Этот цвет может варьироваться в зависимости от конкретного металла и степени окисления.
Плотность: Оксиды металлов обычно имеют высокую плотность, что делает их тяжелыми веществами. Некоторые оксиды, такие как оксид железа (II) и оксид алюминия, имеют очень высокую плотность и являются одними из самых плотных веществ на Земле.
Состояние агрегации: Оксиды металлов могут существовать в различных состояниях агрегации, включая кристаллические и аморфные структуры. Кристаллические оксиды металлов обычно образуют регулярные и упорядоченные структуры, в то время как аморфные оксиды металлов имеют нерегулярную и безупречную структуру.
Растворимость: Оксиды металлов могут быть растворимыми в воде или нерастворимыми. Некоторые оксиды, такие как оксид натрия и оксид калия, легко растворяются в воде, образуя растворы щелочей. Другие оксиды, такие как оксид железа (III) и оксид алюминия, не растворяются в воде и являются нерастворимыми веществами.
Химические свойства оксидов металлов
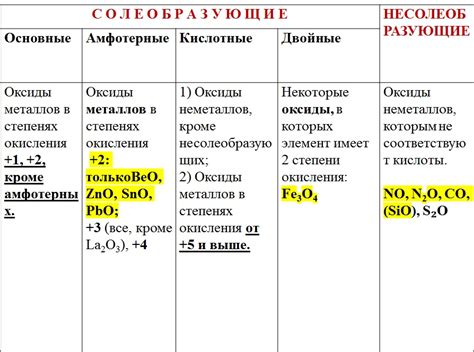
Оксиды металлов являются одной из самых распространенных групп неорганических соединений. Они образуются в результате реакции металла с кислородом, и их химические свойства в значительной степени зависят от их состава и структуры.
В зависимости от степени окисления металла, оксиды металлов могут обладать различными свойствами. Некоторые оксиды считаются кислотными, так как они реагируют с водой, образуя кислоты. Другие оксиды являются основными и реагируют с кислотами, образуя соли и воду.
Оксиды металлов также могут проявлять амфотерные свойства, то есть они могут реагировать как с кислотами, так и с щелочами. Это свойство позволяет оксидам металлов быть важными компонентами в процессах нейтрализации кислот и оснований.
Многие оксиды металлов обладают высокой степенью термической стабильности и устойчивы к высоким температурам. Именно поэтому они широко используются в качестве катализаторов и пигментов в различных процессах производства.
Оксиды металлов также обладают значительной электрохимической активностью. Они могут служить резервуарами кислорода в электрохимических системах, а также участвовать в реакциях окисления и восстановления.
Некоторые оксиды металлов обладают полупроводниковыми свойствами и используются в электронике и солнечных батареях. Они могут образовывать способные проводить электрический ток слои, что позволяет им выполнять роль полупроводников и совершать электронные переходы.
Все эти химические свойства оксидов металлов делают их неотъемлемой частью различных технологических процессов и промышленных производств. Они находят свое применение в катализе, электронике, керамике, металлургии и других отраслях промышленности.
Применение оксидов металлов
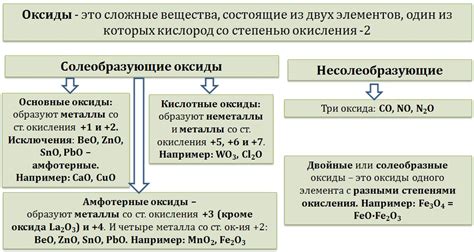
Оксиды металлов находят широкое применение в различных отраслях промышленности и научных исследованиях. Вот некоторые из них:
- Катализаторы: Многие оксиды металлов являются эффективными катализаторами реакций. Например, оксид железа используется в производстве аммиака, а оксид титана - в процессе синтеза этилена.
- Электролитические материалы: Оксиды металлов, такие как оксид алюминия и оксид лития, используются в качестве электролитических материалов в различных электрохимических процессах.
- Красители и пигменты: Некоторые оксиды металлов, например, оксид железа и оксид кобальта, используются в производстве красителей и пигментов для красок, пластиков и косметических продуктов.
- Стекла и керамика: Оксиды металлов добавляются в состав стекла и керамических материалов, чтобы улучшить их физические и химические свойства. Например, оксид свинца используется для придания прозрачности стеклу.
- Электроника и полупроводники: Многие оксиды металлов, такие как оксид кремния и оксид германия, используются в производстве электронных компонентов и полупроводниковых устройств.
В общем, оксиды металлов имеют широкий спектр применений, и их свойства и состав можно настроить путем добавления различных элементов и изменения режимов обработки материалов.
Техническое применение оксидов металлов
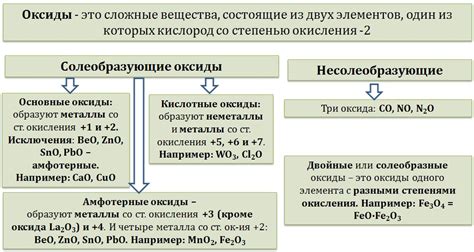
Оксиды металлов широко применяются в различных отраслях промышленности благодаря своим уникальным свойствам и возможностям.
В электронной промышленности оксиды металлов используются в качестве материалов для создания проводников, полупроводников и транзисторов. Например, оксид индия, оксид цинка и оксид олова применяются в производстве транзисторов и солнечных батарей.
Оксиды металлов также используются в керамической промышленности для изготовления керамических изделий с высокой прочностью и теплоустойчивостью. Оксид алюминия, оксид циркония и оксид титана применяются в процессе создания керамических изделий, которые используются в авиационной и космической промышленности, медицине и других отраслях.
Оксиды металлов также широко используются в производстве стекла. Например, оксид свинца используется для придания стеклу оптической прозрачности и яркости, а оксид натрия и оксид калия используются для изменения его химических и физических свойств.
Оксиды металлов применяются и в производстве красок и покрытий. Оксиды железа, меди, цинка и других металлов используются для придания поверхностям металлических изделий стойкости к коррозии и улучшения их внешнего вида.
Также стоит отметить, что некоторые оксиды металлов имеют фотохимические свойства и могут использоваться в фотокатализе, т.е. в процессе разложения загрязнений в воде и воздухе под воздействием света.
В целом, техническое применение оксидов металлов очень разнообразно и находится во многих сферах промышленности, от электроники и керамики, до стекла и красок.
Биологическое применение оксидов металлов
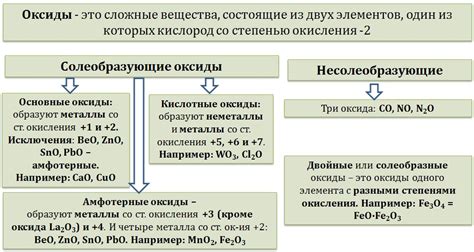
Оксиды металлов находят широкое биологическое применение благодаря своим уникальным свойствам. Они часто используются в медицине для лечения различных заболеваний.
Например, оксид железа (Fe2O3) используется в качестве препарата для лечения анемии. Он улучшает кроветворение и помогает организму восстанавливать запасы железа.
Оксид кремния (SiO2) имеет противовоспалительные свойства и широко применяется в косметологии и медицине для лечения раздражений кожи, ожогов и ран. Этот оксид также используется для производства искусственных костей и зубов.
Оксид цинка (ZnO) обладает антибактериальными и противовоспалительными свойствами. Он используется в качестве ингредиента для косметических средств и солнцезащитных кремов, а также в лечении различных кожных заболеваний.
Другим примером может служить оксид титана (TiO2), который широко применяется в производстве солнцезащитных средств благодаря своей способности отражать ультрафиолетовое излучение. Он также используется в керамике и косметике.
Оксиды металлов играют важную роль в биологии и медицине благодаря своим полезным свойствам. Они предлагают широкий спектр применения, и постоянно исследуются для создания новых препаратов и лекарственных средств.
Вопрос-ответ

Какие свойства имеют оксиды металлов?
Оксиды металлов обладают рядом характерных свойств. Они обычно имеют высокие температуры плавления и кипения, и обычно являются твердыми кристаллическими веществами. Они также обладают высокой теплопроводностью и электропроводностью. Оксиды металлов также могут иметь кислотный или щелочной характер в зависимости от степени окисления металла.
Каково применение оксидов металлов?
Оксиды металлов имеют широкое применение в различных областях. Например, оксид железа (Fe3O4), более известный как магнетит, используется в производстве магнитов и магнитных материалов. Оксид цинка (ZnO) используется в солнечных батареях, косметике, керамике и других областях. Оксид алюминия (Al2O3), также известный как алюминиевое стекло, используется в производстве керамики, стекла и других материалов. Общим применением оксидов металлов является их использование в качестве катализаторов в химической промышленности.
