Соли щелочных металлов являются важными соединениями, которые имеют широкое применение в различных областях науки и промышленности. Они образуются в результате реакции щелочных металлов с кислотами, и их формула следует определенным принципам.
Общая формула соли щелочных металлов имеет вид М+А-, где М обозначает ион щелочного металла, а А- обозначает отрицательно заряженный анион. Эта формула позволяет определить состав соли и ее заряд. Часто используемые ионы щелочных металлов в солях включают натрий (Na+), калий (K+), литий (Li+) и цезий (Cs+).
Приведем несколько примеров общих формул солей щелочных металлов:
- Сульфат натрия: Na2SO4
- Хлорид калия: KCl
- Нитрат лития: LiNO3
- Фосфат цезия: Cs3PO4
Каждый пример демонстрирует соединение ионов щелочных металлов с различными анионами. Соли щелочных металлов обладают различными свойствами, и их использование широко распространено в медицине, пищевой промышленности, сельском хозяйстве и других отраслях. Понимание общей формулы солей щелочных металлов является важным шагом в изучении их свойств и применения.
Основные принципы общей формулы соли щелочных металлов

Щелочные металлы в периодической системе элементов включают в себя лихий, натрий, калий, рубидий, цезий и франций. Соли щелочных металлов имеют общую формулу MX, где M обозначает щелочный металл, а X - анион. Основными принципами общей формулы являются следующие:
- Щелочные металлы всегда являются катионами. Из-за своей низкой ионизационной энергии, щелочные металлы легко отдают электрон и образуют положительно заряженные катионы.
- Анионы в солях щелочных металлов могут быть различными. Анионами могут быть галогены (фтор, хлор, бром, йод), оксиды, сульфаты, нитраты и другие соединения, которые имеют отрицательный заряд.
- Соединения щелочных металлов обычно обладают высокой растворимостью в воде. Большинство солей щелочных металлов хорошо растворимы в воде, что обусловлено высокой положительной зарядностью катиона и его маленьким размером.
- Соли щелочных металлов образуют кристаллическую структуру. Когда соли щелочных металлов растворяются и затем осушаются, группы ионов образуют кристаллическую структуру с определенными регулярными пространственными показателями.
Через общую формулу солей щелочных металлов можно определить их химический состав и структуру. Это позволяет исследователям более глубоко изучать свойства и реактивность таких соединений, а также применять их в различных областях, включая фармакологию, пищевую промышленность и материаловедение.
Примеры солей щелочных металлов и их формулы
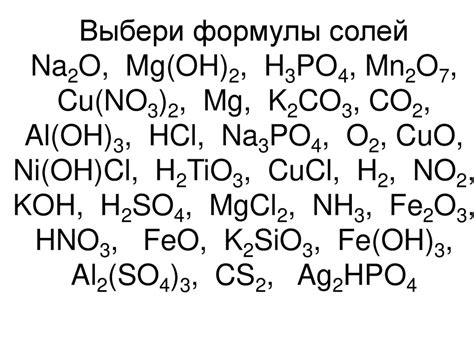
Соли щелочных металлов широко представлены в природе и имеют множество применений в различных отраслях промышленности. Некоторые из примеров солей щелочных металлов и их формулы приведены ниже:
- Нитрат натрия (NaNO3): это белая кристаллическая соль, которая используется в производстве стекла и удобрений. Она обладает свойством плавиться при небольшой температуре и может быть использована в процессе солеплавильного стекла.
- Хлорид калия (KCl): это белая кристаллическая соль, наиболее известная как пищевая и медицинская добавка, а также используется в процессе производства удобрений. Он также используется в процессе очистки воды и в лекарственных препаратах.
- Сульфат лития (Li2SO4): это бесцветные кристаллы, которые используются в производстве керамики, стекла и лекарственных препаратов. Он также применяется в процессе электролиза и в производстве литиевых батарей.
- Карбонат рубидия (Rb2CO3): это белые кристаллические соли, используемые в производстве оптических стекол, в качестве катализаторов и в электронике. Они также могут использоваться в процессе производства огнетушителей и лекарственных препаратов.
Это лишь некоторые примеры солей щелочных металлов. Каждая из этих солей имеет свою уникальную формулу и применение в различных областях. Знание и понимание этих соединений является важным для химической промышленности и научных исследований.
Вопрос-ответ

Что такое общая формула соли щелочных металлов?
Общая формула соли щелочных металлов - это химическая формула, которая позволяет представить структуру и состав солей, содержащих щелочные металлы. Она выражается символами и числами, указывающими какие элементы и в каком количестве присутствуют в соединении.
Какие основные принципы заложены в общую формулу соли щелочных металлов?
Основные принципы, заложенные в общую формулу соли щелочных металлов, связаны с электростатическими взаимодействиями между ионами в соли. Общая формула позволяет определить пропорции ионов щелочного металла и аниона в соли, а также указывает наличие водной оболочки вокруг ионов.
Какие примеры можно привести для общей формулы соли щелочных металлов?
Примеры общей формулы для солей щелочных металлов могут включать соединения калия (К), натрия (Na), лития (Li) и других щелочных металлов. Например, для хлорида калия общая формула будет KCl, для сульфата натрия - Na2SO4, а для нитрата лития - LiNO3.
Какую роль играет общая формула соли щелочных металлов в химии?
Общая формула соли щелочных металлов играет важную роль в химии, так как она позволяет установить соотношение различных элементов и ионов в соли, определить структуру и состав соли, а также предсказать ее химические свойства и реакционную способность. Общая формула помогает в классификации и идентификации различных соединений, содержащих щелочные металлы.
