Гидриды щелочных металлов представляют собой соединения между щелочными металлами (например, литием, натрием, калием и др.) и водородом. Эти соединения обладают важными свойствами и имеют широкое применение в различных сферах науки и техники.
Общая формула гидридов щелочных металлов можно записать следующим образом: MH, где M - символ щелочного металла. Такая формула указывает на наличие одного атома металла и одного атома водорода в молекуле гидрида.
Стоит отметить, что гидриды щелочных металлов являются ионными соединениями. Это означает, что электроны переносятся от металла к водороду, образуя катион щелочного металла и анион гидрида. Именно благодаря такому строению гидриды обладают химической активностью и способностью к реакциям с другими веществами.
Гидриды щелочных металлов находят применение в различных областях. Они используются в процессах синтеза органических соединений, каталитических реакциях, а также во время производства электрических источников. Кроме того, гидриды щелочных металлов могут использоваться в процессе водородации различных веществ, а также в создании специальных материалов и покрытий.
Исследование гидридов щелочных металлов имеет важное значение для разработки новых каталитических процессов, энергетики, химической промышленности и других областей науки. Благодаря своим уникальным свойствам, гидриды щелочных металлов могут быть полезными в решении актуальных проблем и разработке новых технологий в будущем.
Понятие и свойства гидридов

Гидриды - это химические соединения, образованные щелочными металлами и водородом. Они обладают рядом особенных свойств, которые определяют их уникальные химические и физические характеристики.
Свойства гидридов зависят от типа щелочного металла, с которым образуется соединение, а также от условий синтеза и процесса образования. Однако можно отметить некоторые общие характеристики, которые присущи гидридам щелочных металлов.
Во-первых, гидриды обычно обладают высокой химической активностью. Они реагируют с водой, сильными окислителями и другими химическими веществами, образуя соответствующие продукты реакции.
Во-вторых, гидриды обычно обладают низкой плотностью, что обусловлено наличием маломассивного водорода в структуре соединений.
В-третьих, гидриды часто обладают низкой температурой плавления и жидкостью при комнатной температуре. Это делает их удобными для использования в различных промышленных процессах и приложениях.
Также, гидриды щелочных металлов могут быть амфотерными, то есть способны реагировать как с кислотами, так и с основаниями.
В-пятых, гидриды могут образовывать кристаллическую решетку с определенными параметрами, что влияет на их физические свойства, такие как твердость, прозрачность и электропроводность.
Весь этот ряд свойств делает гидриды щелочных металлов значимыми соединениями, используемыми в различных отраслях промышленности и науки. Они находят широкое применение в энергетике, катализе, производстве батарей и др.
Структура и типы гидридов щелочных металлов
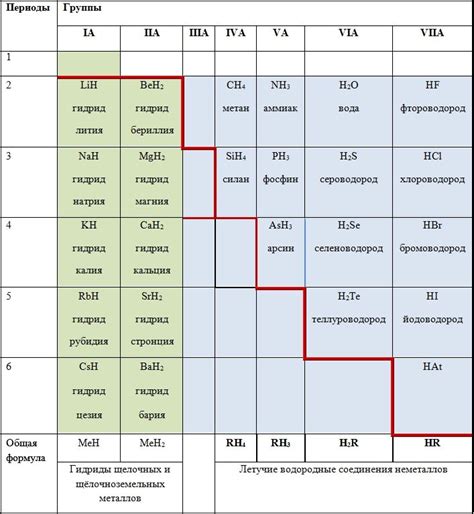
Гидриды щелочных металлов представляют собой соединения металлов с водородом. Они имеют простую структуру и обычно относятся к ионному типу соединений. Гидриды щелочных металлов обладают различными физическими свойствами и могут быть представлены в нескольких различных типах.
Одним из наиболее распространенных типов гидридов щелочных металлов являются ионные гидриды, в которых водород образует отрицательный ион, а металл – положительный ион. Эти гидриды обладают высоким плавлением и кипением, что связано с сильными электростатическими взаимодействиями между ионами в решетке. Примером ионного гидрида является гидрид натрия (NaH).
Кроме того, существуют и металлические гидриды, где водород встраивается в кристаллическую решетку металла. Эти гидриды обладают высокой проводимостью электричества и тепла. Примером металлического гидрида является гидрид лития (LiH).
Также существуют соединения, называемые комплексными гидридами, где водород образует комплекс с другими атомами или молекулами. Эти гидриды обладают сложной структурой и свойствами, и их можно использовать в качестве катализаторов или энергетических материалов. Примером такого гидрида является гидрид калия-бора (KBH4).
В целом, гидриды щелочных металлов имеют важное значение в различных областях химии и материаловедения. Изучение и использование этих соединений позволяет расширить наши знания о свойствах водорода и его взаимодействии с другими веществами. Кроме того, гидриды щелочных металлов могут иметь практическое применение в производстве энергии, хранении водорода и других технологиях будущего.
Физико-химические свойства гидридов щелочных металлов

Гидриды щелочных металлов являются соединениями, в которых щелочные металлы образуют химические связи с водородом. Они обладают рядом интересных физико-химических свойств, которые делают их полезными в различных областях науки и промышленности.
Во-первых, гидриды щелочных металлов обладают высокой растворимостью в воде. Это свойство обусловлено способностью щелочных металлов образовывать ионы гидроксида, которые легко диссоциируются в воде. Благодаря этой высокой растворимости, гидриды щелочных металлов используются в качестве щелочных и алкалиметаллических растворов.
Во-вторых, гидриды щелочных металлов обладают высокой электропроводностью. Они могут быть использованы в качестве электролитов в различных электрохимических процессах, таких как электролиз, гальваническое осаждение и другие. Благодаря этим свойствам, гидриды щелочных металлов находят применение в батареях, аккумуляторах и других энергетических устройствах.
В-третьих, гидриды щелочных металлов обладают способностью к эндо- и экзотермическим реакциям. Это означает, что при взаимодействии с другими веществами они могут как поглощать, так и выделять тепло. Это свойство позволяет использовать гидриды щелочных металлов в реакциях синтеза, водородации и обогащения различных соединений и материалов.
Таким образом, физико-химические свойства гидридов щелочных металлов делают их важными соединениями в химии, электрохимии, материаловедении и других областях науки и технологий. Изучение и применение этих свойств позволяет разрабатывать новые методы синтеза веществ, создавать новые материалы с уникальными свойствами и улучшать существующие технологии и процессы.
Применение гидридов щелочных металлов

Гидриды щелочных металлов, такие как гидрид натрия, калия, лития и других щелочных металлов, широко применяются в различных областях.
Одним из наиболее распространенных применений гидридов щелочных металлов является их использование в химической промышленности. Гидриды щелочных металлов используются в качестве восстановителей при процессах синтеза органических соединений, производстве сплавов и покрытий. Они используются также в процессе очистки и фильтрации воды.
Гидриды щелочных металлов также находят применение в электрохимии. Они используются в качестве водородных носителей или водородных сенсоров. Гидриды способны быстро и обратимо взаимодействовать с водородом, что делает их полезными в процессе получения энергии или контроля концентрации водорода в различных реакциях и процессах.
Гидриды щелочных металлов также используются в батареях и аккумуляторах. Натриевые и литиевые гидриды являются одними из основных компонентов в современных литий-ионных батареях, которые широко применяются в электронике, автомобильной промышленности и других областях.
Благодаря своим химическим и физическим свойствам, гидриды щелочных металлов также находят применение в лабораторных исследованиях. Они могут быть использованы для восстановления или водородации органических соединений, в качестве катализаторов или для синтеза новых веществ. Гидриды щелочных металлов также находят применение в процессе анализа различных образцов и материалов.
Вопрос-ответ

Какая общая формула гидридов щелочных металлов?
Общая формула гидридов щелочных металлов имеет вид MH, где M - щелочный металл.
Для каких металлов применима общая формула гидридов?
Общая формула гидридов применима для щелочных металлов, таких как литий (Li), натрий (Na), калий (K), рубидий (Rb) и цезий (Cs).
Какую роль играют гидриды щелочных металлов в химии?
Гидриды щелочных металлов играют важную роль в химии, поскольку они могут служить источником водорода и использоваться в реакциях с другими веществами.
Какие свойства обладают гидриды щелочных металлов?
Гидриды щелочных металлов обладают высокой реакционной активностью, способностью растворяться в воде и образовывать щелочные растворы, а также способностью образовывать взрывоопасные смеси с воздухом.
Какие применения имеют гидриды щелочных металлов?
Гидриды щелочных металлов используются в различных областях, таких как производство водорода, катализаторы в химической промышленности и в процессах хранения и транспортировки водорода.
