Ковалентная полярная связь – это один из видов химических связей, который возникает при взаимодействии атомов металлов. В этом процессе атомы металлов обменивают электроны, что приводит к образованию пары электронов, связывающей атомы в единое целое.
Процесс образования ковалентной полярной связи начинается с того, что атомы металлов приближаются друг к другу под воздействием различных факторов, например, химической реакции или внешнего воздействия. При этом оболочка электронов атомов перекрывается, и происходит обмен электронами.
Важно понимать, что при образовании ковалентной полярной связи электроны не передаются полностью от одного атома к другому, а взаимодействуют между собой. Таким образом, каждый атом металла получает от соседнего атома дополнительные электроны, при этом сохраняется электрическая нейтральность системы в целом.
Важным аспектом образования ковалентной полярной связи является разность в значении электроотрицательности атомов металлов. Электроотрицательность – это химическая величина, характеризующая способность атома притягивать к себе электроны. В случае, когда атомы металлов имеют разное значениеРазность электроотрицательности приводит к тому, что электроны, взаимодействуя друг с другом, будут проводить больше времени у более электроотрицательного атома. Это приводит к образованию полярной связи со смещением зарядов.
В результате образования ковалентной полярной связи при взаимодействии атомов металлов образуется соединение, в котором происходит совместное использование электронов обоими атомами. Это является основой стабильности и прочности молекулы или кристаллической решетки вещества.
Взаимодействие атомов металлов и образование ковалентной полярной связи
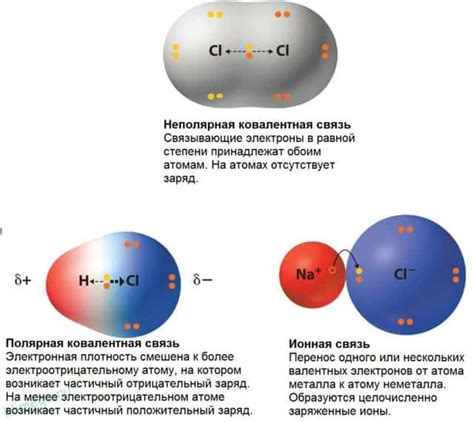
Взаимодействие между атомами металлов приводит к образованию ковалентной полярной связи. Эта связь возникает при обмене электронами между атомами и является основной причиной устойчивости металлической решетки.
Атомы металлов имеют низкую электроотрицательность, что означает, что они имеют тенденцию отдавать электроны другим атомам. Когда два атома металла приближаются друг к другу, их внешние электроны начинают взаимодействовать. Один из атомов отдаст свои электроны, а другой атом примет их.
Этот обмен электронами приводит к образованию полярной связи, в которой один атом становится положительно заряженным (катионом), а другой атом - отрицательным (анионом). Таким образом, образуется ковалентная полярная связь, которая обеспечивает силу притяжения между атомами металлов и делает металлическую решетку устойчивой и прочной.
Свойства ковалентной полярной связи зависят от различных факторов, включая электроотрицательность атомов, их радиусы и особенности кристаллической решетки металла. В результате образования ковалентной полярной связи металлы приобретают характерные свойства, такие как высокая теплопроводность, электропроводность и пластичность.
Принципы образования ковалентной полярной связи
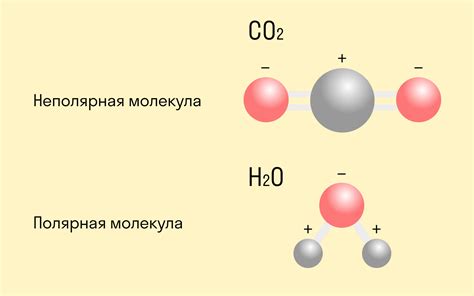
Ковалентная полярная связь образуется между атомами металлов, когда они обменивают электроны. В основе образования такой связи лежит несоответствие в электроотрицательности атомов.
Электроотрицательность - это способность атома притягивать электроны в химической связи. Атомы, имеющие большую электроотрицательность, проявляют большую силу притяжения электронов.
В ковалентной полярной связи один атом, обладающий более высокой электроотрицательностью, привлекает электроны к себе сильнее, чем другой атом. Таким образом, электроны проводимости смещаются ближе к атому с большей электроотрицательностью.
Возникающее разделение зарядов создает полярность в связи. Атом с большей электроотрицательностью приобретает отрицательный заряд, а атом с меньшей электроотрицательностью - положительный заряд.
Ковалентная полярная связь позволяет атомам металлов совместно использовать электроны и образовывать стабильные молекулы. Это явление широко используется в различных химических реакциях и обеспечивает устойчивость многих веществ, среди которых металлы играют важную роль.
Влияние электроотрицательности элементов на образование полярной связи
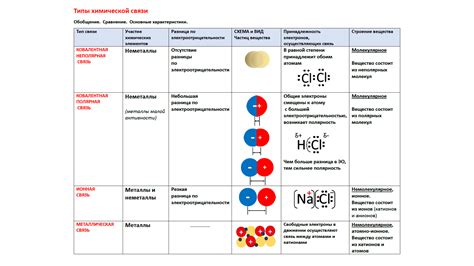
Электроотрицательность элементов – это их способность притягивать электроны в химических связях. Влияние электроотрицательности на образование полярной связи в особенности проявляется при взаимодействии атомов металлов.
Металлы обладают относительно низкой электроотрицательностью, что означает, что они имеют слабую способность притягивать электроны к себе. При взаимодействии металлов с другими элементами, обладающими более высокой электроотрицательностью, происходит образование полярной связи.
Полярная связь возникает в результате неравномерного распределения электронной плотности между атомами. В металлах, например, меди, электроны могут быть слабо удержаны ядром и свободно передвигаться по всей структуре металла. При взаимодействии с большей электроотрицательностью другого элемента, электроны будут притягиваться к этому элементу сильнее, чем к металлу.
Это приводит к образованию полярной связи, где один атом будет обладать положительным зарядом (катионом), а другой – отрицательным зарядом (анионом). Полярная связь обусловливает устойчивость соединений и позволяет атомам металлов осуществлять перекачку электронов. Такие соединения обычно обладают высокой температурой плавления и проводимостью электричества.
Электроотрицательность элементов влияет на образование полярной связи и определяет химическую природу соединения металла с другими элементами. Чем больше разница в электроотрицательности, тем сильнее полярность связи и больше будет разница в зарядах между атомами. Это помогает определить силу связи и химические свойства соединения.
Структура и свойства ковалентной полярной связи между атомами металлов
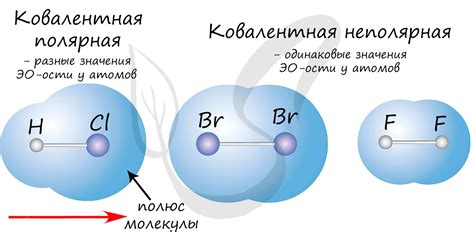
Ковалентная полярная связь между атомами металлов образуется в результате валентной связи, при которой происходит обмен электронами между атомами. В отличие от ионной связи, где происходит передача электронов от одного атома к другому, в ковалентной полярной связи электроны равномерно распределены между атомами.
Структура ковалентной полярной связи состоит из двух компонентов: положительного и отрицательного. Атом, который отдает электроны и становится положительным, называется донором, а атом, который принимает электроны и становится отрицательным, называется акцептором. Этот обмен электронами создает дипольную момент у связей, в результате чего образуется полярность и возникают новые свойства.
Одним из свойств ковалентной полярной связи является её направленность. Между атомами металлов происходит симметричное распределение электронной плотности, что приводит к образованию деформации между атомами и созданию кристаллической решетки. Кроме того, ковалентная полярная связь обладает высокой прочностью и устойчивостью, что обусловлено сильными валентными силами, действующими между атомами.
Также стоит отметить, что ковалентная полярная связь между атомами металлов обладает способностью к изменению длины связи и угла между атомами в зависимости от различных условий. Это свойство позволяет атомам металлов образовывать разнообразные соединения и стабильные химические соединения.
Вопрос-ответ

Какие основные принципы лежат в основе образования ковалентной полярной связи между атомами металлов?
Образование ковалентной полярной связи между атомами металлов основано на обмене электронами между атомами. В этом процессе один атом металла отдает электрон(ы), а другой атом металла принимает эти электроны. Таким образом, оба атома получают заполненную или почти заполненную электронную оболочку, что делает связь между ними более устойчивой и прочной.
Какие факторы влияют на образование ковалентной полярной связи между атомами металлов?
Образование ковалентной полярной связи между атомами металлов зависит от таких факторов, как электроотрицательность атомов металлов и расстояние между этими атомами. Чем больше разница в электроотрицательности между атомами, тем больше полярность образуемой связи. Кроме того, расстояние между атомами также влияет на силу и устойчивость связи: чем ближе атомы, тем сильнее связь между ними.
Можно ли привести пример образования ковалентной полярной связи между атомами металлов?
Да, одним из примеров образования ковалентной полярной связи между атомами металлов является связь между атомами кислорода и атомами лития. Кислород является более электроотрицательным, поэтому он притягивает электроны от атомов лития, создавая полярную связь между ними.
Какие свойства имеет ковалентная полярная связь между атомами металлов?
Ковалентная полярная связь между атомами металлов обладает такими свойствами, как направленность и полярность. Направленность связи означает, что электроны, участвующие в связи, сосредоточены в области между атомами. Полярность связи означает, что атомы имеют разную электроотрицательность, что приводит к неравномерному распределению зарядов в связи.
Возможно ли образование ковалентной полярной связи между разными атомами металлов?
Да, возможно образование ковалентной полярной связи между разными атомами металлов. В этом случае, различные электроотрицательности атомов создают полярность связи, что делает её более устойчивой и прочной.
