Нитриты металлов являются соединениями, содержащими ион NO2-. Они обладают множеством интересных свойств и областей применения. Нитриты металлов широко используются в различных отраслях промышленности, в научных исследованиях и даже в медицине.
Как известно, нитриты представляют собой соли нитритной кислоты, формула которой NO2H. Нитрит металла кислород формула является результатом замены протона в нитритной кислоте на металлический катион. Разные металлы могут образовывать нитриты с разной степенью окисления и различными свойствами.
Нитриты металлов обладают высокой степенью растворимости в воде, что делает их удобными для использования в различных реакциях. Они часто используются как катализаторы в химических процессах, в производстве удобрений и в электрохимии. Некоторые нитриты металлов также имеют антимикробные свойства и могут использоваться в медицине для лечения некоторых инфекционных заболеваний.
Нитрит металла: свойства и применение

Нитриты металлов – это химические соединения, содержащие в своей структуре ион нитрита (NO2-). Они обладают рядом уникальных свойств, которые находят свое применение в различных областях науки и промышленности.
Самыми известными нитритами металлов являются нитрит натрия (NaNO2) и нитрит калия (KNO2). Они обладают схожими свойствами и широко используются в пищевой промышленности в качестве консервантов и антиоксидантов. Нитриты металлов помогают предотвращать окисление пищевых продуктов, а также способствуют улучшению их качества и вкусовых свойств.
Одним из важных свойств нитритов металлов является их антимикробное действие. Они обладают способностью угнетать рост и размножение микроорганизмов, таких как бактерии и грибки. Благодаря этому свойству нитриты металлов нашли применение в производстве медицинских препаратов, антисептиков и средств по уходу за кожей.
Кроме того, нитриты металлов используются в качестве катализаторов в различных химических реакциях. Они способны увеличить скорость реакции и повысить выход продукта. Благодаря этому свойству нитриты металлов применяются в синтезе органических соединений, производстве пластмасс, полимеров и других химических веществ.
Нитриты металлов также обнаруживают широкое применение в электрохимии. Они используются в качестве электролитов, проводящих электрический ток. Благодаря своим свойствам нитриты металлов способны улучшить процесс электролиза и повысить эффективность электрических аппаратов.
Таким образом, свойства нитритов металлов делают их неотъемлемой частью многих отраслей науки и промышленности. Они находят применение в пищевой промышленности, медицине, химической промышленности и электрохимии, что подтверждает их значимость и широкие перспективы использования в различных областях жизни.
Формула нитрита металла
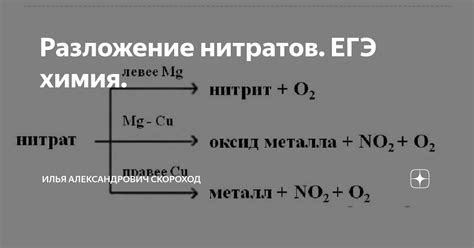
Нитрит металла представляет собой химическое соединение, состоящее из металла и нитритной группы с формулой MNO2, где М обозначает металл. Формула нитрита металла показывает, что одна молекула этого соединения содержит один атом металла и два атома кислорода.
Нитриты металлов обладают различными свойствами в зависимости от типа металла, который входит в состав соединения. Например, нитрит натрия (NaNО2) используется в пищевой промышленности как консервант и антиоксидант, благодаря своей способности замедлять окисление продуктов. Нитрит калия (KNО2) применяется в медицине для лечения ангины, так как он обладает антибактериальными свойствами.
Формула нитрита металла указывает на наличие кислорода в составе соединения, что делает его химически активным средством. Нитриты металлов могут быть использованы в синтезе органических соединений, в производстве красителей и лекарственных препаратов. Они также широко применяются в качестве катализаторов в различных химических реакциях.
Исходя из формулы нитрита металла, можно сделать вывод о его возможной реактивности и способности взаимодействовать с другими веществами. Кроме того, формула нитрита металла указывает на его структуру и химические связи, что позволяет проводить более глубокие исследования данного соединения.
Химические свойства нитрита металла
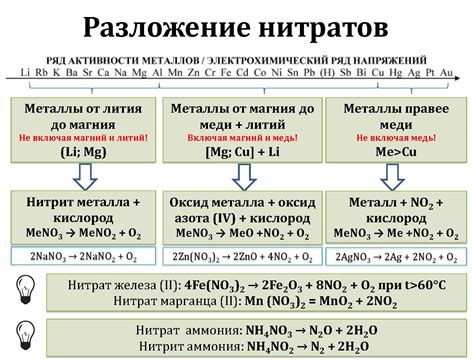
Нитрит металла – химическое соединение, состоящее из металла и нитритной группы (NO2-). Он обладает рядом интересных свойств, которые делают его полезным в различных областях.
Во-первых, нитриты металлов обладают высокой растворимостью в воде. Это делает их удобными для использования в промышленных процессах и лабораторной химии.
Во-вторых, некоторые нитриты металлов обладают консервирующими свойствами. Они могут предотвращать рост бактерий и гниения, что делает их полезными в пищевой промышленности для увеличения срока годности товаров.
Кроме того, некоторые нитриты металлов обладают антисептическими свойствами. Они могут использоваться в медицине для борьбы с инфекциями и бактериями.
Нитрит металла также может быть использован в качестве окислителя в химических реакциях. Он способен передавать кислородные атомы и принимать электроны, что делает его полезным во многих синтетических процессах и производстве.
В общем, нитриты металлов обладают широким спектром свойств, которые делают их полезными в различных областях, включая промышленность, пищевую промышленность, медицину и химическую промышленность.
Физические свойства нитрита металла

1. Кристаллическая структура: Нитрит металла обычно обладает кристаллической структурой, что делает его твердым веществом при комнатной температуре. Кристаллическая структура определяет его устойчивость и химические реакции.
2. Цвет и прозрачность: Нитрит металла может иметь различные цвета, в зависимости от вида металла. Например, нитрит меди имеет светло-синий цвет, нитрит железа – желтый, нитрит свинца – белый. Однако, при некоторых условиях, нитрит металла может быть прозрачным.
3. Точка плавления и кипения: Нитриты металлов обычно имеют достаточно высокие точки плавления и кипения, что обусловлено их кристаллической структурой и сильной связью между атомами. Это свойство может быть использовано для различных технических процессов и применений.
4. Плотность: Нитрит металла имеет характеристику плотности, которая может быть разной в зависимости от вида металла. Например, нитрит меди имеет плотность около 4,3 г/см³, а нитрит железа – около 3,4 г/см³. Это свойство может быть использовано для определения концентрации нитрита металла в растворе.
5. Растворимость: Нитриты металлов обычно растворяются в воде, образуя нитритные ионные комплексы. Растворимость может быть разной в зависимости от вида металла и условий окружающей среды. Это свойство может быть использовано в химических реакциях и различных применениях нитритов металлов.
Области применения нитрита металла

Нитрит металла – это химическое соединение, состоящее из атомов металла и нитритной группы (NO2). Это вещество обладает рядом уникальных свойств, которые позволяют его использовать в различных областях. Рассмотрим некоторые из них.
1. Каталитическая химия: нитриты металла могут использоваться в качестве катализаторов в различных реакциях, таких как окисление алканов и аммиака, гидрогенизация алкенов, фотокаталитические реакции.
2. Производство взрывчатых веществ: нитриты металла часто используются в качестве компонентов при изготовлении тротиловых взрывчатых веществ. Они обладают высокой взрывоопасностью и находят широкое применение в военной и промышленной сферах.
3. Металлургия: нитриты металла могут использоваться в процессе плавки металла для очистки от примесей и в качестве окислителей при производстве сплавов.
4. Электрохимия: нитриты металла могут использоваться в электрохимических процессах, таких как электроосаждение металла на поверхности электрода.
5. Медицина и фармакология: нитриты металла могут быть использованы в медицине и фармакологии в качестве антисептиков и антиоксидантов.
6. Производство красителей: нитриты металла могут быть использованы в производстве красителей и пигментов, таких как нитрософены.
7. Пищевая промышленность: нитриты металла широко используются в пищевой промышленности в качестве консервантов для предотвращения развития бактерий и улучшения качества продуктов.
Исходя из указанных областей применения, видно, что нитрит металла является важным и многоопасным соединением, которое находит применение в различных отраслях науки, техники и промышленности.
Технические свойства нитрита металла

Нитрит металла – соединение, обладающее рядом свойств, которые делают его привлекательным для различных технических применений.
Прежде всего, нитрит металла обладает высокой стойкостью к коррозии. Это означает, что он не подвержен разрушению под воздействием окружающей среды, что делает его идеальным материалом для эксплуатации в агрессивных условиях или в суровых климатических условиях.
Кроме того, нитрит металла обладает высокой теплопроводностью. Это позволяет эффективно передавать и отводить тепло, что делает его идеальным материалом для использования в процессах, связанных с высокими температурами или потоками тепла.
Также нитрит металла обладает устойчивостью к высоким давлениям. Он способен выдерживать значительные нагрузки без деформации или разрушения. Это делает его полезным при проектировании и производстве механизмов, работающих в условиях высокого давления.
Нитрит металла также обладает высокой электропроводностью. Это позволяет использовать его в электронике и электротехнике для создания эффективных и надежных элементов и устройств.
В целом, благодаря своим уникальным техническим свойствам, нитрит металла находит широкое применение в различных промышленных отраслях, таких как производство химических веществ, энергетика, машиностроение и другие.
Риск пользования нитритом металла

Нитрит металла – вещество с высокой реактивностью и способностью образовывать опасные соединения при взаимодействии с другими веществами. Пользование нитритом металла несет определенные риски и требует особой осторожности.
Первое свойство, с которым необходимо быть внимательным, – это его окислительная способность. Нитрит металла может вызывать образование горючих и взрывоопасных смесей при контакте с органическими или другими воспламеняющимися веществами. Для минимизации риска возгорания необходимо хранить нитрит металла в плотно закрытых контейнерах, далеко от источников открытого огня.
Важно учитывать также его токсичность. При вдыхании нитрита металла или контакте с кожей может возникнуть отравление. Нитрит металла является раздражающим веществом и может вызывать ожоги, аллергические реакции и проблемы с дыхательной системой. При работе с нитритом металла необходимо использовать соответствующую индивидуальную защиту – респираторы, перчатки, защитные очки.
Помимо этого, нитрит металла может провоцировать коррозию других материалов. Если он окажется в контакте с металлическими поверхностями, это может привести к повреждению и даже разрушению оборудования. Необходимо быть внимательным и предусмотреть дополнительные меры по защите поверхностей, если они будут подвержены влиянию нитрита металла.
Из-за всех этих рисков, пользование нитритом металла требует строгого соблюдения правил безопасности и контроля за его использованием. Для обеспечения безопасной работы с ним необходимо проводить обучение персонала, использовать специальное оборудование и контролировать условия хранения и использования.
Вопрос-ответ

Какова формула нитрита металла кислород?
Формула нитрита металла кислород зависит от конкретного металла. Например, для нитрита натрия формула NaNO2, для нитрита калия - KNO2
Какие свойства имеет нитрит металла кислород?
Нитрит металла кислород обладает рядом свойств. Он является солью нитритной кислоты, обладает слабой щелочной реакцией и может быть растворимым в воде или других растворителях. Он также может быть токсичным и имеет специфический запах.
В каких областях применяют нитрит металла кислород?
Нитрит металла кислород имеет широкое применение. Например, его используют в пищевой промышленности в качестве консерванта и антиоксиданта. Также он находит применение в медицине как вазодилататор, а в некоторых случаях может использоваться и в промышленности для производства взрывчатых веществ.
Какие особенности у нитрита металла кислород?
Нитрит металла кислород обладает несколькими особенностями. Он может быть очень реактивным и нестабильным в некоторых условиях. Также он может образовывать взрывчатые смеси с некоторыми другими веществами. Важно соблюдать меры предосторожности при работе с ним, так как он может быть токсичным и вызывать раздражение кожи и слизистых оболочек.
