Нитрат металла серной кислоты - это соединение, образующееся в результате взаимодействия металлов с нитратной группой (NO3-) серной кислоты (H2SO4). Это вещество обладает рядом уникальных свойств, которые делают его полезным для различных промышленных и научных приложений.
Во-первых, нитраты металлов серной кислоты являются хорошими окислителями и могут использоваться в реакциях окисления-восстановления. Они способны передавать кислородные атомы другим веществам, что делает их полезными для процессов синтеза и анализа органических соединений.
Во-вторых, нитраты металлов серной кислоты обладают высокой стабильностью и способностью растворяться в воде. Это делает их прекрасными реагентами для проведения химических реакций в водной среде. Кроме того, их растворы обычно являются прозрачными и безцветными, что облегчает наблюдение за процессами, происходящими во время реакций.
Наконец, нитраты металлов серной кислоты находят применение в различных отраслях промышленности. Они используются в производстве взрывчатых веществ, глазированных керамических изделий, пигментов для красок и многих других материалов.
Примечательно, что некоторые нитраты металлов, например нитрат аммония (NH4NO3), являются одними из самых мощных окислителей и могут использоваться в производстве ракетного топлива и взрывчатых веществ.
Свойства нитрата металла
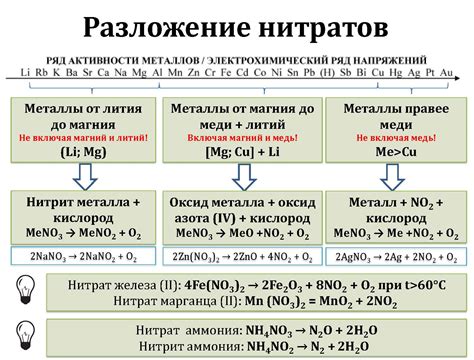
Нитрат металла - это химическое соединение, состоящее из металла и ионов нитрата. Оно обычно представляет собой кристаллическую соль, растворимую в воде.
Нитраты металла обладают различными физическими и химическими свойствами в зависимости от типа металла. Они могут быть твердыми или жидкими при комнатной температуре, иметь разнообразные цвета и обладать различной степенью растворимости в разных средах.
Важным свойством нитратов металла является их способность к окислению и восстановлению. Они могут служить как окислителями, так и восстановителями в химических реакциях. Это свойство делает их полезными в различных промышленных процессах и лабораторных исследованиях.
Нитраты металла также могут обладать термической стабильностью, то есть сохранять свои свойства при высоких температурах. Это делает их полезными в процессах, требующих нагрева или высоких температур, например, при производстве керамики или в ракетно-космической отрасли.
Нитраты металла широко применяются в различных областях, включая химическую промышленность, фармацевтику, производство удобрений, производство пиротехнических изделий, каталитические процессы и многое другое. Их свойства и применение могут быть уникальными для каждого конкретного металла, что делает их важными объектами научных исследований.
Химическое соединение с металлом

Нитрат металла серной кислоты представляет собой химическое соединение металла и нитратной группы, образующейся в результате реакции металла с серной кислотой.
В зависимости от металла, с которым образуется нитрат, свойства данного соединения могут значительно различаться. Например, нитрат металла серной кислоты может быть растворимым или нерастворимым в воде, обладать определенной степенью термической стабильности и иметь разнообразные цветовые характеристики.
Химические соединения с металлом, включая нитраты, широко используются в различных областях науки и техники. Например, нитраты металлов серной кислоты находят применение в процессах окрашивания и пигментации, а также в производстве взрывчатых веществ. Кроме того, нитраты могут использоваться в качестве удобрений для растений, так как содержащийся в них азот является основным элементом питания для растений.
Химическое соединение с металлом, такое как нитрат металла серной кислоты, представляет собой важный объект исследований в области химии и материаловедения. Ученые изучают его свойства и возможности применения, с целью создания новых материалов с определенными химическими и физическими характеристиками.
Свойства нитрата металла серной кислоты

Нитрат металла серной кислоты (NO3)2 — химическое соединение, представляющее собой соль серной кислоты и металла, где металл является катионом. Нитраты металла серной кислоты обладают некоторыми уникальными свойствами и находят применение в различных областях.
Одним из главных свойств нитратов металла серной кислоты является их растворимость в воде. Большинство нитратов металла серной кислоты легко растворяются в воде, образуя прозрачные растворы. Это делает их удобными для использования в различных процессах и реакциях.
Нитраты металла серной кислоты обладают высокой термической стабильностью. Они могут выдерживать высокие температуры без разложения, что позволяет использовать их в высокотемпературных процессах. Кроме того, некоторые нитраты металла серной кислоты обладают способностью к термическому разложению, что может быть использовано в производстве взрывчатых веществ.
Нитраты металла серной кислоты также имеют важные электрохимические свойства. Они могут выступать в роли окислителя или восстановителя в реакциях электрохимического окисления и восстановления. Это делает их полезными в производстве и хранении электрической энергии в батареях.
В заключение, нитраты металла серной кислоты — это важные соединения с уникальными свойствами. Их высокая растворимость, термическая стабильность и электрохимические свойства делают их полезными в различных областях, включая химическую и электрохимическую промышленность, а также взрывчатые вещества.
Основные физико-химические свойства

Нитрат металла серной кислоты (MNO3) представляет собой соль, образованную в результате реакции металла с серной кислотой. Имеет вид кристаллического вещества, обладает высокой степенью растворимости в воде.
При комнатной температуре нитрат металла серной кислоты является бесцветным или белым кристаллическим порошком. Он обладает слабым характерным запахом, который может быть заметен только в высоких концентрациях. Нитрат металла серной кислоты обладает резким вкусом и обычно является ядовитым веществом.
Одним из главных свойств нитратов металла серной кислоты является их способность окисляться. Взаимодействие нитратов металла серной кислоты с другими веществами может привести к образованию различных соединений, в том числе взрывчатых. Поэтому нитраты металла серной кислоты обычно хранятся в специальных условиях и требуют особой осторожности при обращении с ними.
Также следует отметить, что нитраты металла серной кислоты обладают высокой устойчивостью к высоким температурам. Это делает их применимыми в разных отраслях промышленности, например, в производстве пиротехники, в процессе катализа реакций или в качестве катализаторов. Кроме того, нитраты металла серной кислоты могут использоваться в процессе создания различных лакокрасочных материалов, удобрений или в качестве добавки в пищевую промышленность.
Применение нитрата металла и серной кислоты
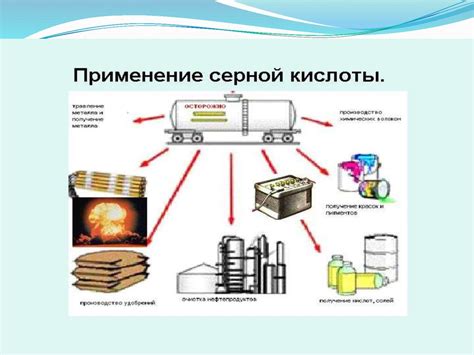
Нитрат металла является химическим соединением, состоящим из металла и нитратного иона. Он находит широкое применение в различных отраслях промышленности и научных исследованиях.
Одним из основных применений нитрата металла является его использование в процессах окисления и химического синтеза. Нитраты металла могут служить источником кислорода или окислителя в различных реакциях, способствуя образованию новых соединений с заданными свойствами.
Также нитраты металла широко применяются в производстве удобрений. Они содержат азот, который является одним из основных элементов, необходимых для роста и развития растений. При добавлении нитратов металла в почву, растения получают дополнительный источник азота, что способствует их более активному росту и повышению урожайности.
Серная кислота также имеет множество применений в различных отраслях промышленности и научных исследованиях.
Одним из ключевых применений серной кислоты является ее использование в производстве удобрений. Серная кислота является одним из основных источников серы, которая является важным макроэлементом для растений. При добавлении серной кислоты в почву, растения получают необходимый запас серы, что способствует их здоровому росту и развитию.
Также серная кислота применяется в процессах очистки воды от загрязнений. Она является эффективным дезинфицирующим средством и может использоваться для уничтожения бактерий и других микроорганизмов, оказывающих воздействие на качество воды.
В области производства химических веществ и материалов серная кислота служит важным компонентом многих процессов. Она используется в производстве пластмасс, удобрений, красителей, аккумуляторов и многих других продуктов. Ее кислотные свойства делают ее востребованным реагентом в различных химических реакциях и процессах синтеза.
Вопрос-ответ

Какие свойства имеет нитрат металла серной кислоты?
Нитраты металлоидов серной кислоты (H2SO4), такие как аммоний, медь, свинец, железо и т. д., обычно существуют в виде кристаллических соединений. Они растворяются в воде, образуя растворы, которые могут быть безцветными либо иметь различные оттенки в зависимости от конкретного металла. Нитраты металла серной кислоты обладают высокой стабильностью и не очень хорошей проводимостью электрического тока.
В каких областях применяются нитраты металла серной кислоты?
Нитраты металла серной кислоты имеют широкий спектр применений. В медицине они используются для лечения различных заболеваний, таких как ангина, инфекции мочевыводящих путей и т. д. Они также находят применение в производстве пиротехнических смесей, удобрений и красителей. В некоторых промышленных процессах они используются в качестве катализаторов и окислителей. Еще одно важное применение нитратов металла серной кислоты - в производстве взрывчатых веществ и военной промышленности.
Каковы основные особенности нитратов металла серной кислоты?
Основная особенность нитратов металла серной кислоты - их высокая стабильность и низкая проводимость электрического тока. Это делает их полезными в различных областях, таких как медицина, производство удобрений и красителей, пиротехника и т. д. Кроме того, нитраты металла серной кислоты обладают хорошей растворимостью в воде, что облегчает их использование в различных приложениях.
