Нитрат алюминия является химическим соединением, представляющим собой соль алюминия и азотной кислоты. Это вещество обладает широким спектром взаимодействия с различными металлами и находит применение в различных областях.
Одним из основных аспектов взаимодействия нитрата алюминия с металлами является его способность к окислительным реакциям. В реакциях среды нитрата алюминия может проявлять свои окислительные свойства, что позволяет использовать его в процессах синтеза и окисления металлов.
Важным аспектом взаимодействия нитрата алюминия с металлами является его способность образовывать комплексные соединения. Благодаря этому свойству, нитрат алюминия может использоваться в качестве стабилизирующего агента при синтезе комплексных соединений металлов, а также в качестве катализатора в различных химических реакциях.
Применение нитрата алюминия в различных областях включает его использование в производстве фертильных составов для сельского хозяйства, в качестве ингибитора коррозии металлических поверхностей, в процессах электрохимического осаждения металлов и других областях промышленности.
Химический состав и свойства нитрата алюминия

Нитрат алюминия (Al(NO3)3) представляет собой кристаллическое соединение, состоящее из алюминия и нитратного иона. Это бесцветные кристаллы с мелкими игольчатыми зернами. Вещество хорошо растворимо в воде и обладает высокой температурой плавления.
Химический состав нитрата алюминия позволяет ему обладать рядом уникальных свойств. Оно является сильным окислителем и способно реагировать с различными веществами, в том числе с металлами. Также нитрат алюминия образует соли с различными кислотами, что делает его важным сырьем для получения других химических соединений.
Нитрат алюминия обладает высокой стабильностью и реакционной способностью. При взаимодействии с металлами, например, железом или медью, происходит образование соответствующих солей. Это явление можно использовать для различных технологических процессов, включая гальваническое покрытие, производство сплавов и прочих химических реакций.
Свойства нитрата алюминия также определяют его применение в различных отраслях промышленности. Он используется как катализатор, окислитель, высокоэффективный компонент удобрений. Нитрат алюминия также имеет применение в фотографии, производстве пиротехники и как добавка в промышленных и бытовых реагентах.
Физические и химические свойства металлов

Металлы обладают рядом характерных физических и химических свойств, которые отличают их от других веществ.
Физические свойства:
- Проводимость тепла и электричества. Металлы являются отличными проводниками тепла и электричества из-за свободно движущихся электронов в их структуре.
- Пластичность и формоизменяемость. Металлы обладают способностью деформироваться без разрушения и принять желаемую форму.
- Металлический блеск. Металлы отражают свет и обладают характерным металлическим блеском.
- Твердость. Металлы могут быть как мягкими (например, свинец), так и очень твердыми (например, кремний).
- Высокая плотность. Металлы обладают высокой плотностью, что делает их тяжелыми в сравнении с другими веществами.
Химические свойства:
- Коррозионная стойкость. Некоторые металлы, такие как алюминий и нержавеющая сталь, обладают способностью образовывать защитные оксидные пленки на поверхности, что предотвращает их дальнейшую коррозию.
- Реактивность с кислотами. Многие металлы реагируют с кислотами, образуя соли и выделяя водород.
- Способность к образованию сплавов. Металлы могут образовывать сплавы с другими металлами, что позволяет получать материалы с новыми свойствами.
- Каталитическая активность. Некоторые металлы обладают способностью ускорять химические реакции в качестве катализаторов.
- Магнитные свойства. Некоторые металлы имеют магнитные свойства и способность притягиваться к магниту.
Эти физические и химические свойства металлов определяют их широкое применение в различных отраслях промышленности и технологии.
Реакции нитрата алюминия с различными металлами
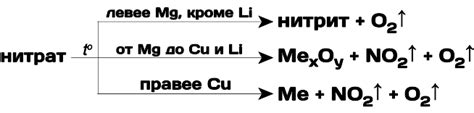
Нитрат алюминия - это химическое соединение, состоящее из алюминия и нитратного иона. Он может вступать в реакцию с различными металлами, образуя разнообразные продукты.
При взаимодействии нитрата алюминия с цинком происходит окислительно-восстановительная реакция. При этом алюминий окисляется, а цинк восстанавливается. В результате образуется алюминиевая фольга и цинковый нитрат.
С медью нитрат алюминия также может взаимодействовать. Однако в этом случае реакция протекает медленнее. Результатом реакции будет образование алюминиевой фольги и медного нитрата.
Если смешать нитрат алюминия с железом, то произойдет реакция, в результате которой образуется алюминиевая фольга и железный нитрат.
Реакция нитрата алюминия с магнием приводит к образованию алюминиевой фольги и нитрата магния.
Наконец, нитрат алюминия может реагировать с свинцом. В результате образуется алюминиевая фольга и нитрат свинца.
Особенности взаимодействия нитрата алюминия с щелочными металлами

Нитрат алюминия – это соль, образующаяся в результате растворения в воде оксида алюминия. Одной из особенностей взаимодействия нитрата алюминия является его реакция с щелочными металлами.
Щелочные металлы – это элементы первой группы периодической системы: литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs), франций (Fr). При контакте нитрата алюминия с щелочными металлами происходит реакция, сопровождающаяся выделением большого количества тепла.
Во время взаимодействия нитрата алюминия с щелочными металлами образуется соответствующий нитрат щелочного металла и алюминий в металлической форме. Реакция происходит в следующем виде:
- 2Al(NO3)3 + 6Na → 6NaNO3 + 2Al
Уравнение реакции показывает, что алюминий переходит из оксидного состояния (в нитрате алюминия) в металлическое состояние. При этом образуются нитраты щелочных металлов.
Данное взаимодействие можно использовать в различных сферах при производстве, например в пиротехнике для создания эффектов взрывов или искр. Также нитрат алюминия с щелочными металлами используется в процессе получения алюминия в металлической форме.
Взаимодействие нитрата алюминия с переходными металлами

Нитрат алюминия – соединение, используемое в качестве источника алюминия и нитрогруппы в различных процессах и реакциях. Одно из интересных направлений его применения связано с взаимодействием с переходными металлами. Переходные металлы, такие как железо, медь, никель и многие другие, являются важными катализаторами в различных процессах, и их соединения могут обладать разнообразными свойствами, которые можно использовать в различных промышленных процессах.
Взаимодействие нитрата алюминия с переходными металлами может привести к образованию различных продуктов реакции. Например, при взаимодействии с железом может образоваться нитрат алюминия и гидроксид железа. При этом происходит окислительное взаимодействие, в результате которого алюминий окисляет железо, а сам становится ионом алюминия. Аналогичные реакции могут происходить и с другими переходными металлами.
Интересно, что нитрат алюминия может также взаимодействовать с различными комплексными соединениями переходных металлов, образуя комплексы. Комплексные соединения обладают особыми свойствами и используются в качестве катализаторов, ингибиторов и в других процессах.
Взаимодействие нитрата алюминия с переходными металлами имеет большой потенциал в различных областях применения, включая промышленную и органическую синтезы, электрохимические процессы и другие. Дальнейшие исследования и разработки в этой области позволят расширить спектр применения нитрата алюминия и оптимизировать процессы, в которых он используется.
Реакции нитрата алюминия с редкоземельными металлами
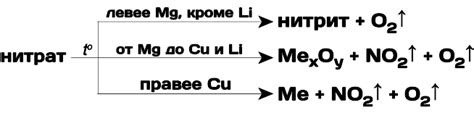
Нитрат алюминия - соединение, которое может активно реагировать с редкоземельными металлами. Редкоземельные металлы представляют собой группу металлов, которые встречаются в природе в небольших количествах и имеют уникальные химические свойства. Эти металлы используются в различных областях науки и техники, включая электронику, магнитные материалы и катализаторы.
Взаимодействие нитрата алюминия с редкоземельными металлами может происходить при различных условиях, но обычно включает нагревание или растворение в воде. В результате реакции образуются различные соединения, включая нитраты редкоземельных металлов и гидроксид алюминия.
Реакции нитрата алюминия с редкоземельными металлами могут быть использованы для получения новых соединений с интересными свойствами. Например, нитраты редкоземельных металлов, полученные в результате реакции, могут использоваться в процессе синтеза новых материалов с улучшенными магнитными, оптическими или электрическими свойствами.
Кроме того, реакции нитрата алюминия с редкоземельными металлами могут быть использованы для получения катализаторов, которые могут быть применены в различных промышленных процессах. Например, такие катализаторы могут применяться в процессе производства пластмасс, фармацевтических веществ или химических волокон.
Практическое применение реакции нитрата алюминия с металлами

Реакция нитрата алюминия с металлами имеет широкое практическое применение в различных отраслях промышленности и научных исследованиях.
Одним из основных применений этой реакции является получение металлов и их сплавов. При взаимодействии нитрата алюминия с металлами, например магнием или цирконием, происходит образование соответствующих металлических соединений. Такие соединения могут быть использованы в производстве различных изделий, включая авиационные и автомобильные детали, электронные компоненты и промышленные каталитические системы.
Кроме того, реакция нитрата алюминия с металлами может быть использована для получения порошковых материалов. Образовавшиеся соединения представляют собой порошок, который может быть использован в лазерного пакетирования, 3D-печати, производстве керамических изделий и других технологиях. Порошок, полученный из нитрата алюминия и металлов, обладает высокой чистотой и хорошими свойствами, что позволяет использовать его в различных областях промышленности.
Реакция нитрата алюминия с металлами также может быть использована в научных исследованиях. Эта реакция позволяет изучать физико-химические свойства металлических соединений, исследовать их структуру и свойства. Такие исследования могут быть полезными для разработки новых материалов и технологий, а также для изучения реакций между металлами и другими веществами.
В целом, реакция нитрата алюминия с металлами имеет широкий спектр практического применения и служит основой для получения металлических соединений, порошковых материалов и проведения научных исследований. Такое разностороннее использование этой реакции свидетельствует о ее значимости в современных технологиях и науке.
Перспективы развития и исследования взаимодействия нитрата алюминия с металлами
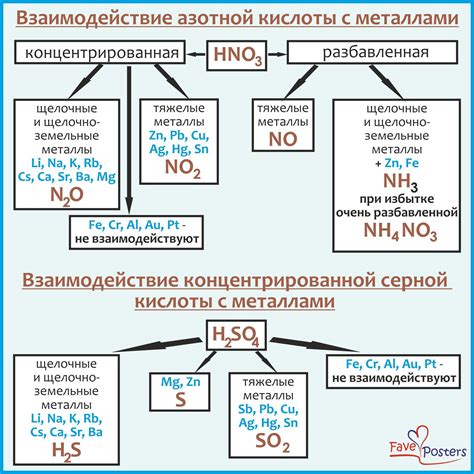
Взаимодействие нитрата алюминия с металлами является одной из актуальных тем в современной науке и промышленности. Оно представляет значительный потенциал для разработки новых материалов и технологий, а также для улучшения существующих.
Исследования в области взаимодействия нитрата алюминия с металлами имеют широкий спектр применений. Например, такие исследования позволяют разрабатывать новые составы сплавов с улучшенными физико-химическими и механическими свойствами. Это может быть особенно полезно в промышленности, где требуются материалы с высокой прочностью, стойкостью к коррозии и температурными перепадами.
Кроме того, изучение взаимодействия нитрата алюминия с металлами может привести к улучшению методов обработки и сварки металлов. Использование нитрата алюминия в качестве добавки или покрытия позволяет добиться более качественного стыка металлических деталей, что снижает риск возникновения дефектов и повышает надежность конструкций.
Дополнительно, исследование взаимодействия нитрата алюминия с металлами также имеет значение в сфере энергетики. Оно может способствовать разработке новых материалов для эффективных систем хранения и преобразования энергии, таких как аккумуляторы и топливные элементы. Понимание процессов, происходящих при взаимодействии нитрата алюминия с металлами, открывает новые возможности для создания экологически чистых и высокоэффективных энергетических устройств.
Вопрос-ответ

Что такое нитрат алюминия?
Нитрат алюминия - это соединение алюминия и азотной кислоты. Его химическая формула - Al(NO3)3. Это белый кристаллический порошок, который хорошо растворяется в воде. Нитрат алюминия также называется алюминиевой селитрой.
Какое взаимодействие нитрата алюминия с металлами?
Нитрат алюминия может реагировать с разными металлами. Эта реакция может протекать с выделением тепла и/или газов. Например, при контакте с железом, нитрат алюминия окисляет железо, образуя оксиды и азот оксиды. Взаимодействие нитрата алюминия с металлами может иметь различные практические применения.
Какие металлы реагируют с нитратом алюминия и для каких целей это используется?
Нитрат алюминия может реагировать с множеством металлов, включая железо, медь, цинк и другие. Реакция с железом может использоваться для отжига поверхности металла и удаления окислов. Реакция с медью используется для получения алюминиевой бронзы. Взаимодействие нитрата алюминия с разными металлами может применяться в металлургии, производстве сплавов и других отраслях промышленности.
Какова роль нитрата алюминия в процессе гальванического осаждения металлов?
Нитрат алюминия может использоваться в качестве компонента электролита при гальваническом осаждении металлов. В данном процессе, нитрат алюминия участвует в формировании пленки на поверхности металла, которая способствует равномерной и стабильной осаждению металла. Это позволяет получить качественные покрытия на металлических изделиях при проведении гальванических работ.
