Щелочные металлы, такие как литий, натрий, калий, рубидий и цезий, являются элементами первой группы периодической системы. Они обладают уникальными свойствами и широко применяются в различных сферах, начиная от обычного бытового использования до применения в промышленности и научных исследованиях. Соединения щелочных металлов имеют особенности, которые делают их особо интересными для изучения и применения.
Одним из основных методов получения соединений щелочных металлов является реакция металла с кислотой. Она протекает с образованием соли и выделением водорода. Например, реакция калия с серной кислотой приводит к образованию сульфата калия и выделению водорода. Этот метод широко используется в лабораторных условиях для получения соединений щелочных металлов в чистом виде.
Вторым методом получения соединений щелочных металлов является реакция металла с оксидом или гидроксидом другого щелочного металла. Например, реакция натрия с гидроксидом калия приводит к образованию гидроксида натрия и гидроксида калия. Этот метод также применяется для получения соединений щелочных металлов в промышленных масштабах.
Соединения щелочных металлов обладают рядом интересных свойств. Например, они хорошо растворяются в воде и образуют щелочные растворы. Кроме того, они обладают высокой электропроводностью и используются в производстве аккумуляторов и электролитов. Также соединения щелочных металлов широко применяются в стекольной промышленности для придания специальных свойств стеклу.
Особенности соединений щелочных металлов
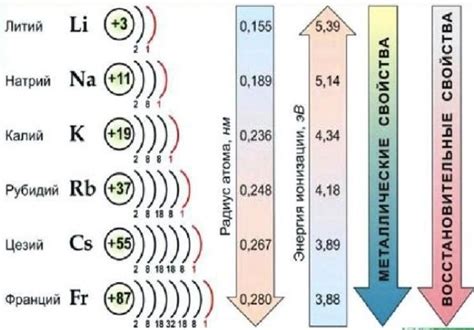
Щелочные металлы - это элементы первой группы периодической таблицы, которые включают литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Они характеризуются высокой активностью и реакционностью из-за наличия одной электронной оболочки с одним электроном.
Соединения щелочных металлов имеют ряд особенностей, которые делают их уникальными. Первое, на что следует обратить внимание, это образование щелочных гидридов. Щелочные металлы реагируют с водородом и образуют гидриды, которые могут быть использованы в различных химических процессах.
Другая особенность соединений щелочных металлов заключается в их способности образовывать сольные растворы. Это связано с высокой растворимостью щелочных металлов в воде. Сольные растворы щелочных металлов являются хорошими электролитами и используются в различных областях, включая химическую промышленность и медицину.
Некоторые соединения щелочных металлов обладают пирофорными свойствами. Это значит, что они могут воспламеняться при контакте с воздухом или водой. Это свойство делает эти соединения опасными и требует особой осторожности при их хранении и использовании.
Одной из важных особенностей соединений щелочных металлов является их высокая основность. Щелочные металлы образуют сильные щелочи, которые широко используются в разных областях, включая производство мыла, стекла и бумаги.
Таким образом, соединения щелочных металлов обладают рядом особенностей, которые делают их важными для множества приложений в различных отраслях промышленности и научных исследований.
Методы получения соединений щелочных металлов

Соединения щелочных металлов можно получить различными методами, в зависимости от требуемых свойств и состава исходных материалов.
1. Реакция металла с кислородом
Один из основных методов получения соединений щелочных металлов - реакция металла с кислородом. В результате такой реакции образуются оксиды щелочных металлов, которые могут быть использованы в различных областях, например, в производстве стекла или керамики.
2. Реакция металла с водой
Другим способом получения соединений щелочных металлов является их реакция с водой. В результате такой реакции образуется щелочное гидроксидное соединение, например, щелочная сода или гидроксид натрия. Эти вещества широко применяются в различных отраслях, включая производство мыла, бумаги и стекла.
3. Электролиз солей
Также можно получать соединения щелочных металлов путем электролиза их солей. При этом происходит разложение соли на металлический катион и отрицательный анион, которые осаждается на электроды. Этот метод широко используется в промышленности для получения чистых металлов и сплавов, а также для получения щелочных гидроксидов.
4. Реакция металла с другими веществами
Некоторые соединения щелочных металлов можно получить путем их реакции с другими веществами. Например, реакцией натрия с хлоридом получается хлорид натрия, широко используемый в пищевой промышленности.
В итоге, методы получения соединений щелочных металлов разнообразны и позволяют получать вещества с различными свойствами для применения в различных областях науки и промышленности.
Свойства соединений щелочных металлов
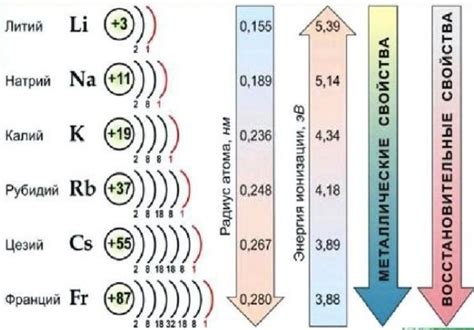
1. Растворимость: Соединения щелочных металлов, такие как гидроксиды и некоторые соли, обладают высокой растворимостью в воде. Это связано с положительным зарядом щелочных металлов, который позволяет им образовывать ионы в растворе. Некоторые из этих соединений образуют так называемые «светлые растворы», которые благодаря высокой растворимости щелочных металлов пропускают свет.
2. Щелочная реакция: Соединения щелочных металлов обладают щелочной реакцией. Они способны нейтрализовывать кислоты, образуя соли и воду. Благодаря этому свойству они часто используются в бытовой химии и промышленности, например, в производстве товаров для уборки и химических реактивов.
3. Проводимость: Щелочные металлы и их соединения обладают высокой электропроводностью. Это связано с наличием свободных электронов в их зоне проводимости. Это свойство используется в производстве электролитических растворов и электрических элементов.
4. Высокая температура плавления: Большинство соединений щелочных металлов обладают высокой температурой плавления. Это связано с наличием мощных межатомных связей, которые требуют большой энергии для перехода от твердого состояния в жидкое.
5. Флюоресценция: Некоторые соединения щелочных металлов обладают свойством флюоресценции, то есть способностью испускать свет под воздействием ультрафиолетового излучения. Это свойство используется в различных областях, включая медицину, экологию и оптику.
Вопрос-ответ

Какие существуют особенности соединений щелочных металлов?
Особенности соединений щелочных металлов включают высокую степень реакционной способности, низкую температуру плавления и кипения, а также возможность образования растворов с водой.
Какие методы синтеза щелочных металлов наиболее распространены?
Наиболее распространенными методами синтеза щелочных металлов являются электролиз, термический разложение соединений и восстановление металлов.
Какие свойства имеют соединения щелочных металлов?
Соединения щелочных металлов обладают высокой ионной проводимостью, хорошей растворимостью в воде, а также свойством образования кристаллической решетки.
Какова роль щелочных металлов в химических реакциях?
Щелочные металлы играют важнейшую роль в химических реакциях, так как они служат активными агентами протекающих процессов и могут выступать в качестве катализаторов.
Какие свойства щелочных металлов делают их полезными в промышленности?
Свойства щелочных металлов, такие как низкая плотность, хорошая теплопроводность и высокая реакционная способность, делают их полезными для использования в различных отраслях промышленности, включая производство стекла, луженых металлов и щелочей.
