Реакция между азотной кислотой (HNO3) и металлами широко изучена в химии и имеет важное практическое применение. В ходе этой реакции происходит окисление металла, при котором выделяются оксиды и происходит образование нитратов. Однако, стоит отметить, что с некоторыми металлами, такими как золото (Au), платина (Pt) и ряд других, реакция с азотной кислотой не приводит к образованию нитратов или солей воды. Вместо этого происходит частичное или полное окисление металла, что может вызывать интерес в контексте изучения реактивности и использования данных металлов.
Это явление обусловлено тем, что азотная кислота является сильным окислителем и может приводить к образованию нитратных и нитритных ионов. В случае с металлами, с которыми не образуются нитраты или нитриты, считается, что они обладают высокой устойчивостью и не подвергаются окислению в присутствии азотной кислоты. Это свойство можно использовать при различных химических исследованиях, а также в промышленности при обработке и использовании данных металлов.
Интересно отметить, что реакция между азотной кислотой и металлами может протекать не только в водном растворе, но и в других средах, таких как сухие смеси или в самом металле. Это позволяет расширить возможности применения этой реакции и исследовать различные аспекты взаимодействия азотной кислоты с металлами.
В итоге, отсутствие образования соли воды при реакции азотной кислоты с определенными металлами является интересным исследовательским наблюдением, который может найти применение в различных областях науки и технологии. Данное явление открывает дополнительные возможности для изучения реакций окисления-восстановления и позволяет лучше понять особенности взаимодействия азотной кислоты с металлическими системами.
Реакция азотной кислоты с металлами: отсутствие образования соли воды
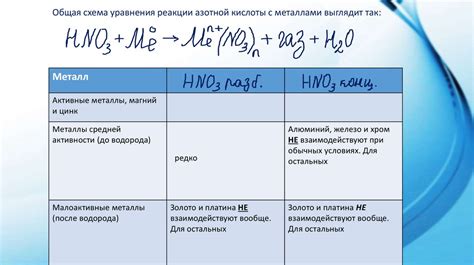
Реакция азотной кислоты с металлами является важным объектом изучения в химии. Обычно, при взаимодействии кислоты с металлами, образуется соль и выделяется водород. Однако, при реакции азотной кислоты с металлами, образование соли воды отсутствует.
При обычных условиях, азотная кислота взаимодействует с металлами с выделением оксида азота и образованием коррозионного слоя на поверхности металла. Однако, эта реакция не приводит к образованию соли воды, так как азотная кислота сама по себе не образует ионы, способные реагировать с металлом.
Причем, модификация азотной кислоты, содержащей более высокую концентрацию азота, также не приводит к образованию соли воды при взаимодействии с металлами. Это объясняется тем, что азотная кислота не обладает свойствами образования ионов водорода, которые могли бы реагировать с металлами.
Таким образом, реакция азотной кислоты с металлами не приводит к образованию соли воды, что отличает данную реакцию от типичных реакций кислоты с металлом. Это явление требует дальнейшего изучения и может быть использовано в различных приложениях, например, при использовании азотной кислоты в химической промышленности.
Особенности реакции на практике

Реакция азотной кислоты с металлами, такими как медь, железо и алюминий, представляет собой интересное явление, обладающее несколькими особенностями.
Во-первых, во время реакции происходит выделение обильного количества газа – это одна из специфических характеристик данного процесса. Газ, возникающий при взаимодействии азотной кислоты с металлами, является азотной оксидом и обладает резким запахом.
Во-вторых, удивительно, но при этой реакции не образуется соль. Обычно, когда кислота вступает в реакцию с металлом, происходит образование соли и выделение водорода. Но в данном случае, за счет особого химического состава азотной кислоты, отсутствует образование соли и вместо этого происходит выделение азотной оксиды.
Одной из причин такой особенности являются свойства азотной кислоты, включая ее сильную окислительную способность. Когда металл вступает в реакцию с азотной кислотой, происходят окислительно-восстановительные процессы, и в результате образуется азотной оксид. Это объясняет отсутствие образования соли при данной реакции.
Такие особенности реакции азотной кислоты с металлами сделали ее предметом научных исследований и зрелищным экспериментом. Эта реакция проходит со значительным выделением газа и может быть потенциально опасной, поэтому требует особой осторожности при проведении в лабораторных условиях.
Образование оксида металла

При реакции азотной кислоты с металлами происходит образование оксида этого металла. Азотная кислота, взаимодействуя с металлом, окисляет его, что приводит к образованию соответствующего оксида. Оксид металла представляет собой химическое соединение, состоящее из атомов металла и кислорода.
Образование оксида металла возможно только при наличии металла, который может вступать в реакцию с азотной кислотой. Некоторые металлы обладают достаточной активностью, чтобы реагировать с азотной кислотой и образовывать соответствующие оксиды.
Оксиды металлов обладают различными физическими и химическими свойствами. Некоторые оксиды металлов представляют собой твёрдые вещества, другие - газы или жидкости. Они могут обладать различными цветами и иметь разные структуры.
Образование оксида металла при реакции азотной кислоты с металлами является одним из примеров химической реакции, которая происходит с участием кислот и металлов. Эта реакция является важной для химической промышленности и научных исследований, так как позволяет получать различные оксиды металлов, которые могут иметь различные применения в разных областях науки и технологии.
Окислительное действие азотной кислоты

Азотная кислота (HNO3) обладает сильным окислительным свойством, что делает ее востребованной в множестве химических реакций и промышленных процессах. Благодаря своей способности окислять различные вещества, азотная кислота применяется в производстве удобрений, взрывчатых веществ и других химических соединений.
При контакте с металлами азотная кислота проявляет свое окислительное действие, превращая металлы в соответствующие оксиды. В процессе реакции азотная кислота отдает свои кислородные атомы, которые окисляют металлы, превращаясь сама в азотокислоту соответствующего металла. В результате реакции образуется солевая основа, которая растворяется в воде.
Однако, в ряде случаев при взаимодействии азотной кислоты с определенными металлами, образуется соль, не обладающая способностью растворяться в воде. Это связано с рядом факторов, таких как концентрация и температура реакции, а также сами свойства металла.
Интересно, что образование соли воды при реакции азотной кислоты с металлами может быть изменено путем добавления других веществ. Например, при добавлении кислоты фосфорной, образующаяся соль будет обладать способностью растворяться в воде.
Сравнение с другими кислотами

Азотная кислота (HNO3) является одной из наиболее распространенных неорганических кислот и отличается от других кислот своими особенностями. В отличие от соляной кислоты (HCl) и серной кислоты (H2SO4), азотная кислота обладает свойством необразовывать соли воды при реакции с металлами.
Соляная кислота образует соли при реакции с металлами, поскольку ее кислотности достаточно для образования ионов металла и позволяет протекать реакцию отщепления атома водорода. В результате образуются соответствующие хлориды металлов.
Серная кислота также способна образовывать соли при реакции с металлами благодаря высокой кислотности, что позволяет протекать реакцию отщепления атома водорода и образованию соответствующих сульфатов металлов.
Концентрированная азотная кислота обеспечивает окислительные свойства, что делает ее более подходящей для реакций согласно своей характеристики донора протоно-окислителя. В таком случае металлы реагируют с кислотой, но не образуют соли воды, а вместо этого наблюдается образование оксидов металлов и оксидов азота.
Значение реакции в промышленности

Реакция азотной кислоты с металлами имеет важное значение в различных отраслях промышленности. Одним из основных применений данной реакции является производство удобрений.
Азотные удобрения являются необходимыми компонентами для обеспечения питания растений и повышения урожайности сельскохозяйственных культур. Реакция азотной кислоты с металлами позволяет получать азотные соединения, которые затем применяются в производстве удобрений.
Кроме того, реакция азотной кислоты с металлами является важным этапом в процессе получения азотной кислоты для химической промышленности. Азотная кислота широко используется в производстве различных химических соединений, таких как пластмассы, красители, взрывчатые вещества и другие продукты промышленности.
В процессе реакции азотной кислоты с металлами образуется азотная соль, которая может быть использована для получения других соединений. Например, нитраты металлов, полученные в результате данной реакции, могут быть использованы в производстве взрывчатых веществ или в качестве катализаторов в химической промышленности.
Таким образом, реакция азотной кислоты с металлами играет важную роль в производстве удобрений и химической промышленности, обеспечивая необходимые компоненты для роста растений и производства различных химических соединений.
Вопрос-ответ

Что происходит при реакции азотной кислоты с металлами?
При реакции азотной кислоты с металлами происходит образование азотнокислых солей и выделение диоксида азота.
Почему при реакции азотной кислоты с металлами не образуются соли?
Образование солей в реакции азотной кислоты с металлами зависит от металла. Если металл является активным и способен реагировать с кислородом, то образуются азотнокислые соли. Однако, если металл не может реагировать с кислородом, то при реакции с азотной кислотой не образуется соль.
Какова причина отсутствия образования солей при реакции азотной кислоты с некоторыми металлами?
Причина отсутствия образования солей при реакции азотной кислоты с некоторыми металлами заключается в их низкой активности. Низкоактивные металлы не способны реагировать с кислородом, который присутствует в азотной кислоте. Поэтому, в таких случаях, при взаимодействии с низкоактивным металлом азотная кислота не образует соли.
