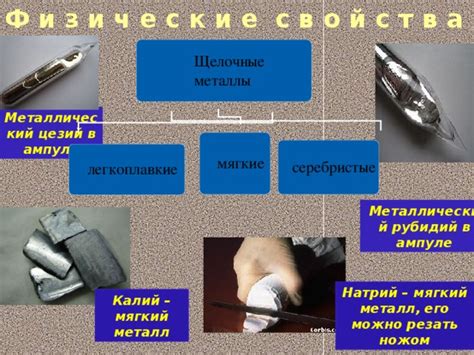
Натрий - химический элемент периодической системы, номер 11 в таблице Менделеева. Его открытие и изучение позволило ученым точно определить его состав и свойства. Этот элемент имеет атомный номер 11 и входит в группу щелочных металлов. Однако, некоторые исследования исследователей предлагают другую точку зрения на этот вопрос.
Одной из особенностей натрия является его реакция с водой, в результате которой образуется щелочная соль - гидроксид натрия. Этот процесс хорошо известен и применяется в различных областях, например, в производстве мыла и стекла. Более того, натрий имеет низкую плотность и низкую температуру плавления, что делает его привлекательным материалом для использования в различных инженерных и технических приложениях.
Однако привлекательность натрия как материала не является единственным критерием для определения его классификации. Исследования показали, что натрий обладает некоторыми характеристиками, которые отличают его от других щелочных металлов. Например, натрий имеет более слабый эффект щелочности и менее активное взаимодействие с кислородом. Кроме того, он имеет более высокую плотность и твердость по сравнению с другими щелочными металлами.
Таким образом, несмотря на то, что натрий обладает некоторыми характеристиками, характерными для щелочных металлов, его уникальные свойства и особенности позволяют некоторым ученым сомневаться в его принадлежности к этой группе. Дальнейшие исследования и эксперименты помогут нам лучше понять и классифицировать натрий и его место в периодической системе элементов.
Научное обоснование натрия
В химии натрий представляет собой щелочной металл, входящий в первую группу периодической системы. Он имеет атомный номер 11 и химический символ Na. Несмотря на свою активность, научное обоснование натрия также находится в его важной роли в органической и биологической химии.
Натрий является необходимым элементом для поддержания жизни в организмах. Он играет ключевую роль в регуляции баланса воды и электролитов, участвует в передаче нервных импульсов и сокращении мышц. Кроме того, он содержится в составе многих интревитаминов и ферментов, которые обеспечивают жизненно важные процессы в организме.
Научные исследования показывают, что натрий влияет на работу сердца и кровеносной системы. Как и другие щелочные металлы, он способен усилить действие гормонов, что может приводить к повышению артериального давления. Однако, необходимо помнить, что натрий потребляется в организме в разумных количествах, и его избыток может вызывать негативные последствия для здоровья.
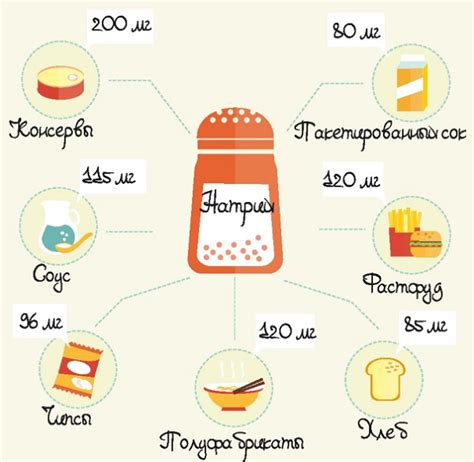
Общеизвестно, что поваренная соль (хлорид натрия) являет основным источником натрия в питании человека. Однако, избыточное потребление соли может быть причиной гипертонии и сердечно-сосудистых заболеваний. Следовательно, контроль потребления натрия в виде соли является важным мероприятием для поддержания здоровья и хорошего самочувствия.
Научное обоснование натрия показывает, что этот элемент играет важную роль в организмах, участвуя в регуляции баланса воды и электролитов, передаче нервных импульсов и работе сердца. Однако, необходимо помнить о нужном дозировании и контроле потребления натрия из различных источников, чтобы избежать возможных негативных последствий для здоровья.
Химические свойства натрия

Натрий (Na) - щелочной металл, обладающий рядом химических свойств, которые делают его одним из наиболее важных и широко используемых элементов в химии и промышленности.
Первое и наиболее известное свойство натрия - его высокая реактивность. Натрий реагирует быстро с водой, образуя гидроксид натрия и выделяя водород. Эта реакция является экзотермической, то есть сопровождается выделением тепла и образованием пламени.
Натрий также реагирует с большинством неметаллов, образуя соответствующие соли. Эта способность делает натрий важным реагентом в органической химии, используемым для синтеза различных органических соединений.
Важным свойством натрия является его способность образовывать ионы Na+, которые широко используются в ряде химических реакций и в промышленных процессах. Катионы натрия имеют достаточно низкую энергию ионизации, что делает их стабильными и легкими в использовании в качестве химических реагентов.
Внешне натрий является мягким металлом, который легко режется ножом. Однако, вследствие высокой реактивности, натрий должен храниться в аргоновой среде или покрытый слоем паравосковой кислоты для предотвращения его окисления.
Также натрий широко используется в промышленности для производства различных продуктов, таких как стекло, щелочные и солевые растворы, синтез органических соединений и многое другое.
Научные аргументы о классификации натрия

Натрий является щелочным металлом, что подтверждается научными исследованиями и классификацией элементов по своим физико-химическим свойствам.
Во-первых, натрий имеет очень низкую электроотрицательность, что говорит о его способности активно взаимодействовать с другими химическими элементами. Эта особенность характерна для щелочных металлов, включая натрий.
Во-вторых, натрий имеет низкую плотность и низкую температуру плавления, что также характерно для щелочных металлов. Эти свойства позволяют натрию быстро реагировать с водой, образуя щелочь, и использоваться в различных промышленных процессах.
Кроме того, натрий имеет химические свойства, позволяющие ему легко образовывать ионы Na+ в растворах. Это также характерно для щелочных металлов, которые образуют положительные ионы, обладающие высокой подвижностью.
Таким образом, научные аргументы о классификации натрия подтверждают его принадлежность к группе щелочных металлов. Это связано с его физико-химическими свойствами, такими как низкая электроотрицательность, низкая плотность, низкая температура плавления и способность образовывать положительные ионы в растворах.
Вопрос-ответ

Научное обоснование натрия как щелочного металла?
Натрий является щелочным металлом по признаку своей химической активности. Он легко реагирует с водой, выделяя водородный газ, и образует щелочную среду. Также натрий обладает свойствами щелочных металлов, такими как низкая плотность, низкая температура плавления, способность образовывать ионы Na+. Эти признаки научно подтверждают его статус щелочного металла.
Почему натрий не считается полноценным щелочным металлом?
Натрий обладает некоторыми особенностями, которые не совпадают полностью со свойствами типичных щелочных металлов. Например, он имеет большую плотность и высокую температуру плавления по сравнению с другими щелочными металлами. Также существуют и другие элементы, например аммоний, которые могут образовывать с натрием сходные соединения, но не являются щелочными металлами. Поэтому, хотя натрий обладает многими свойствами щелочного металла, он не полностью удовлетворяет их характеристикам и поэтому не считается полноценным щелочным металлом.