Металлы - это класс веществ, отличающихся определенными свойствами, такими как хорошая электропроводность, блестящий внешний вид и способность образовывать ионы положительного заряда. Наиболее типичным металлом считается железо, обладающее электронной формулой Fe.
Электронная формула металла представляет собой запись его электронной конфигурации, то есть расположение электронов в атоме металла. В случае железа эта формула выглядит следующим образом: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Всего в атому железа 26 электронов.
Железо входит в число самых распространенных металлов на Земле и используется во многих отраслях промышленности, а также в медицине, электронике и других сферах. Благодаря своим свойствам, железо широко применяется для изготовления различных конструкций, механизмов и изделий, в том числе стальных и чугунных. Это делает его наиболее типичным и значимым представителем металлов.
Наиболее обычный материал обладает электронным составом
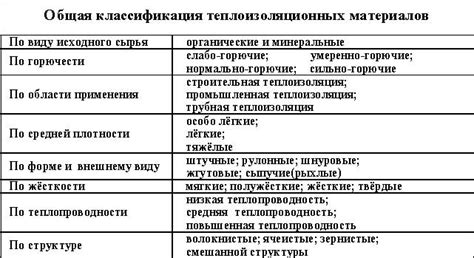
Электронный состав вещества является одной из основных характеристик, определяющих его свойства. Электроны - элементарные частицы, которые находятся вокруг атомного ядра и обладают отрицательным электрическим зарядом. В различных материалах, электроны могут находиться на разных энергетических уровнях и образовывать электронные облака или оболочки.
В наиболее обычном материале, электронная формула определяется числом электронов во внешней оболочке атомов. Такие материалы называются простыми веществами или элементами, и их электронные формулы принято записывать в виде химических символов и чисел. Например, водород - H, у которого во внешней оболочке один электрон, или кислород - O, где в внешней оболочке находятся шесть электронов.
Однако, для понимания свойств материала важно не только знать его электронную формулу, но и понимать структуру электронных облаков. В окружности каждого атома находятся энергетические уровни, на которых располагаются электроны. Электроны на наиболее нижнем уровне имеют наименьшую энергию и наибольшую близость к атому. Электроны в более высоких уровнях имеют большую энергию и наибольшую возможность для взаимодействия с другими атомами.
Таким образом, электронный состав материала определяет его химические и физические свойства. Количество и расположение электронов в атомах влияет на химическую активность, проводимость и теплопроводность материала. Понимание электронной формулы и структуры вещества позволяет ученым создавать новые материалы с определенными свойствами и применять их в различных областях науки и техники.
Углерод - самый распространенный элемент в природе

Углерод - один из самых известных и широко распространенных элементов в природе. Его химический символ - C, а атомный номер - 6. Углерод является необходимым компонентом жизни на Земле, так как он образует основу органических веществ, включая все живые организмы.
Одна из самых известных форм углерода - алмазы. Алмазы обладают твердостью, прочностью и блеском, что делает их ценными для ювелирных изделий. Однако алмазы представляют лишь небольшую часть всего углерода на Земле, в основном углерод находится в другой форме - графите.
Графит - это мягкий и проводящий электричество материал. Он широко используется в качестве графитового сланца в карандашах и в промышленности для производства электродов и смазок. Графит также служит основным компонентом в изготовлении графитовых стержней, используемых в ядерных реакторах и электролизе алюминия.
Углерод также находится в органической форме, например, в углеводородах, жирах, белках и ДНК. Углеродные соединения являются основой всех живых организмов и играют важную роль в метаболических процессах, энергетическом обмене и структуре клеток.
Благодаря своей уникальной способности образовывать разнообразные связи с другими атомами, углерод играет ключевую роль в химических реакциях и органической химии. Он может образовывать длинные цепочки, кольца и трехмерные структуры, такие как графен, который является одним из самых прочных и тонких материалов, известных человечеству.
Железо - базовый строительный блок для многих металлов
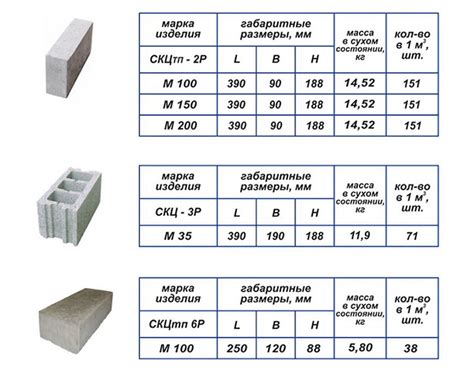
Железо – химический элемент из группы металлов, который играет важную роль во многих аспектах человеческой жизни. Оно является базовым строительным блоком для множества других металлов.
Железо находит применение в различных отраслях промышленности, таких как строительство, автомобильная промышленность, электротехника и многие другие. Одно из наиболее широко используемых железных сплавов – сталь, которая состоит из железа и углерода. Сталь обладает высокой прочностью, устойчивостью к коррозии и хорошей пластичностью, что делает ее незаменимым материалом для создания различных конструкций.
Кроме того, железо играет важную роль в процессе кроветворения. Железо содержится в гемоглобине красных кровяных клеток и ответственно за перенос кислорода из легких в организм. Недостаток железа может привести к различным заболеваниям, связанным с нарушением кроветворения.
Одним из наиболее распространенных металлических соединений железа является оксид железа, который обладает свойством окрашивать ряд природных объектов, включая почву и камни. Этот процесс можно наблюдать, например, при ржавлении железных изделий.
Медь - неизменный компонент в электротехнике

Медь - один из самых популярных и неизменных материалов, используемых в электротехнике. Ее электронная формула, записываемая как Cu, обуславливает ее уникальные электрические свойства.
Электропроводность меди является одним из самых высоких среди всех металлов. Благодаря этому, медные провода и кабели широко используются для передачи электроэнергии и сигналов в различных электрических системах. В энергетике, медные провода служат для подачи электричества от источника к потребителю с минимальными потерями энергии.
Теплопроводность меди также является высокой, что делает ее отличным материалом для радиаторов и теплообменников. Медные радиаторы эффективно отводят тепло от нагретых приборов, предотвращая их перегрев и повышение температуры в помещении.
Устойчивость к окислению меди является еще одной причиной ее широкого использования в электротехнике. Поверхностные оксиды на меди имеют способность образовывать устойчивую пленку, которая защищает металл от дальнейшего окисления. Это позволяет меди сохранять свою электропроводность на протяжении длительного времени.
Кроме того, медь является мигрирующими и формообразующим материалом, что позволяет легко изготавливать провода, пайки и различные электроотводящие и соединительные элементы. Благодаря этим свойствам, медь широко применяется в изготовлении различных электронных компонентов и устройств.
Алюминий - легкий и прочный материал для многих применений

Алюминий - это металл с атомным номером 13 в периодической системе элементов. Он имеет химическую формулу Al и относится к группе щелочноземельных металлов.
Одной из основных причин популярности алюминия является его легкость. Вес единицы объема алюминия примерно в три раза меньше, чем у стали. Это делает его идеальным материалом для применений, где вес имеет значение, например, в авиационной и автомобильной промышленности.
Но, несмотря на свою легкость, алюминий также обладает высокой прочностью. Это позволяет использовать его в строительстве зданий, мостов, а также в производстве различных инженерных конструкций.
Одной из уникальных особенностей алюминия является его способность реагировать с кислородом воздуха и образовывать тонкую пленку оксида на поверхности. Эта пленка является еще одним фактором, который делает алюминий таким популярным материалом - она обеспечивает ему защиту от коррозии и повышает его долговечность.
Алюминий также обладает хорошей теплопроводностью и электропроводностью. Это делает его востребованным материалом для изготовления радиаторов, проводов и электронных устройств.
В заключение, алюминий - это универсальный материал, который сочетает в себе легкость, прочность и химическую стойкость. Благодаря своим уникальным свойствам, он находит широкое применение во многих отраслях промышленности и строительства.
Свинец - химический элемент с высокой плотностью

Свинец является химическим элементом с атомным номером 82 и символом Pb (от латинского слова "plumbum"). Он принадлежит к группе 14 периодической системы элементов и является одним из наиболее тяжелых металлов. Свинец имеет высокую плотность, которая составляет около 11 г/см³. Такая высокая плотность делает его полезным для различных промышленных и научных приложений.
Свинец был известен человечеству еще с древних времен и широко использовался в различных сферах жизни. До нашего времени свинец нашел применение в производстве аккумуляторов, покрытий для электронных компонентов, косметических продуктах и пулях. Кроме того, свинец используется в производстве свинцовых кабелей, керосина и сурьмы, а также в оловянных сплавах.
Однако в последние десятилетия свинец стал объектом общественной озабоченности из-за своей токсичности. Великое внимание было уделено исследованиям последствий воздействия свинца на здоровье человека и окружающую среду. Негативный эффект свинца на организм включает повреждение нервной системы, печени, почек и костей. В связи с этим были введены строгие нормы по содержанию свинца в воде, пищевых продуктах и других материалах.
Свинец также используется в научных исследованиях, например, в качестве источника рентгеновского излучения для рентгеновских аппаратов и генераторов микроволновых волн. Его стабильные изотопы имеют применение при определении возраста различных объектов, например, в археологии и геологии.
Никель - необходимый элемент для прочных и коррозионностойких сплавов

Никель - один из наиболее важных металлов, используемых в производстве прочных и коррозионностойких сплавов. Он обладает рядом уникальных свойств, которые делают его необходимым компонентом во многих отраслях промышленности и науке.
Прочность и стойкость к коррозии - главные преимущества никеля. Он способен выдерживать высокие температуры, агрессивные среды и механическое напряжение без потери своих свойств. Это делает никель идеальным материалом для производства различных компонентов, используемых в аэрокосмической и энергетической промышленности, химической и пищевой промышленности.
На основе никеля создаются разнообразные сплавы, которые обладают высокой прочностью и коррозионной стойкостью. Они применяются для производства криогенных оборудований, химических реакторов, зажимов для буровых штанг, воздушных компрессоров, а также для создания покрытий и пленок, предотвращающих коррозию истирающихся поверхностей.
Никель широко используется в различных отраслях промышленности и науке, таких как авиационная и космическая промышленность, нефтегазовая отрасль, медицина и электроника. Его свойства и применение делают его одним из наиболее ценных металлов для современных технологий и производства высокотехнологичных изделий.
Цинк - защитник от коррозии

Цинк является одним из наиболее эффективных материалов для защиты от коррозии. Этот металл широко применяется в различных отраслях, таких как строительство, автомобильная промышленность, производство электроники и др. Основным свойством цинка, позволяющим ему служить защитным покрытием, является его способность к анодной защите.
Цинк имеет электронную формулу [Ar]3d104s2, что означает, что у него есть два электрона в наружной оболочке. Эти электроны легко отделяются и могут передаваться на частицы вещества, с которым взаимодействует цинк. Таким образом, цинк выступает в качестве анода, покрывая собой более реактивные металлы и защищая их от окисления.
Одним из примеров применения цинка как защитного покрытия является процесс гальванизации. При гальванизации металлическую поверхность покрывают тонким слоем цинка, который создает защитный барьер между металлом и агрессивной средой. Этот метод применяется для защиты деталей автомобилей от коррозии и увеличения их срока службы.
Цинк также широко используется в производстве цинковых покрытий, которые наносят на металлические изделия. Эти покрытия создают прочный и долговечный барьер, защищающий металл от воздействия окружающей среды. Кроме того, цинковые покрытия способны самоисправляться при повреждении, что обеспечивает дополнительную защиту от коррозии.
В целом, цинк является незаменимым материалом для защиты металлических изделий от коррозии. Его способность к анодной защите и высокая стойкость к различным агрессивным средам делают его очень популярным в различных отраслях промышленности.
Титан - металл с высокой прочностью и низкой плотностью

Титан - один из наиболее характерных металлов, имеющих электронную формулу. Этот химический элемент обладает множеством уникальных свойств, которые делают его очень ценным и востребованным в различных отраслях промышленности и науке.
Основное преимущество титана - это его высокая прочность при одновременно низкой плотности. Это означает, что титановые конструкции могут выдерживать большие нагрузки при относительно малом весе. Поэтому титан широко используется в авиационной и космической промышленности, где важно максимально снижать массу летательных аппаратов.
Кроме того, титан обладает отличной коррозионной стойкостью, что делает его незаменимым материалом для создания судов и оборудования, работающих в агрессивных средах, особенно соленой воде. Титановые сплавы отлично справляются с длительным воздействием высоких температур и экстремальных условий.
Титан также проявляет отличные биологические свойства, так как он не вызывает аллергических реакций и хорошо срастается с тканями организма. Поэтому титановые имплантаты активно применяются в медицине для создания зубных коронок, искусственных суставов и других медицинских протезов.
Вопрос-ответ

Какую электронную формулу имеет наиболее типичный металл?
Наиболее типичный металл имеет электронную формулу, в которой валентная оболочка содержит от одного до трех электронов. Например, у железа (Fe) валентная оболочка содержит два электрона, а у меди (Cu) - один электрон.
Как определить типичный металл по его электронной формуле?
Типичный металл можно определить по электронной формуле, в которой валентная оболочка содержит от одного до трех электронов. Это значит, что он имеет потенциал отдать эти электроны и образовать положительные ионы. Например, железо (Fe) и медь (Cu) - типичные металлы, так как их электронные формулы такие.
Какие металлы имеют электронную формулу с одним электроном в валентной оболочке?
Металлы, у которых электронная формула содержит один электрон в валентной оболочке, включают медь (Cu), серебро (Ag) и золото (Au). Эти металлы относятся к самым распространенным и известным металлам. Они обладают высокой электропроводностью и хорошей теплопроводностью.
Какие металлы имеют электронную формулу с двумя электронами в валентной оболочке?
Некоторые металлы, у которых электронная формула содержит два электрона в валентной оболочке, включают железо (Fe), никель (Ni) и цинк (Zn). Эти металлы являются важными компонентами различных материалов и используются в широком спектре промышленных процессов.
