Металлы - это один из основных классов химических элементов, обладающих высокой электропроводностью, блистательной поверхностью и способностью образовывать сплавы. Металлы можно разделить на несколько групп в зависимости от их химических и физических свойств.
Первая группа металлов - щелочные металлы, включает в себя литий (Li), натрий (Na), калий (K) и другие элементы. Они характеризуются высокой реакционностью с водой и кислородом, ростом активности в ходе серии и низкой плотностью. Щелочные металлы широко используются в различных областях: от производства щелочных батарей до синтеза химических соединений.
Вторая группа металлов - щелочно-земельные металлы, включает в себя бериллий (Be), магний (Mg), кальций (Ca) и другие. Щелочно-земельные металлы обладают высокой плотностью, но более низкой реакционностью, чем щелочные металлы. Они широко применяются в строительстве, авиации и других отраслях.
Третья группа металлов - переходные металлы, включает в себя железо (Fe), медь (Cu), цинк (Zn) и другие элементы. Переходные металлы характеризуются высокой прочностью, хорошей проводимостью тепла и электричества, а также способностью образовывать разнообразные сплавы. Они находят широкое применение в промышленности, электронике и строительстве.
Таким образом, группы металлов имеют свои особенности и предназначение в различных сферах человеческой деятельности. Изучение их свойств и классификации позволяет более эффективно использовать их в различных приложениях.
Обзор групп металлов
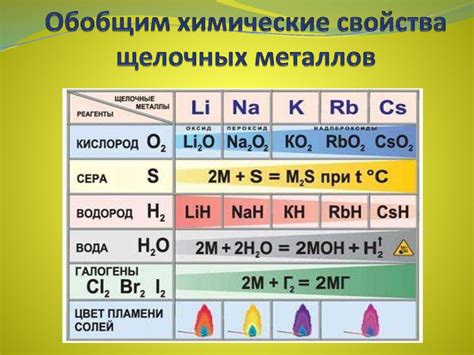
Металлы - это группа химических элементов, обладающих определенными физическими и химическими свойствами. В зависимости от своих характеристик, металлы можно разделить на несколько групп.
Первая группа металлов – щелочные металлы, к ним относятся литий, натрий, калий, рубидий, цезий и франций. Щелочные металлы обладают высокой химической активностью и сильным целыйанидным эффектом. Они реагируют с водой, образуя щелочь и высвобождая гидроген. Они хорошо проводят электричество и тепло, и обычно имеют низкую плотность.
Вторая группа металлов – щелочноземельные металлы, к которым относятся бериллий, магний, кальций, стронций, барий и радий. Щелочноземельные металлы обладают высоким плавлением и плотностью. Они также хорошо проводят электричество и тепло, и, в отличие от щелочных металлов, не реагируют с водой.
Третья группа металлов – переходные металлы, к которым относятся такие элементы, как железо, никель, медь, цинк и многие другие. Переходные металлы обладают высокой механической прочностью и устойчивостью к коррозии. Они являются хорошими проводниками тепла и электричества и находят широкое применение в разнообразных отраслях промышленности.
Четвертая группа металлов – легкие и тяжелые металлы, к которым относятся алюминий, магний, свинец, ртуть и другие. Легкие металлы обладают низкой плотностью, хорошей пластичностью и химической инертностью. Тяжелые металлы, напротив, обладают высокой плотностью и прочностью, но могут быть токсичными и окружающей среды.
Пятая группа металлов – лантаноиды и актиноиды. Лантаноиды, такие как лантан, церий и празеодим, используются в производстве катализаторов и электродов, а актиноиды, например, уран и плутоний, имеют ядерные свойства и используются в ядерной энергетике и промышленности.
Изучение групп металлов позволяет более полно понять их особенности и разнообразные применения в промышленности и науке. Каждая группа металлов имеет свои уникальные свойства и применение, что делает их незаменимыми в различных областях жизни человека.
Первая группа металлов: щелочные металлы
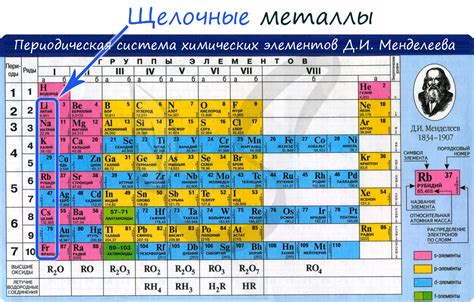
Щелочные металлы являются одной из групп металлов, которые располагаются в периодической таблице химических элементов. Эта группа состоит из лития (Li), натрия (Na), калия (K), рубидия (Rb), цезия (Cs) и франция (Fr). Щелочные металлы получили свое название из-за свойства образования гидроксидов, которые обладают щелочной реакцией.
Одной из особенностей щелочных металлов является их высокая химическая реактивность. Они активно взаимодействуют с водой и воздухом, что делает их очень реактивными элементами. Щелочные металлы имеют низкую плотность, низкую температуру плавления и кипения, а также низкую твердость.
Щелочные металлы являются отличными проводниками электричества и тепла. Они обладают высокой электроотрицательностью и образуют ионы с одиночным положительным зарядом. Эти металлы широко используются в различных областях, включая производство батареек, взрывчатых веществ, стекла и сплавов.
- Литий (Li) - легкий металл, используемый в производстве электродов, лекарств и аккумуляторов.
- Натрий (Na) - широко распространенный элемент, используется для приготовления пищи и производства щелочей.
- Калий (K) - важный элемент для растений, используется в удобрениях и производстве стекла.
- Рубидий (Rb) - используется в научных исследованиях и в производстве фоточувствительных устройств.
- Цезий (Cs) - одно из самых реактивных металлов, используется в научных исследованиях и в производстве оптического оборудования.
- Франций (Fr) - очень редкий и радиоактивный элемент, используется только в научных исследованиях.
Вторая группа металлов: щелочноземельные металлы

Щелочноземельные металлы – это элементы второй группы периодической системы элементов, которые включают бериллий (Be), магний (Mg), кальций (Ca), стронций (Sr), барий (Ba) и радий (Ra). Они получили свое название благодаря своей способности образовывать оксиды со щелочными свойствами.
Щелочноземельные металлы обладают рядом общих особенностей. Они имеют металлический блеск, высокую теплопроводность и электропроводность. В основном они образуют ионные соединения, обладающие высокой степенью пучности, что делает эти металлы хорошими вторичными источниками засветки.
Каждый из щелочноземельных металлов имеет свои уникальные свойства. Например, бериллий является легким и прочным, обладает высокой теплостойкостью и хорошей коррозионной устойчивостью. Магний обладает низкой плотностью и хорошей прочностью. Кальций является важным элементом для развития и поддержания здоровых костей и зубов. Стронций, барий и радий имеют меньшую практическую значимость, но все же находят применение в различных областях науки и промышленности.
Щелочноземельные металлы широко используются в различных отраслях, включая металлургию, строительство, химическую промышленность, электронику и многие другие. Они также играют важную роль в биологии, где выполняют ряд важных функций, таких как поддержание физиологического баланса и стабильность клеточных мембран.
Третья группа металлов: переходные металлы
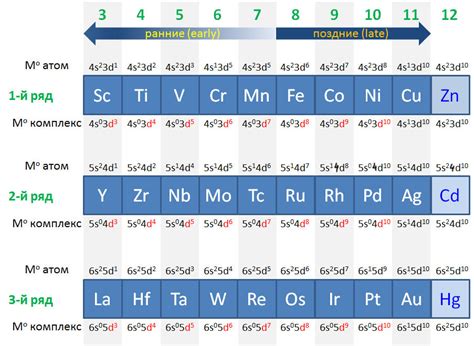
Переходные металлы - это элементы, расположенные в третьей группе периодической системы и характеризующиеся наличием нескольких энергетических уровней. Они обладают специфической структурой электронных оболочек и обобщенной формулой электронной конфигурации.
В то время как первые две группы периодической системы представлены металлами, обладающими одним энергетическим уровнем, третья группа переходных металлов содержит элементы, у которых есть возможность образования комплексных соединений. Это обусловлено наличием дополнительных d-электронов в электронной оболочке.
Переходные металлы обладают рядом химических и физических свойств, в том числе высокой термической и электрической проводимостью, способностью к образованию сплавов и сложных соединений. Их присутствие в природе и их использование в различных сферах человеческой деятельности делает их высокоценными элементами.
Некоторые известные переходные металлы включают железо, медь, никель, цинк, кобальт и другие. Они широко используются в промышленности, строительстве, электронике и других отраслях народного хозяйства. Их уникальные свойства позволяют им выполнять различные функции, от производства стали до создания электронных устройств и катализаторов.
Четвертая группа металлов: легкоплавкие металлы

Четвертая группа металлов включает в себя легкоплавкие металлы, которые обладают низкой температурой плавления и гибкостью. Они имеют мягкую текстуру и хорошую проводимость тепла и электричества. Все металлы этой группы находятся на левой стороне периодической таблицы.
Известными примерами легкоплавких металлов из четвертой группы являются олово (Sn) и свинец (Pb). Олово имеет температуру плавления около 232 градусов Цельсия, а свинец плавится при температуре около 327 градусов Цельсия.
Легкоплавкие металлы четвертой группы широко используются в различных отраслях промышленности. Например, олово применяется в производстве припоев, а свинец используется для изготовления труб и аккумуляторов.
Одной из основных особенностей легкоплавких металлов является их способность к амальгамированию. Они легко соединяются с другими металлами, что делает их полезными в различных процессах и применениях.
Пятая группа металлов: редкоземельные металлы

Пятая группа металлов в периодической системе элементов включает в себя редкоземельные металлы. Редкоземельные металлы - это группа элементов, которые обладают схожими химическими свойствами. Они включают 15 элементов, начиная с лантана (57-й элемент) и заканчивая лютецием (71-й элемент), а также скандием (21-й элемент) и иттербием (70-й элемент).
Редкоземельные металлы имеют уникальные свойства, которые делают их важными для множества промышленных процессов. Они обладают высокими плотностью, тугоплавкостью и твердостью, а также способностью образовывать стойкие соединения с другими элементами. Кроме того, редкоземельные металлы обладают специфическими магнитными и оптическими свойствами, что позволяет использовать их в производстве магнитов, лазеров и других устройств.
Редкоземельные металлы находят применение во многих отраслях промышленности. Например, они используются в производстве электроники, катализаторов, магнитов, сплавов и стекол. Также, редкоземельные металлы играют важную роль в производстве чистой энергии, так как они используются в производстве солнечных батарей и ветряных турбин.
Из-за своей высокой стоимости и ограниченного количества месторождений редкоземельные металлы являются ценными ресурсами. Их добыча и переработка являются сложными процессами, которые требуют специального оборудования и технологий. Поэтому, разработка альтернативных методов добычи и переработки редкоземельных металлов является актуальной проблемой современной науки и инженерии.
- Лантан (La)
- Церий (Ce)
- Празеодим (Pr)
- Неодим (Nd)
- Прометий (Pm)
- Самарий (Sm)
- Европий (Eu)
- Гадолиний (Gd)
- Тербий (Tb)
- Диспрозий (Dy)
- Гольмий (Ho)
- Эрбий (Er)
- Тулий (Tm)
- Иттербий (Yb)
- Лютеций (Lu)
Вопрос-ответ

Какие группы металлов можно выделить по их классификации?
По классификации можно выделить следующие группы металлов: щелочные металлы, щелочноземельные металлы, переходные металлы, лантаноиды, актиноиды, постпереходные металлы и полупроводниковые металлы.
Какие особенности характеризуют щелочные металлы?
Щелочные металлы характеризуются низкой плотностью, низкой температурой плавления и кипения, мягкостью и химической активностью.
В чем особенности переходных металлов?
Особенности переходных металлов включают высокую плотность, тугоплавкость и твердость, а также способность образовывать соединения с разными степенями окисления.
Какие свойства отличают актиноиды от лантаноидов?
Актиноиды отличаются от лантаноидов большей изменчивостью химических свойств и более высокими энергиями электронов на внешних энергетических уровнях.
