Молярная масса сульфата двухвалентного металла является важной характеристикой в химии. Сульфаты двухвалентных металлов широко представлены в природе и играют значительную роль в различных химических и технических процессах. Расчет молярной массы сульфата двухвалентного металла является необходимым для изучения и понимания его свойств и реакционной способности.
Молярная масса определяется суммой атомных масс атомов, составляющих молекулу сульфата двухвалентного металла. Сульфат состоит из атомов серы, кислорода и металла. Сера и кислород имеют постоянную атомную массу, которая взята из периодической системы химических элементов. Металл может иметь разную атомную массу в зависимости от своего типа.
Для расчета молярной массы сульфата двухвалентного металла необходимо узнать атомные массы серы, кислорода и металла, а также их количество в молекуле сульфата. Зная эти данные, можно определить молярную массу сульфата двухвалентного металла, что позволит более полно и точно описывать его свойства и использовать в соответствующих химических процессах.
Что такое молярная масса?

Молярная масса – это физическая величина, которая определяет массу одного молярного количества вещества. Молярная масса измеряется в граммах на моль (г/моль) и является средней массой атомов или молекул вещества.
Молярная масса позволяет сравнивать массу различных веществ и определять их количество в реакционной смеси. Чтобы рассчитать молярную массу, необходимо знать атомные или молекулярные массы каждого элемента, входящего в состав вещества, и их стехиометрические коэффициенты.
Расчет молярной массы особенно важен в химических реакциях, где необходимо определить количество реагентов и продуктов. Зная молярную массу вещества, можно рассчитать количество вещества по его массе или массу по количеству вещества.
Молярная масса также имеет важное значение при проведении экспериментов и измерений в химической лаборатории. Она позволяет переводить единицы измерения массы в единицы количества вещества и обратно, что упрощает проведение химических расчетов и анализов.
Зачем нужно рассчитывать молярную массу?

Расчет молярной массы является важной операцией в химических исследованиях и применяется в различных областях, таких как фармацевтика, пищевая промышленность, аналитическая химия и другие. Молярная масса, выраженная в г/моль, позволяет определить количество вещества в определенном объеме или массе.
Расчет молярной массы помогает установить точные пропорции элементов в соединениях и определить их химический состав. Это особенно полезно при синтезе новых веществ или при изучении реакций.
Также молярная масса позволяет определить объем газа, исходя из его массы, посредством использования уравнений состояния и закона Гей-Люссака. Это важно при проведении экспериментов по газовой хроматографии или оценке эффективности реакций с участием газовых веществ.
Кроме того, молярная масса может быть использована для рассчета концентрации растворов или смесей, так как позволяет определить количество вещества в единице объема или массе растворителя. Это особенно полезно при разработке новых лекарственных препаратов или контроле качества продукции в пищевой промышленности.
В целом, расчет молярной массы является фундаментальным инструментом в химических исследованиях, который позволяет установить точные пропорции и свойства веществ, облегчает синтез и анализ соединений, а также помогает в разработке новых технологий и продуктов.
Сульфат двухвалентного металла

Сульфат - это единственное сульфурное соединение, которое легко растворяется в воде и образует кристаллические структуры. Он является солью, образованной из иона двухвалентного металла и аниона сульфата.
Два заряда двухвалентного металла в сульфате компенсируются четырьмя зарядами аниона сульфата, что делает его электрически нейтральным соединением. Сульфаты двухвалентных металлов имеют важное применение в различных областях, включая химическую промышленность, лекарственную промышленность и сельское хозяйство.
Одной из ключевых задач при работе с сульфатами двухвалентных металлов является расчет их молярной массы. Молярная масса сульфата двухвалентного металла определяется суммой масс двухвалентного металла и массы аниона сульфата.
Для выполнения расчетов обычно используют периодическую таблицу элементов и соответствующие химические формулы. Найдя массы каждого атома, входящего в состав сульфата двухвалентного металла, можно определить общую массу соединения и вычислить его молярную массу.
Что такое сульфат двухвалентного металла?

Сульфат двухвалентного металла - это химическое соединение, состоящее из ионов двухвалентного металла и сульфатного иона. Сульфатный ион образуется при окислении атомов серы, а двухвалентный металл может быть различным, например, медь (Cu), цинк (Zn), железо (Fe) и другие.
Сульфат двухвалентного металла является распространенным компонентом многих химических веществ и соединений. Он используется в различных отраслях промышленности, а также в лабораториях для проведения химических исследований и анализов.
Сульфат двухвалентного металла обладает определенными физическими и химическими свойствами. Например, его растворимость в воде может варьироваться в зависимости от типа металла и условий эксперимента. Также сульфат двухвалентного металла может образовывать кристаллические соединения, которые имеют свои уникальные свойства и структуру.
Расчет молярной массы сульфата двухвалентного металла является одним из важных аспектов в химии. Для этого необходимо знать массу самого металла и его количественное соотношение с атомами серы и кислорода в сульфатном ионе. Результат расчета молярной массы позволяет получить информацию о количестве вещества в данном соединении и применять ее для различных химических расчетов и определений.
Какие металлы могут образовывать сульфат двухвалентного металла?

Сульфаты двухвалентных металлов образуются из соединений металлов, которые могут образовывать двухвалентные ионы. Такие металлы имеют два положительных иона в своем ионном состоянии и способны образовывать стабильные соединения с серной кислотой, образуя сульфаты.
Список металлов, которые могут образовывать сульфаты двухвалентных металлов, достаточно обширен. В него входят такие металлы, как железо, медь, цинк, никель, марганец, медь, кобальт и др. Эти металлы обладают свойством образовывать двухвалентные ионы в химических реакциях и способны соединяться с серной кислотой.
Сульфаты двухвалентных металлов находят применение в различных отраслях промышленности. Например, сульфат цинка используется в производстве удобрений, в гальванических процессах и в медицине. Сульфат меди применяется в производстве фунгицидов, пигментов и в медицинских препаратах. Сульфат железа широко используется в качестве добавки для лечения анемии и в производстве синтетического пигмента.
Образование сульфатов двухвалентных металлов является одним из важных химических процессов, применяемых в различных сферах деятельности человека. Изучение свойств и применение сульфатов двухвалентных металлов помогает развивать и улучшать различные технологии и процессы, а также способствует развитию науки и медицины.
Формула молярной массы
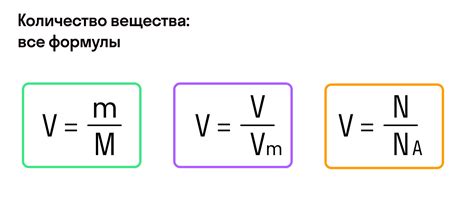
Молярная масса химического вещества представляет собой массу одного моля этого вещества. Для расчета молярной массы сульфата двухвалентного металла необходимо учесть массы всех его атомов.
Формула расчета молярной массы состоит из следующих шагов:
- Найти атомную массу каждого элемента, входящего в состав сульфата двухвалентного металла. Для этого можно воспользоваться периодической системой химических элементов.
- Узнать количество атомов каждого элемента в формуле сульфата двухвалентного металла. Для этого нужно обратиться к химической формуле вещества.
- Умножить массу каждого элемента на его количество атомов в формуле.
- Сложить полученные значения масс и получить молярную массу сульфата двухвалентного металла, выраженную в г/моль.
Приведем пример расчета молярной массы сульфата двухвалентного металла, где источником служит серебро (Ag):
- Атомная масса серебра (Ag) составляет 107.87 г/моль.
- Формула сульфата серебра (Ag2SO4) указывает, что в ней присутствует 2 атома серебра.
- Умножим массу серебра на его количество атомов в формуле: 107.87 г/моль * 2 = 215.74 г/моль.
Таким образом, молярная масса сульфата двухвалентного металла, состоящего из серебра, равна 215.74 г/моль.
Как рассчитать молярную массу сульфата двухвалентного металла?

Молярная масса сульфата двухвалентного металла является важным параметром при проведении химических расчетов. Для ее определения необходимо знать атомные массы каждого элемента, входящего в сульфат, а также их количества. Сульфат двухвалентного металла состоит из одного атома металла и четырех атомов кислорода, связанных с атомом металла. Для расчета молярной массы следует учитывать атомные массы всех элементов и их стехиометрические коэффициенты.
Первым шагом при расчете молярной массы сульфата двухвалентного металла является определение атомных масс каждого элемента, входящего в состав сульфата. Для этого необходимо воспользоваться периодической системой элементов или другим надежным источником информации. Например, атомная масса серы (S) составляет около 32 г/моль, атомная масса кислорода (O) равна примерно 16 г/моль, а атомная масса металла может быть разной в зависимости от выбранного вещества.
Следующим шагом является определение количества атомов каждого элемента в молекуле сульфата двухвалентного металла. Эта информация обычно содержится в химической формуле вещества. Например, в формуле CuSO4 имеется 1 атом металла меди (Cu), 1 атом серы (S) и 4 атома кислорода (O).
После определения атомных масс и количества атомов каждого элемента можно приступить к расчету молярной массы сульфата двухвалентного металла. Для этого необходимо умножить атомные массы каждого элемента на их стехиометрические коэффициенты и сложить результаты.
Например, для расчета молярной массы сульфата меди (CuSO4) можно использовать следующую формулу:
- Атомная масса меди (Cu) = 63.55 г/моль
- Атомная масса серы (S) = 32.06 г/моль
- Атомная масса кислорода (O) = 16.00 г/моль
Количество атомов каждого элемента:
- 1 атом меди (Cu)
- 1 атом серы (S)
- 4 атома кислорода (O)
Молярная масса сульфата меди (CuSO4) будет равна:
(63.55 г/моль × 1) + (32.06 г/моль × 1) + (16.00 г/моль × 4) = 159.61 г/моль
Таким образом, молярная масса сульфата меди составляет 159.61 г/моль.
Аналогичным образом можно рассчитать молярную массу сульфатов других двухвалентных металлов, учитывая их атомные массы и стехиометрические коэффициенты.
Примеры расчета молярной массы сульфата двухвалентного металла

Для расчета молярной массы сульфата двухвалентного металла необходимо знать атомные массы всех элементов, входящих в соединение. Например, для расчета молярной массы сульфата кальция (CaSO4) нужно знать атомные массы кальция (Ca), серы (S) и кислорода (O).
Молярная масса кальция (Ca) равна примерно 40 г/моль, серы (S) - примерно 32 г/моль, а кислорода (O) - примерно 16 г/моль. Таким образом, для расчета молярной массы сульфата кальция можно использовать следующую формулу:
Молярная масса CaSO4 = Молярная масса Ca + Молярная масса S + 4 * Молярная масса O
Подставив значения атомных масс в формулу, получим:
Молярная масса CaSO4 = 40 г/моль + 32 г/моль + 4 * 16 г/моль = 136 г/моль
Таким образом, молярная масса сульфата кальция равна 136 г/моль.
Аналогичным образом можно расчитать молярную массу сульфатов других двухвалентных металлов, заменяя атомные массы элементов в соответствующей формуле. Например, для сульфата цинка (ZnSO4) молярная масса будет вычисляться по формуле:
Молярная масса ZnSO4 = Молярная масса Zn + Молярная масса S + 4 * Молярная масса O
И так далее для остальных сульфатов двухвалентных металлов.
Пример расчета молярной массы сульфата двухвалентного металла

Молярная масса сульфата двухвалентного металла рассчитывается на основе массовых долей элементов в соединении. Для проведения расчета необходимо знать атомные массы всех элементов, входящих в молекулу сульфата двухвалентного металла.
Например, для расчета молярной массы сульфата кальция (CaSO4) необходимо знать атомные массы кальция (Ca), серы (S) и кислорода (O). Кальций имеет атомную массу 40, сера - 32, а кислород - 16.
Далее, нужно установить количественное соотношение между элементами в молекуле сульфата кальция. В данном случае, молекула сульфата кальция содержит один атом кальция, один атом серы и четыре атома кислорода. Соответственно, массовая доля кальция в молекуле равна 40/136, массовая доля серы - 32/136, а массовая доля кислорода - 4*16/136.
Для расчета молярной массы сульфата кальция можно использовать следующую формулу: молярная масса = (массовая доля кальция * атомная масса кальция) + (массовая доля серы * атомная масса серы) + (массовая доля кислорода * атомная масса кислорода).
Подставив значения массовых долей и атомных масс в формулу, получаем молярную массу сульфата кальция - около 136 г/моль.
Таким образом, для расчета молярной массы сульфата двухвалентного металла необходимо знать атомные массы всех элементов в соединении и их количественное соотношение в молекуле. С помощью формулы можно вычислить молярную массу и получить ее числовое значение в г/моль.
Вопрос-ответ

Как рассчитать молярную массу сульфата двухвалентного металла?
Молярная масса сульфата двухвалентного металла может быть рассчитана путем сложения атомных масс всех элементов в молекуле сульфата. Для этого необходимо узнать атомные массы серы, кислорода и металла, который является двухвалентным. Затем умножьте атомные массы каждого элемента на их количество в молекуле сульфата и сложите полученные значения. Полученная сумма будет молярной массой сульфата двухвалентного металла.
Можно ли использовать молярную массу сульфата двухвалентного металла для расчета массы сульфата в заданном количестве вещества?
Да, молярную массу сульфата двухвалентного металла можно использовать для расчета массы сульфата в заданном количестве вещества. Для этого вам необходимо знать количество молей сульфата и умножить его на молярную массу сульфата двухвалентного металла. Таким образом, вы получите массу сульфата в заданном количестве вещества.
Какая молярная масса у сульфата двухвалентного металла?
Молярная масса сульфата двухвалентного металла зависит от самого металла. Конкретное значение можно рассчитать путем сложения атомных масс серы, кислорода и металла в молекуле сульфата. Таким образом, молярная масса может быть различной в зависимости от металла, который используется в сульфате. Например, для сульфата цинка (ZnSO4) молярная масса будет равна примерно 161 г/моль.
