Металлы являются одним из основных классов материалов, обладающих широким спектром применения в индустрии и научных исследованиях. Их уникальные свойства, такие как высокая тепло- и электропроводность, прочность и пластичность, связаны с их молекулярно структурным строением.
Молекулярно структурное строение металлов состоит из регулярной решетки атомов, образующих кристаллическую структуру. Кристаллическая решетка металлов характеризуется наличием свободных электронов в атомах, что придает им особые физические свойства.
Одним из важных аспектов молекулярно структурного строения металлов является их кристаллическая геометрия. Она определяется симметричным расположением атомов в кристаллической решетке. Различные металлы имеют разные типы кристаллической геометрии, такие как кубическая, гексагональная или тетрагональная структуры.
Молекулярно структурное строение металлов также оказывает влияние на их физические и механические свойства, такие как плавление, пластичность, тугоплавкость и твердость. Изменение молекулярной структуры металлов может привести к изменению их свойств, что имеет важное значение для разработки новых материалов с определенными характеристиками.
Определение и основные понятия
Металлы - это класс веществ, характеризующихся своими уникальными физическими и химическими свойствами. Основные характеристики металлов - высокая термическая и электрическая проводимость, блеск, пластичность и деформируемость.
Металлическое строение представляет собой сетку идеально сферических атомов, в которой ячейки кристаллической решетки соприкасаются друг с другом по граням, ребрам и вершинам. Такая атомная решетка образуется за счет взаимодействия электронов валентной зоны с положительно заряженными атомными ядрами.
Молекулярное строение металлов является одной из основных характеристик металлических материалов. Оно определяет их физические и химические свойства, а также влияет на их механическую прочность, упругость и пластичность.
Основными компонентами молекулярной структуры металлов являются кристаллическая решетка и атомарный размер. Кристаллическая решетка металла может быть простой, в виде кубической или гексагональной решетки, или сложной, в виде сплава из нескольких металлов.
Атомарный размер металла определяет размер его атомов в кристаллической решетке и влияет на его механические свойства. Большой атомарный размер обеспечивает металлу высокую деформируемость и пластичность, в то время как маленький размер делает его хрупким и жестким.
Кристаллическая решетка металлов
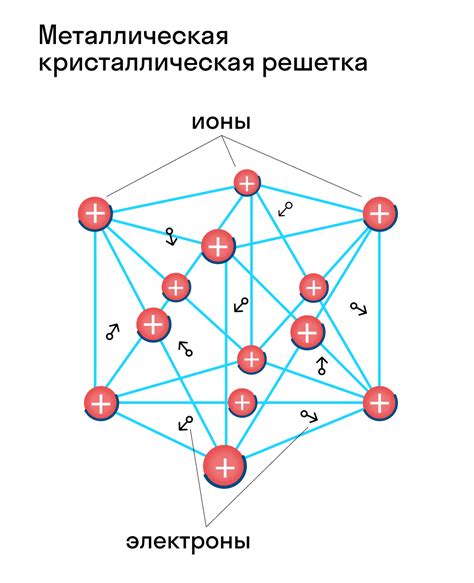
Металлы обладают кристаллической структурой, основой которой является кристаллическая решетка. Кристаллическая решетка металлов представляет собой трехмерную упаковку атомов, образующую устойчивую и регулярную сетку.
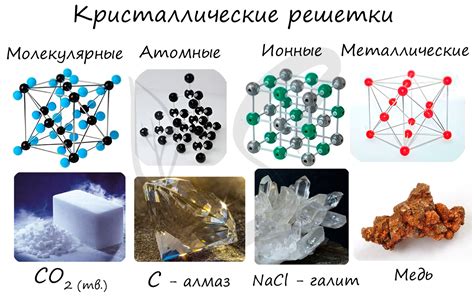
В зависимости от типа взаимодействия атомов и структуры кристаллической решетки, металлы классифицируются на различные типы структур, такие как гранецентрированная кубическая решетка (ГЦК), простая кубическая решетка (ПКР) и гексагональная ближнепакетная решетка (ГБР).
ГЦК решетка характеризуется пространственной укладкой атомов, при которой атомы находятся в узлах кубической решетки, а также находятся в центре каждой грани куба. ПКР решетка представляет собой прямой куб со сторонами, вдоль которых расположены атомы. ГБР решетка имеет шестиугольные сечения, а атомы располагаются в шестиугольных пакетах.
Структура кристаллической решетки металла определяет его физические и химические свойства, такие как механическая прочность, электропроводность и теплопроводность. Понимание кристаллической решетки металлов является важной составляющей при изучении и использовании металлических материалов в различных отраслях промышленности и науки.
Межмолекулярные взаимодействия в металлах
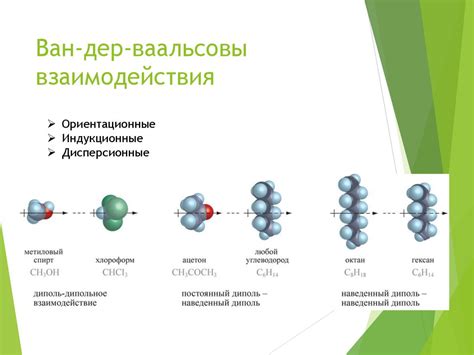
Межмолекулярные взаимодействия в металлах играют важную роль в их структуре и свойствах. Один из основных типов таких взаимодействий - межчастичные взаимодействия между атомами металла. Эти взаимодействия определяют стабильность кристаллической решетки и ее механические свойства.
В металлах также присутствуют межатомные взаимодействия, которые проявляются через обмен электронами между атомами. Это взаимодействие способствует скрещиванию атомных орбиталей и образованию так называемых металлических связей. Эти связи играют важную роль в электропроводности и теплопроводности металлов.
Однако в металлах также наблюдаются межмолекулярные взаимодействия более слабых типов. Например, молекулярные структуры в металлах могут быть связаны межмолекулярными взаимодействиями водородной связи. Эти взаимодействия способствуют образованию сложных молекулярных структур и могут влиять на их физические свойства.
В целом, межмолекулярные взаимодействия в металлах определяют их структурные особенности и свойства. Понимание этих взаимодействий помогает разрабатывать новые материалы с желаемыми свойствами и улучшать уже существующие металлические структуры.
Связь между строением и свойствами металлов
Металлы - это материалы с характерным строением и свойствами, связанными с этим строением. Структура металлов состоит из металлической решетки, где положительно заряженные ионы металла окружены облаком свободно движущихся электронов. Именно связь между строением и свойствами металлов определяет их уникальные характеристики и широкое применение в различных отраслях промышленности.
С помощью различных методов исследования, таких как рентгеноструктурный анализ и электронная микроскопия, ученые изучают трехмерную структуру металлов. Отличительной особенностью металлической решетки является регулярное расположение кристаллических зерен и скоплений атомов, которые формируют положительно заряженные ионы. Электроны, перемещающиеся внутри решетки, связаны с положительно заряженными ядрами и слабо взаимодействуют с другими электронами, что обусловливает характерные свойства металлов, такие как высокая теплопроводность и электропроводность.
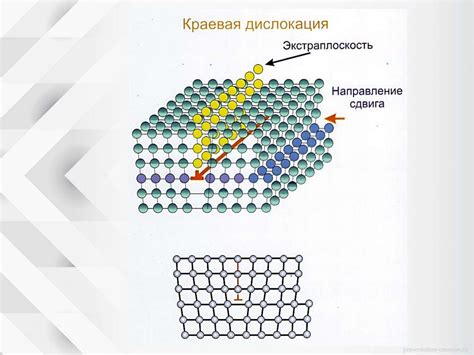
Строение металлов также оказывает влияние на их механические свойства, такие как прочность, пластичность и твердость. Границы зерен и дислокации внутри структуры металла играют роль в механизме деформации и влияют на его механическую прочность. Если границы зерен не регулярные и в материале присутствуют дислокации, то металл будет обладать высокой пластичностью. Однако, если границы зерен находятся близко друг к другу и отсутствуют дислокации, то металл будет более твердым и хрупким.
Некоторые свойства металлов также определяются их структурой на более микроскопическом уровне. Например, магнитные свойства металлов связаны с порядком ориентации магнитных моментов атомов внутри решетки, а светопропускание - с электронными переходами между энергетическими уровнями внутри металлической структуры.
Металлическая связь как основа молекулярного строения

Металлическая связь является ключевым аспектом молекулярного строения металлов. Она обусловлена специфическим взаимодействием электронов в кристаллической решетке металла. Основной особенностью металлической связи является наличие общих электронов, которые могут свободно двигаться по всей структуре металла. Эти электроны образуют так называемое "море электронов", которое окружает положительные ионы металла.
Металлическая связь является очень сильной и обеспечивает прочность металлических материалов. Прочность металлов обусловлена возможностью электронов свободно двигаться внутри структуры металла. Это позволяет металлам выдерживать большие давления и деформации без разрушения. Электроны образуют сильные связи с положительными ионами металла, обеспечивая стабильность и прочность структуры.
Металлическая связь также обуславливает хорошую электропроводность и теплопроводность металлов. Подвижность электронов позволяет им легко переносить электрический ток и тепло. Благодаря этому свойству металлы являются отличными проводниками и используются во многих электрических и электронных устройствах.
Выводы:
- Металлическая связь основана на наличии общих электронов, формирующих "море электронов".
- Металлическая связь обеспечивает прочность и устойчивость структуры металлов.
- Металлы обладают хорошей электропроводностью и теплопроводностью благодаря подвижности электронов.
Твердые растворы и сплавы металлов
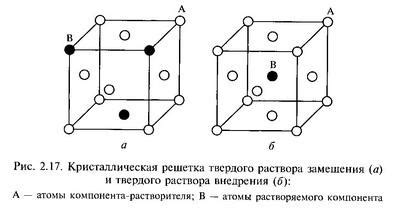
В металловедении твердые растворы и сплавы металлов представляют собой особый тип материалов, обладающих уникальными свойствами и структурой.
Твердый раствор представляет собой смесь двух или более металлов, объединенных в монолитную структуру. Однако, в отличие от обычных растворов, в твердых растворах металлов атомы не перемещаются внутри смеси, а остаются на своих местах в кристаллической решетке. В результате этого образуется металлическая матрица с включениями атомов добавленного металла.
В сплавах металлов атомы могут быть перемешаны в решетке, образуя равномерное сочетание различных элементов. Это приводит к взаимодействию атомов разных видов и возникающим при этом эффектам, таким как утверждение материала, повышенная твердость и стойкость к коррозии.
Твердые растворы и сплавы металлов широко используются в промышленности, в частности в производстве металлических конструкций, авиационной и автомобильной промышленности, электроники и других отраслях. Они обладают уникальными механическими, физическими и термическими свойствами, которые делают их идеальными материалами для различных приложений.
Криогенные идеальные металлические решетки и их свойства
Криогенные идеальные металлические решетки – это структуры, образованные атомами металла, которые находятся в идеальном порядке при очень низких температурах, близких к абсолютному нулю. Они представляют собой важную модель для изучения базовых свойств металлов.
В идеальной металлической решетке атомы расположены в виде геометрической структуры, называемой кристаллической решеткой. Эти решетки могут иметь различные формы, такие как кубическая, гексагональная или квадратная. Структура решетки определяет множество свойств металла, включая его электрическую проводимость, механическую прочность и теплопроводность.
Одно из важных свойств криогенных идеальных металлических решеток - их низкая температура, которая близка к абсолютному нулю. Это обеспечивает уникальные возможности для изучения квантовых явлений и поведения атомов в материале. Также они обладают высокой устойчивостью к деформации и имеют очень низкие уровни тепловых и электрических сопротивлений.
Исследование криогенных идеальных металлических решеток позволяет углубить наше понимание основных принципов, лежащих в основе структуры и свойств металлов. Это имеет большое значение для разработки новых материалов с улучшенными свойствами и их применения в различных областях, включая электронику, энергетику и медицину.
Вопрос-ответ

Какова основная структура металлов?
Основная структура металлов состоит из кристаллической решетки, состоящей из атомов металла, которые образуют регулярные упорядоченные ряды.
Что такое сегнетоэлектрический эффект?
Сегнетоэлектрический эффект - это способность некоторых материалов при наличии электрического поля изменять свою форму и объем.
Какие фазы существуют у металлов?
У металлов существуют различные фазы, такие как кристаллическая, аморфная и жидкая фазы.
Как возникают примеси в металлах и как они влияют на структуру?
Примеси в металлах могут возникать как при производстве, так и в процессе использования. Они могут влиять на структуру металла, изменяя его свойства и поведение при различных условиях.
Какие методы используются для анализа структуры металлов?
Для анализа структуры металлов используются различные методы, такие как рентгеноструктурный анализ, электронная микроскопия и дифракция электронов.
