Металлы - это особый класс материалов, которые обладают высокой проводимостью электрического тока и тепла. Однако, что именно отличает металлы от других веществ? Одно из ключевых свойств металлов заключается в их кристаллической структуре, которая представляет собой упорядоченное расположение атомов в пространстве.
Металлическая кристаллическая решетка является основой для понимания многих свойств металлов. Решеткообразная структура образуется благодаря тесному упаковыванию атомов металла в пространстве, при котором они образуют регулярные и повторяющиеся паттерны.
В металлической кристаллической решетке атомы металла упакованы таким образом, что образуется трехмерная сетка, состоящая из одинаковых маленьких ячеек. Атомы металла находятся в центре каждой ячейки, а решетка продолжается во все стороны. Такое тесное упаковывание атомов обеспечивает высокую плотность, прочность и эластичность металлов.
Важно отметить, что связь между атомами металла в решетке не является ковалентной или ионной, как в случае неметаллических соединений, а является металлической связью.В металлической связи электроны внешней энергетической оболочки атомов металла перемещаются свободно и не связаны ни с каким конкретным атомом. Физическая природа такой связи объясняет многие уникальные свойства металлов, такие как их высокая проводимость тепла и электричества.
Структура металлической кристаллической решетки
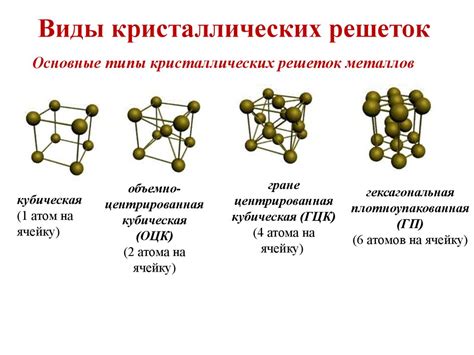
Металлическая кристаллическая решетка представляет собой структуру, в которой атомы металла упорядочены в трехмерной решетке. Эта структура обусловлена взаимодействием электронов внутри металла.
Металлическая решетка характеризуется наличием межатомных связей между соседними атомами металла. Основными характеристиками металлической решетки являются: межатомные расстояния и углы между связями.
Внутри металлической кристаллической решетки атомы металла образуют регулярные кристаллические узлы, которые повторяются в пространстве. Эти узлы образуют трехмерную сетку, которая состоит из двух типов элементарных клеток: позиции атомов и интерститиций.
Интерститции представляют собой свободные промежутки между атомами металла. Они обеспечивают свободное движение электронов в металле и являются местом пребывания дефектов решетки.
Таким образом, структура металлической кристаллической решетки представляет собой упорядоченную трехмерную сетку атомов металла, в которой присутствуют интерститции. Эта структура обусловливает многочисленные свойства металлов, такие как проводимость электрического тока и теплопроводность.
Роль электронов в связи между атомами металлов
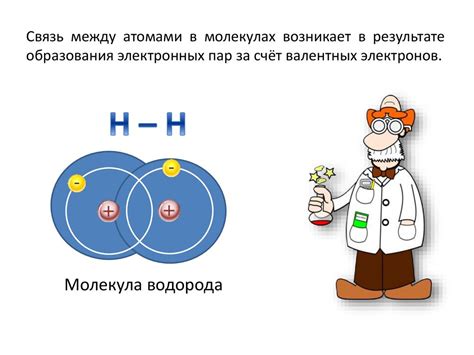
Связь между атомами металлов в кристаллической решетке осуществляется за счет взаимодействия электронов. Основную роль здесь играют так называемые "свободные" электроны, которые находятся в валентной зоне.
Эти свободные электроны обладают высокой подвижностью и могут свободно перемещаться между атомами металла. Таким образом, они образуют электронное облако, окружающее положительно заряженные атомы металла.
Именно электроны являются не только связующим звеном между атомами металла, но и ответственны за большинство характеристик металлической структуры. Они обеспечивают высокую теплопроводность и электропроводность металлов, а также их способность подвергаться пластической деформации и образованию металлического блеска.
Электроны в метальных кристаллах обладают также особенностью - они создают эффект экранирования. Это означает, что электроны между атомами металла отталкивают друг друга, устанавливая определенное расстояние между атомами и способствуя стабильности кристаллической решетки.
Таким образом, электроны играют важную роль в связи между атомами металлов, обеспечивая их структурную устойчивость и определяя множество физических свойств металлических материалов.
Пространственная организация атомов в кристаллической решетке
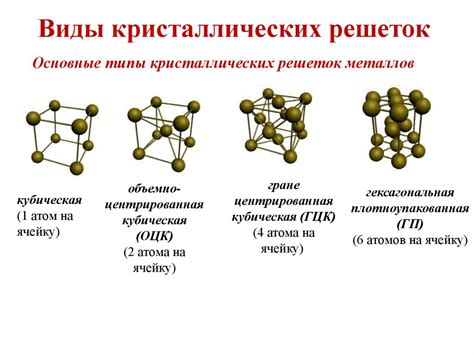
Кристаллическая решетка представляет собой особую структуру, в которой атомы металла упорядочены в пространстве. Она обладает периодическим повторением, что позволяет атомам занимать определенные позиции и образовывать сильные атомные связи между собой.
В кристаллической решетке атомы металла расположены в узлах трехмерной сетки, которая образуется периодическим повторением базиса – набора атомов, являющихся прототипом всей решетки. Каждый атом окружен шестью соседними атомами, и связи между ними обладают высокой прочностью.
Организация атомов в кристаллической решетке влияет на многие свойства металлов. Например, электрическая проводимость и теплопроводность металлов зависят от геометрического расположения атомов в решетке и их взаимодействия. Кроме того, структура кристаллической решетки определяет механические свойства металлов, такие как прочность и пластичность.
Существуют различные типы кристаллических решеток, такие как кубическая, гексагональная, квадратная и другие. Каждый тип решетки имеет свои особенности и приводит к появлению специфических свойств материалов. Например, кубическая решетка характерна для многих металлов, а гексагональная решетка обычна для некоторых металлов и полупроводников.
Ковалентная и металлическая связи между атомами

В металлической кристаллической решетке атомы металла образуют особую связь, называемую металлической связью. Она характеризуется свободным перемещением электронов между атомами, что придает металлам такие свойства, как электропроводность и теплопроводность.
Ковалентная связь, в свою очередь, характеризуется обменом электронами между атомами. Она образуется между неметаллами или металлом и неметаллом. Ковалентная связь обусловливает формирование молекулярных и ковалентных кристаллических решеток.
Отличие металлической связи от ковалентной заключается в том, что в металлической связи электроны считаются общими для всех атомов металла и могут свободно двигаться по всей решетке. В ковалентной связи каждый атом вносит свой вклад в формирование общих электронных областей, образуя пары электронов между соседними атомами молекулы или между атомами в кристаллической решетке.
Из-за различий в типе связи у атомов металлов и неметаллов металлическая решетка отличается от ковалентной решетки. В металлической решетке атомы металлов расположены в сетке, состоящей из катионов, вокруг которых находятся электроны. В ковалентной решетке атомы образуют кристаллическую структуру с общими электронами, образованными при обмене электронами между атомами.
Влияние температуры на связь между атомами металлов

Температура является одним из важнейших факторов, влияющих на связь между атомами металлов в их кристаллической решетке. При повышении температуры металлическая решетка может изменять свою структуру, что приводит к изменению свойств материала.
Связь между атомами металлов обеспечивается электрическими взаимодействиями между ионами и электронами. При низких температурах электроны занимают определенные энергетические уровни в решетке, образуя так называемую "электронную оболочку". Эта структура обеспечивает прочность и устойчивость кристаллической решетки.
Однако, при повышении температуры энергия электронов увеличивается, и они начинают переходить на более высокие энергетические уровни или покидать атомы металла. Это может приводить к нарушению связи между атомами и изменению структуры решетки.
Например, при нагреве металла до достаточно высокой температуры он может перейти из кристаллической фазы в аморфную, где связь между атомами уже не является упорядоченной и представляет собой скопление атомов случайной формы. Это может снижать прочность и устойчивость материала.
Также изменение связи между атомами металлов под воздействием высоких температур может привести к термическому расширению материала. При нагреве атомы начинают колебаться с большей амплитудой, а межатомные расстояния увеличиваются. Это может приводить к изменению геометрических размеров и формы изделий, что необходимо учитывать при проектировании и производстве металлических конструкций.
Практическое применение связи между атомами металлов в различных отраслях промышленности
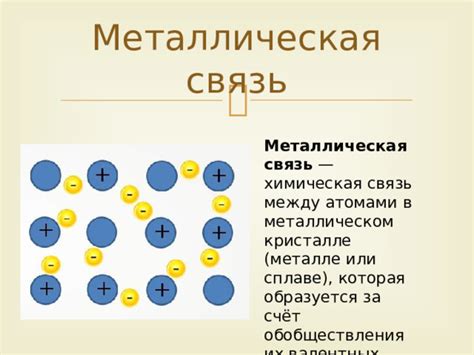
Связь между атомами металлов является основой для множества процессов и технологий, которые нашли применение в различных отраслях промышленности. Одной из таких отраслей является металлургия, где металлическая кристаллическая решетка используется для создания прочных и устойчивых металлических конструкций.
В строительстве также активно используется связь между атомами металлов. Металлические соединения широко применяются в конструкции зданий, мостов, судов и других сооружений, которые должны выдерживать большие нагрузки и обеспечивать долговечность.
Связь между атомами металлов играет важную роль и в электронике. Многие электронные компоненты, такие как проводники, транзисторы и диоды, содержат металлическую кристаллическую решетку, которая обеспечивает эффективный токопроводящий путь и стабильность работы устройства.
Не обошла связь между атомами металлов и сфера материаловедения. Металлические материалы с определенной структурой решетки обладают уникальными свойствами, такими как прочность, эластичность, теплопроводность и другие. Используя знания о связи между атомами, можно создавать материалы с необходимыми характеристиками для различных приложений.
Также следует отметить применение связи между атомами металлов в химической промышленности. Металлические соединения используются в качестве катализаторов при проведении химических реакций, что позволяет увеличить скорость реакции и повысить выход продукта. Кроме того, многие металлы и их соединения широко применяются в производстве различных химических веществ и материалов.
Таким образом, практическое применение связи между атомами металлов охватывает множество отраслей промышленности и играет важную роль в создании современных технологий и материалов.
Вопрос-ответ

Какие металлы образуют металлическую кристаллическую решетку?
Металлическую кристаллическую решетку образуют большинство металлов, таких как железо, алюминий, медь, золото и другие.
Чем отличается металлическая кристаллическая решетка от других типов решеток?
Металлическая кристаллическая решетка отличается от других типов решеток тем, что в ней атомы металлов располагаются в упорядоченной трехмерной структуре.
Как атомы металлов связаны в металлической кристаллической решетке?
Атомы металлов в металлической кристаллической решетке связаны между собой металлическими связями, при которых свободные электроны образуют общую "оболочку" и перемещаются вокруг положительно заряженных ионов металла.
Какие свойства имеет металлическая кристаллическая решетка?
Металлическая кристаллическая решетка обладает такими свойствами, как хорошая электропроводность, теплопроводность, пластичность и механическая прочность.
Какая роль у свободных электронов в металлической кристаллической решетке?
Свободные электроны в металлической кристаллической решетке играют роль "скользящей электронной жидкости", которая обеспечивает электропроводность и теплопроводность металлов.
