Электролиз - это процесс разложения вещества под влиянием электрического тока. Он широко используется в производстве металлов и является одним из наиболее эффективных методов их получения. Метод электролиза позволяет получать чистые и высококачественные металлы с высокой степенью чистоты.
Процесс электролиза основан на том, что под действием постоянного электрического тока ионные вещества разлагаются на положительно и отрицательно заряженные ионы, которые перемещаются к электродам, заряжая их. При этом на катоде относительно низкое значение степени окисления элементов, а на аноде - высокое. Таким образом, в результате электролиза на катоде металлы восстанавливаются из соединений.
Метод электролиза широко применяется в процессе получения металлов, таких как алюминий, цинк, медь и другие. Этот метод позволяет получать металлы с высокой степенью чистоты и химической активности. Кроме того, он также позволяет регулировать процесс получения металлов, что делает его универсальным и применимым в различных отраслях промышленности.
Метод электролиза в процессе получения металлов является одним из наиболее важных и эффективных способов. Он позволяет получать высококачественные металлы, обладающие необходимыми характеристиками и свойствами. Благодаря этому методу, процесс получения металлов становится более эффективным, экономичным и экологически чистым.
Применение электролиза в процессе производства металлов

Метод электролиза широко применяется в металлургии для получения различных металлов. Он основан на использовании электрического тока для разложения соединений металлов на ионы и последующего осаждения их на электродах.
Процесс электролиза проводится в электролитической ячейке, которая состоит из анода (положительно заряженного электрода) и катода (отрицательно заряженного электрода), погруженных в электролит. При подаче электрического тока происходит окисление металла на аноде и его восстановление на катоде, что позволяет извлечь чистый металл из раствора.
Преимущества электролиза в процессе производства металлов заключаются в его высокой эффективности и точности. Этот метод позволяет получать чистые металлы с высокой степенью очистки от примесей и загрязнений. Кроме того, он позволяет производить металлы с заданными характеристиками, такими как размеры, форма и прочность.
Применение электролиза возможно для получения широкого спектра металлов, включая алюминий, медь, цинк, никель, свинец и другие. Каждый металл требует своих условий процесса электролиза, таких как температура, состав электролита, плотность тока и другие параметры. Однако, в целом, электролиз является важным и эффективным способом производства металлов в промышленных масштабах.
Определение электролиза и его принцип работы
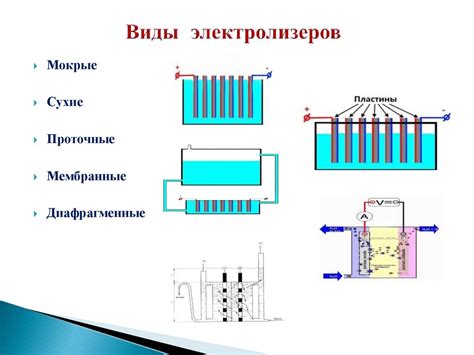
Электролиз - это химический процесс, основанный на разложении веществ под действием электрического тока. Электролиз заключается в пропускании электрического тока через электролит – вещество, способное проводить электрический ток. В результате электролиза в электролите происходит разделение вещества на ионы на положительные ионы (катионы), заряженные положительным электрическим зарядом, и отрицательные ионы (анионы), заряженные отрицательным электрическим зарядом.
Принцип работы электролиза основан на применении постоянного электрического тока. Электролит размещается в специальной емкости, в которой находятся два электрода – анод и катод. При подключении электродов к источнику электрического тока, положительно заряженный анод и отрицательно заряженный катод становятся местами, в которых происходят реакции.
Катод притягивает положительные ионы, которые выполнены отрицательно заряженный электрод, где ион погружается в раствор и получает электроны. Анод же притягивает отрицательные ионы, которые из раствора выходят в виде газа или осадка при окислении. Таким образом, на катоде проходит процесс восстановления, а на аноде – окисления.
Основные металлургические процессы, основанные на электролизе
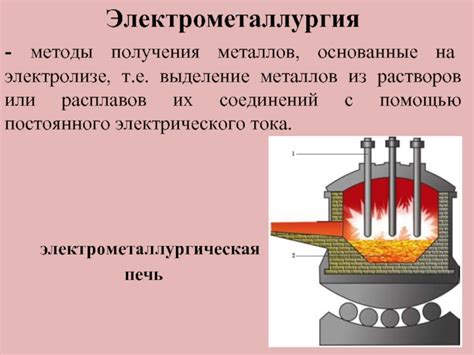
Метод электролиза широко используется в металлургической промышленности для получения различных металлов. Основными процессами, основанными на электролизе, являются процессы рафинирования, электролитического получения металлов и гальванического покрытия.
Процесс рафинирования позволяет получить высококачественные металлы, освободив их от примесей. В процессе рафинирования металла, его растворяют в электролите и пропускают через электролизер. На аноде, обычно изготовленном из металла с низкой чистотой, происходит окисление примесей, а металл оседает на катоде в виде высокочистого вещества.
Электролитическое получение металлов применяется для извлечения металлов из руд или растворов. В процессе электролиза, руда или раствор помещают в электролитическую ячейку, где они служат анодами, и проводят электрический ток через ячейку. Металлы осаждается на катоде, а нежелательные примеси остаются в растворе или оседают на аноде.
Гальваническое покрытие позволяет нанести тонкое слоевое покрытие металлов на поверхность другого материала. При этом металл, который необходимо нанести на поверхность, служит анодом, а материал, на который наносят покрытие, выступает в роли катода. Покрытие осуществляется при прохождении тока через электролитическую ячейку, где металл осаждается на поверхности катода.
Процесс электролиза в производстве цинка
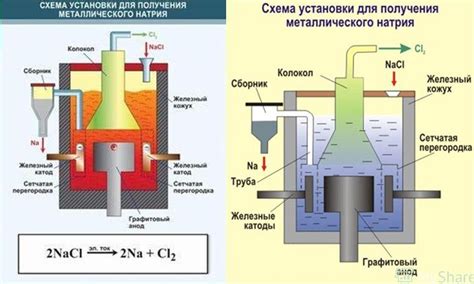
Цинк является одним из важных металлов, который широко используется в различных отраслях промышленности. Один из способов получения цинка - это метод электролиза. В процессе электролиза цинк получается из раствора, содержащего соединение цинка.
Процесс электролиза в производстве цинка проводится в специальных электролизерах. В электролизере находятся два электрода: анод и катод. Анод изготовлен из материала, не реагирующего с раствором, например, свинца. Катод обычно представляет собой лист цинкового металла. Между электродами находится электролит, содержащий раствор цинка.
При подключении электрического тока к электродам происходит процесс электролиза. На аноде происходит окисление цинка, а на катоде происходит восстановление цинка. При этом ионы цинка из раствора переносятся на катод и образуют металлический цинк. Кислород, образующийся на аноде, выводится в виде газа.
Полученный металлический цинк собирается на катоде и затем подвергается дополнительной обработке для удаления примесей. Полученный цинк может быть использован в различных отраслях промышленности, таких как производство аккумуляторов, гальваническое покрытие и производство сплавов.
Процесс электролиза в производстве алюминия
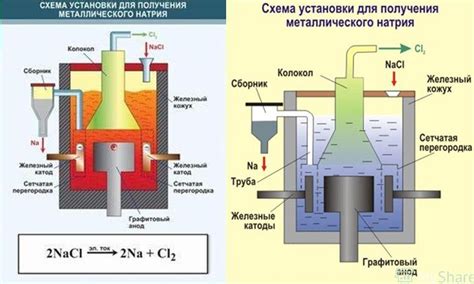
Алюминий является одним из самых распространенных металлов в мире и используется в различных отраслях промышленности. Процесс электролиза играет значительную роль в его производстве.
Процесс начинается с получения раствора алюминия, который содержит оксид алюминия в расплавленной соли – криолите. Этот раствор используется как электролит в электролизной ячейке, где происходит разложение оксида алюминия на алюминий и кислород под воздействием постоянного электрического тока.
В электролизной ячейке алюминий получается на катоде, который представляет собой графитовую пластину. Катод окружен криолитовым раствором, который выполняет функцию электролита и обеспечивает проводимость тока.
Анод в электролизной ячейке представляет собой посудину из графита с поддерживающей структурой. Под действием тока на аноде происходит окисление кислорода, который выделяется в виде газа. Анод постепенно разрушается и периодически заменяется.
Полученный в процессе электролиза алюминий собирается в специальные емкости, где охлаждается и затвердевает. Затем из него изготавливают различные изделия или он может быть использован для производства сплавов с другими металлами.
Применение электролиза в гальваническом покрытии

Гальваническое покрытие – это процесс нанесения тонкого слоя металла на поверхность изделия с целью защиты от коррозии, придания декоративности или улучшения функциональных характеристик. Один из основных методов нанесения гальванического покрытия – это электролиз.
В электролизе используется электрический ток, чтобы перенести металлические ионы из раствора на поверхность изделия. Для этого используется электролит – раствор соли металла, который разлагается под действием электрического тока. Отрицательно заряженные ионы металла перемещаются под воздействием электрического поля и осаждается в виде металлического покрытия на поверхности изделия.
Электролиз позволяет наносить тонкие и ровные слои металла на изделия различной формы и размера. Благодаря этому методу можно получить покрытия с заданными физико-механическими характеристиками, такими как твердость, износостойкость, адгезия к основе. Часто гальваническое покрытие используется для придания декоративности изделию, так как возможно нанесение покрытия различных металлов с разнообразными цветовыми оттенками.
Для эффективного применения электролиза в гальваническом покрытии необходимо учитывать ряд факторов, таких как состав электролита, температура и скорость процесса, а также электрические параметры. Контроль параметров процесса электролиза позволяет получить покрытия высокого качества с заданными характеристиками.
Электролиз в гальваническом покрытии находит широкое применение в различных областях, таких как автомобильная, электронная, медицинская, ювелирная промышленность. Он позволяет создавать не только декоративные покрытия, но и повышать функциональные свойства изделий, такие как защита от коррозии, повышение теплопроводности или электропроводности. Применение электролиза в гальваническом покрытии существенно расширяет возможности производства и повышает качество изготовляемых изделий.
Вопрос-ответ

Какой метод используется для получения металлов?
Один из методов, используемых для получения металлов, это метод электролиза.
Что такое метод электролиза?
Метод электролиза - это процесс, основанный на применении электрического тока для разложения химических соединений и получения металлов из их соединений.
Каким образом происходит электролиз металлов?
В электролизе металлов используется электролитическая ячейка, в которой размещаются два электрода: катод и анод. Под влиянием электрического тока металлы осаждается на катоде, а соединения металлов разлагаются на аноде, образуя ионы.
Какие металлы можно получить с помощью метода электролиза?
Метод электролиза позволяет получить различные металлы, включая алюминий, магний, натрий, кальций, свинец, цинк и другие. Конкретный металл зависит от соединения металла, которое используется в процессе электролиза.
