Металлы и вода - два вещества, которые встречаются в ежедневной жизни человека. Их взаимодействие имеет важное значение в различных отраслях науки и техники, поэтому важно понимать физико-химические процессы, происходящие при контакте металлов с водой.
Вода - универсальный растворитель, способный реагировать с различными веществами. Металлы, в свою очередь, обладают особенной структурой и электрохимическими свойствами, которые определяют их поведение при контакте с водой. Под действием воды металлы могут проявлять разные свойства - реактивность, коррозионную стойкость, способность образовывать соединения с водой и др.
Важный аспект взаимодействия металлов с водой - их электрохимическое поведение. Металлы могут вступать в реакцию с водой за счет своих электрохимических свойств. Некоторые металлы реагируют с водой, образуя гидроксиды и/или водород, другие - образуют соединения с водой и проявляют реакцию амфотерности. Эти процессы важны для понимания химического поведения металлов в воде и их роли в различных природных и технических системах.
Исследования взаимодействия металлов с водой позволяют не только лучше понять процессы, происходящие в природе, но и применять эти знания в различных областях - от химической промышленности до медицины и экологии. Понимание взаимодействия металлов с водой под обычными условиями имеет большое практическое значение и помогает создавать новые материалы и технологии относительно безопасными для окружающей среды.
Процесс окисления и образование оксида

Взаимодействие металлов с водой под обычными условиями часто сопровождается процессом окисления, при котором металл одновременно теряет электроны и образует оксид. Окисление является результатом химической реакции между металлом и молекулами воды.
В процессе окисления, электроны переходят с поверхности металла на атомы кислорода воды, образуя оксид металла. Это явление может происходить спонтанно или при воздействии электрического тока, а также при повышении температуры.
Образование оксида металла является важным аспектом изучения взаимодействия металлов с водой, так как оксиды металлов имеют различные свойства и могут быть использованы в разных отраслях промышленности, например, как катализаторы, абсорбенты, материалы для создания покрытий и других применений.
Окисление металлов в воде может привести к образованию различных оксидов, в зависимости от химического состава металла и условий реакции. Некоторые из наиболее распространенных оксидов, образующихся при взаимодействии металлов с водой, включают оксиды железа, оксид алюминия, оксид меди и другие.
Количество и скорость реакции

Реакция металлов с водой может происходить с разной интенсивностью и скоростью в зависимости от характеристик металлов и условий эксперимента. Количество металла, которое растворяется в воде, может быть определено как физической, так и химической методикой.
Обычно чистые щепотки металла сразу же при погружении в воду начинают реагировать и образовывать газы. В зависимости от металла, реакция может быть более или менее интенсивной. Некоторые металлы, такие как калий и натрий, реагируют очень активно, выпуская пламя и выделяя большое количество водорода. Другие металлы, например железо или цинк, реагируют менее активно и не так быстро растворяются в воде.
Скорость реакции металлов с водой может быть различной в зависимости от температуры воды, концентрации металла и других факторов. Высокая температура воды обычно способствует более активной реакции, так как повышает скорость химических реакций. Также скорость реакции может зависеть от структуры металла и наличия оксидной пленки на его поверхности.
Некоторые металлы, такие как алюминий, образуют защитную оксидную пленку на своей поверхности, которая может затруднять взаимодействие с водой. В таких случаях, реакция может начинаться медленно, но затем ускоряться после пробития оксидной пленки.
Различные виды реакций металлов с водой

Металлы могут проявлять разные виды реакций при контакте с водой. Они могут быть химически активными и реагировать с водой, выделяя газы или инициируя окислительно-восстановительные процессы.
Некоторые металлы, такие как натрий и калий, очень реактивны и сразу начинают реагировать с водой при контакте с ней. При этом образуются щелочные гидроксиды и выделяется водородный газ. Реакция с натрием или калием проходит очень быстро и с сильным выделением тепла.
Другие металлы, например, магний и цинк, медленно реагируют с водой. Они образуют гидроксиды и выделяются водородный газ, но реакция протекает медленнее и без сильного выделения энергии. Раствор гидроксида, образующийся при реакции, может быть щелочным или нейтральным.
Некоторые металлы, вроде железа и алюминия, реагируют с водой только в присутствии кислорода или менее окисленных веществ. В результате образуются оксиды металлов и водород. Реакция с железом проходит медленно, однако алюминий способен реагировать с водой достаточно быстро.
Также существуют металлы, которые не реагируют с водой вообще или реагируют очень медленно. К таким металлам относятся, например, серебро и платина.
Влияние температуры на реакцию

Температура является одним из основных факторов, влияющих на реакцию между металлами и водой. Увеличение температуры может значительно ускорить химическую реакцию, а также изменить направление и характер процесса.
При повышении температуры молекулы воды получают дополнительную энергию, что облегчает разрушение металлических связей и активирует реактивность металла. Это приводит к ускорению скорости реакции и, соответственно, более быстрому образованию продуктов реакции.
Однако, с повышением температуры могут изменяться и свойства металла. Например, при высокой температуре алюминий начинает образовывать оксидную пленку, которая защищает его поверхность от дальнейшего взаимодействия с водой. Таким образом, влияние температуры на реакцию зависит не только от характеристик металла, но и от его окружающей среды и условий эксперимента.
Механизм взаимодействия металлов с водой под высокой температурой еще не полностью изучен и возможны дополнительные факторы, влияющие на реакцию. Дальнейшие исследования в этом направлении позволят более точно определить влияние температуры на химические процессы и использовать эту информацию в различных технических и промышленных областях.
Специфика взаимодействия редких металлов с водой

Взаимодействие редких металлов с водой имеет свои особенности, которые отличают их от других металлов. Одной из таких особенностей является их высокая стабильность в контакте с водой под обычными условиями. Редкие металлы не реагируют с водой так же активно, как, например, щелочные металлы.
Вода не оказывает угнетающего влияния на редкие металлы, что делает их более долговечными в контакте с водой. Это свойство редких металлов позволяет им использоваться в различных сферах, где требуется высокая устойчивость к коррозии и другим агрессивным воздействиям порошки и компоненты, используемые в медицине, энергетике и промышленности.
Взаимодействие редких металлов с водой также имеет применение в электрохимических процессах, таких как производство водорода или электролиз воды. Редкие металлы являются эффективными и стабильными катализаторами в этих процессах, что позволяет эффективно использовать воду в производственных целях и получать энергию из возобновляемых источников.
В целом, специфика взаимодействия редких металлов с водой заключается в их высокой стабильности и низкой реактивности в контакте с жидкостью. Это свойство делает их ценными материалами для различных промышленных и научных приложений, а также способствует развитию новых технологий и исследований в области электрохимии и катализа.
Коррозия и образование пассивной пленки
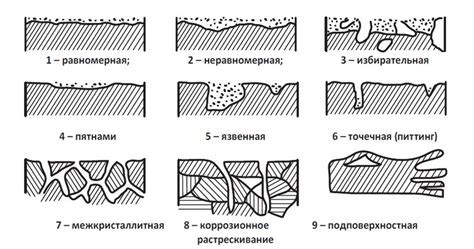
Коррозия – это процесс уничтожения металла под воздействием окружающей среды. Когда металл взаимодействует с водой, начинается коррозия, которая может привести к его разрушению. Однако некоторые металлы способны образовывать защитную пленку – пассивную пленку, которая предотвращает дальнейшую коррозию и сохраняет металл от разрушения.
Образование пассивной пленки происходит за счет химических реакций между металлом и водой. Например, алюминий образует пассивную пленку оксида алюминия, которая защищает его от коррозии. Схожим образом, нержавеющая сталь содержит хром, который образует пассивную пленку оксида хрома. Другие металлы, такие как железо, медь или цинк, не образуют такую защитную пленку и подвержены коррозии взаимодействием с водой.
Качество образующейся пассивной пленки зависит от состава металла и условий окружающей среды. Если пассивная пленка повреждается, например, в результате механического воздействия или воздействия агрессивных химических веществ, металл становится уязвимым и может продолжить корродировать. Поэтому важно учитывать условия окружающей среды и принимать меры для защиты металла от коррозии.
В целом, образование пассивной пленки является важным механизмом, позволяющим металлам сохранять свою структуру и противостоять коррозии при взаимодействии с водой. Понимание процессов образования и разрушения пассивной пленки позволяет разработать эффективные методы защиты металлов и повысить их долговечность при использовании в различных условиях.
Важность взаимодействия металлов с водой в промышленности

Взаимодействие металлов с водой имеет большое значение в промышленности. Металлы широко используются в производстве различных товаров, их свойства и качество зависят от химических реакций с водой. Кроме того, вода служит важным реагентом при процессах очистки и обработки металлов.
При взаимодействии металлов с водой происходят различные химические процессы, в результате которых могут образовываться новые соединения или изменяться свойства металла. Например, некоторые металлы могут растворяться в воде, что приводит к образованию ионов и комплексных соединений. Эти процессы могут быть использованы для получения новых материалов или для обработки уже существующих металлов.
Вода также является важным средством для очистки металлов от загрязнений. В промышленности часто используются специальные процессы очистки, включающие промывку металлических поверхностей водой. Это позволяет удалить ржавчину, грязь и другие загрязнения, повышая качество и долговечность металлических изделий.
Также вода может использоваться как охлаждающая среда при обработке металлов. Охлаждение металла помогает предотвратить его перегрев и деформацию в процессе обработки, что влияет на качество и точность изготовления металлических изделий.
Таким образом, взаимодействие металлов с водой играет важную роль в промышленности, влияя на свойства и качество металлических изделий, а также используется для их очистки и обработки. Понимание этих процессов позволяет разрабатывать более эффективные технологии и улучшать производственные процессы в промышленности.
Практическое применение знаний о взаимодействии металлов с водой
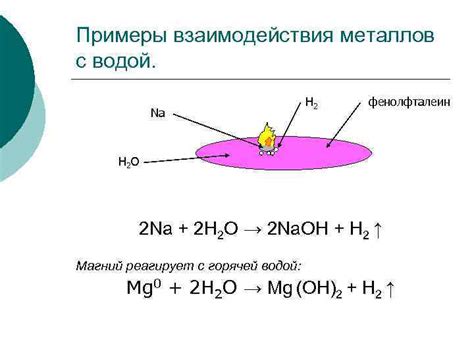
Знание о взаимодействии металлов с водой имеет практическое применение в различных областях. Одной из них является технология производства водорода. Металлы, такие как алюминий или натрий, реагируют с водой, освобождая водород. Этот процесс может быть использован для производства водорода как возобновляемого источника энергии.
Кроме того, знания о взаимодействии металлов с водой широко применяются в производстве и хранении пищевых продуктов. Некоторые металлы, такие как нержавеющая сталь и алюминий, обладают свойствами, которые делают их удобными для использования в пищевой промышленности. Они не окисляются и не реагируют с водой, что помогает сохранять свежесть и качество продуктов.
Знания о взаимодействии металлов с водой также используются в создании различных химических реакций. Металлы могут служить катализаторами для различных химических процессов, которые требуют воды. Например, некоторые металлы могут использоваться в процессе электролиза воды, который применяется для получения кислорода и водорода.
Кроме того, знание о взаимодействии металлов с водой является важным при решении проблем, связанных с коррозией. Коррозия металлов под воздействием влаги является серьезной проблемой во многих отраслях, включая строительство, автомобильную промышленность и морские перевозки. Понимание того, как металлы реагируют с водой и какие меры предосторожности необходимо принять, позволяет предотвратить и уменьшить коррозию и сохранить долговечность и надежность конструкций и изделий.
Таким образом, знание о взаимодействии металлов с водой не только интересно с научной точки зрения, но и имеет широкое применение в различных отраслях промышленности и научных исследованиях. Оно способствует разработке новых технологий, повышению эффективности производства и решению практических проблем, связанных с водой и металлами.
Вопрос-ответ

Какие металлы реагируют с водой?
Реакция металлов с водой зависит от их активности. Например, очень активные металлы, такие как натрий и калий, реагируют с водой очень быстро и взрывоопасно. Некоторые другие металлы, такие как железо и цинк, реагируют с водой медленнее, но все равно могут образовывать гидроксиды и выделяться водород. Тем не менее, некоторые металлы, такие как свинец или платина, не реагируют с водой под обычными условиями.
Каковы последствия реакции металлов с водой?
Последствия реакции металлов с водой могут быть различными. Если металл очень активный, то взаимодействие с водой может быть взрывоопасным. В этом случае образуется металлический гидроксид и выделяется водород, который может воспламениться при взаимодействии с воздухом. Если металл менее активный, то он может образовывать гидроксид и выделяться водород, но взрывного реагирования не происходит. Кроме того, реакция некоторых металлов с водой может приводить к образованию оксидов или других соединений.
