Металлы – это группа химических элементов, которые обладают множеством уникальных свойств и широким применением в различных областях науки и промышленности. Один из важных аспектов химического поведения металлов заключается в их способности образовывать соединения с другими элементами, при этом каждый металл имеет определенную степень окисления.
Степень окисления – это электрический заряд, который принадлежит атому данного элемента в химическом соединении. У металлов степень окисления обычно положительная, так как они имеют тенденцию отдавать электроны другим элементам. Однако степень окисления металла может варьироваться в зависимости от условий реакции и химического окружения.
Знание степени окисления металла является фундаментальным принципом в химии и играет важную роль при проведении химических реакций. Оно позволяет определить количество электронов, которые обмениваются между атомами в процессе реакции и помогает установить химическую формулу соединения. Кроме того, знание степени окисления позволяет предсказывать свойства и поведение соединений и помогает в изучении реакций окисления и восстановления.
Понимание степени окисления металлов является неотъемлемой частью химического образования и играет ключевую роль в практическом применении металлов в различных отраслях науки и промышленности. Знание степени окисления металлов позволяет предсказывать и контролировать их взаимодействие с другими веществами и создавать новые материалы с уникальными свойствами.
Металлы в химии: важное понятие степени окисления
Степень окисления – это числовое значение, которое указывает на потенциал электронного переноса в химической реакции. Для металлов, которые играют важную роль в химии, понятие степени окисления имеет особое значение.
Металлы могут иметь несколько вариантов степени окисления, которые зависят от конкретных условий и окружающих их атомов или молекул. Наличие различных вариантов степени окисления позволяет металлам проявлять разнообразные химические свойства и участвовать в различных реакциях.
Знание степени окисления металлов является основой для понимания и предсказания химической активности и реакционной способности металлов. Например, степень окисления может использоваться для определения, какие соединения металла могут быть стабильными в определенной среде.
Для металлов, степень окисления обычно указывается с помощью римских цифр или знаков "+" или "-", что позволяет определить количество электронов, которые переходят от металла к другим атомам или молекулам. Например, у железа может быть степень окисления II (Fe2+), что означает, что оно передало два электрона, или степень окисления III (Fe3+), что означает передачу трех электронов.
Изучение степени окисления металлов позволяет углубить наше понимание их роли в химических реакциях и применении в различных областях, таких как катализ и электрохимия. Это важное понятие позволяет нам контролировать и оптимизировать свойства металлов для создания новых материалов и технологий.
Понятие степени окисления в химии

Степень окисления в химии является одним из ключевых понятий, которое позволяет определить степень окисления или восстановления атома в химическом соединении. Она указывает на число электронов, которые атом может получить или отдать при формировании связей с другими атомами. Степень окисления является важным фактором, определяющим химические свойства и реакционную способность атома.
Степень окисления обозначается числом с положительным или отрицательным знаком. Положительная степень окисления указывает на потерю электронов атомом, а отрицательная – на приобретение электронов атомом. Например, в водороде (H2) степень окисления атома равна нулю, так как он не обменивает электронами с другими атомами.
Для определения степени окисления атома необходимо учесть его электроотрицательность и количество связей, а также количество электронов, которые входят в образование связи. Степень окисления атома может быть определена на основе электронного формализма, такого как правила определения степени окисления, установленные Методом слева направо и Методом по направлению электрона наибольшей вероятности.
Значение степени окисления для металлов

Степень окисления – это числовое значение, которое показывает, сколько электронов металл отдал или принял при образовании химической связи. У металлов степень окисления может быть положительной или отрицательной величиной в соответствии с тем, сколько электронов они отдают или принимают. Она играет важную роль в химических реакциях и определяет химические свойства металлов.
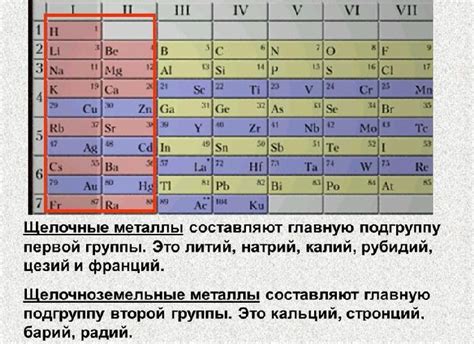
Степень окисления металлов в соединениях может быть различной и зависит от их положения в периодической системе. Некоторые металлы, такие как щелочные и щелочноземельные металлы, обычно обладают положительной степенью окисления, так как они склонны отдавать электроны и образовывать катионы. Например, натрий, обладающий степенью окисления +1, отдает один электрон при образовании Na+.
В то же время, некоторые металлы могут иметь различные степени окисления. Например, железо может иметь степень окисления +2 или +3 в своих соединениях. Это связано с тем, что железо может отдавать два или три электрона, что зависит от условий реакции.
Знание степени окисления металлов позволяет предсказывать и анализировать их реакционную способность и взаимодействие с другими веществами. Оно также играет важную роль в определении окислителей и восстановителей в химических реакциях, а также в рациональном выборе условий проведения реакций и синтеза новых соединений.
Физические свойства металлов и их взаимосвязь со степенью окисления

Металлы, как класс химических элементов, обладают определенными физическими свойствами, которые влияют на их взаимосвязь со степенью окисления. Во-первых, металлы обладают высокой электропроводностью. Это значит, что они способны передавать электрический ток, что является особенно важным свойством для многих промышленных и технических приложений.
Кроме того, металлы обладают высокой теплопроводностью. Это свойство позволяет им эффективно передавать тепло, что делает их полезными для использования в различных системах охлаждения и обогрева. Высокая теплопроводность также влияет на процессы окисления металлов, поскольку они могут быстро поглощать или отдавать тепло, что может влиять на скорость и интенсивность окисления.
Кроме электропроводности и теплопроводности, металлы обладают достаточно высокой плотностью и твердостью. Эти физические свойства могут влиять на процессы окисления, так как металлы могут быть более или менее устойчивы к нападению окислителей в зависимости от их структурной прочности и плотности.
В связи с этим, степень окисления металла может варьироваться в зависимости от его физических свойств. Например, металлы с высокой электропроводностью и теплопроводностью могут иметь более низкую степень окисления, так как они могут быстро удалять образующиеся окисные слои и предотвращать дальнейшее окисление. С другой стороны, металлы с более низкой плотностью и твердостью могут быть более подвержены окислению, так как окислительные вещества могут легче проникать в их структуру и вызывать окислительные реакции.
Таким образом, физические свойства металлов играют важную роль в их взаимосвязи со степенью окисления. Понимание влияния этих свойств может помочь в разработке более эффективных методов предотвращения окисления металлов, что может быть полезно во многих областях, включая промышленность, энергетику и электронику.
Способы определения степени окисления металлов

Существует несколько способов определения степени окисления металлов в химических соединениях. Один из них основан на знании общей схемы электронного строения металлов и их ионов. В соответствии с этой схемой, металлы в элементарном состоянии имеют степень окисления 0. Если металл находится в ионном состоянии, его степень окисления соответствует заряду иона.
Другой способ определения степени окисления металлов основан на правиле о сохранении общего заряда соединения. Согласно этому правилу, сумма степеней окисления всех элементов в химическом соединении равна нулю или равна заряду соединения. При определении степени окисления металлов в соединении, можно использовать информацию о степени окисления других элементов и общем заряде соединения.
Также для определения степени окисления металлов можно использовать таблицы степеней окисления. В этих таблицах указывается максимальная и минимальная степень окисления металла в различных соединениях. При анализе соединения, можно определить степень окисления металла, сопоставив его с указанными значениями. Это позволяет быстро и удобно определить степень окисления металла без необходимости проведения подробных вычислений или анализа электронной структуры.
Структура и классификация окислов металлов
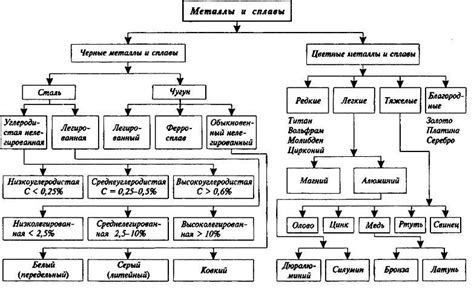
Окислы металлов представляют собой соединения металлов с кислородом, в которых кислород играет роль отрицательного ионного радикала. Они имеют сложную структуру и могут быть представлены как простыми, так и сложными соединениями.
Классификация окислов металлов основывается на степени окисления металла и его химических свойствах. Существует несколько видов окислов металлов, таких как металлические окислы, супероксиды, оксиды металлов с переменной степенью окисления и др.
Металлические окислы представляют собой соединения, в которых металл имеет фиксированную степень окисления. Такие окислы в основном являются неактивными химическими веществами, не способными к реакциям с другими веществами.
Супероксиды – это окислы, в которых степень окисления металла равна -1/2. Это достигается благодаря наличию кислорода с двойной связью. Супероксиды имеют высокую реакционную активность и способны к реакциям с кислородом и другими веществами.
Оксиды металлов с переменной степенью окисления представляют собой окислы, в которых металл может иметь разные степени окисления. Это связано с наличием различных ионов металла в соединении. Такие окислы являются активными химическими веществами и могут проводить реакции с различными веществами.
Классификация окислов металлов является важной составляющей изучения химических свойств и реакций металлов. Знание о структуре и классификации окислов металлов позволяет более точно предсказывать и объяснять их химическую активность и взаимодействия с другими веществами.
Роль степени окисления в реакциях металлов

Степень окисления - важный показатель, определяющий химические свойства и реактивность металлов. Она позволяет определить, сколько электронов металл отдал или принял во время реакций.
При окислительно-восстановительных реакциях, металлы могут изменять свою степень окисления, позволяя им использовать электроны для получения энергии или передачи ее в реакцию. Металлы с положительной степенью окисления, такие как натрий или алюминий, имеют склонность отдавать электроны, что позволяет им выступать в качестве восстановителей. Металлы с отрицательной степенью окисления, такие как кислород или хлор, имеют склонность принимать электроны и действовать в качестве окислителей.
Знание степени окисления металла позволяет ученому прогнозировать его поведение в химических реакциях. На основе степени окисления можно предсказать, какой ион металла будет образовываться при растворении металла в растворе или при взаимодействии с другими веществами.
Степень окисления металла также играет важную роль в практическом применении металлов. Например, степень окисления используется для определения активности металлов в анодной и катодной сторонах электрохимических элементов, таких как батареи и аккумуляторы. Это помогает ученым разрабатывать эффективные и надежные источники энергии.
Применение степени окисления в различных областях химии
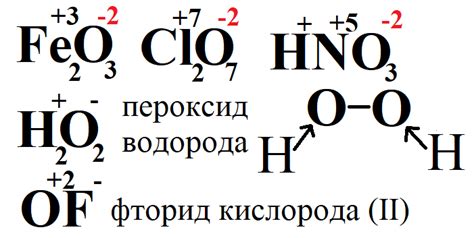
Степень окисления играет ключевую роль в различных областях химии, позволяя определить, какой электронный потенциал имеет атом или ион, и какие возможности у него есть для образования химических связей.
В аналитической химии степень окисления помогает идентифицировать и качественно анализировать различные вещества. Она может быть определена с использованием реактивов, специально разработанных для реагирования с определенными степенями окисления. Это позволяет определить наличие или отсутствие определенных групп функциональных групп в органических соединениях или наличие определенных ионов в растворе.
В органической химии степень окисления играет важную роль в реакционах окисления и восстановления. Степень окисления атомов углерода и других элементов в органических соединениях может изменяться в результате различных реакций, и знание степени окисления атомов позволяет предсказать и объяснить химические свойства и реакции органических веществ.
В неорганической химии степень окисления используется для классификации металлических элементов. Она позволяет определить их химическую активность и способность образовывать соединения с определенными степенями окисления. Например, металлы с положительной степенью окисления обычно образуют ионы с этой же степенью окисления, в то время как металлы с отрицательной степенью окисления образуют ионы с положительной степенью окисления.
В химической термодинамике степень окисления используется для рассчета энергетического эффекта реакций окисления и восстановления. Знание степени окисления атомов позволяет определить изменение энергии связи при реакции и предсказать, будет ли реакция экзотермической или эндотермической.
Таким образом, степень окисления играет важную роль во многих областях химии, позволяя определить свойства и реактивность веществ, классифицировать элементы и предсказывать энергетические эффекты реакций. Без понимания степени окисления невозможно полное понимание химической реакции и ее механизма.
Вопрос-ответ

Можете объяснить, что такое степень окисления металлов?
Степень окисления металлов - это числовое значение, которое указывает на количество электронов, переданных металлом во время химической реакции. Она позволяет определить, какие ионы металла будут образовываться в процессе реакции.
Зачем нужно знать степень окисления металла?
Знание степени окисления металла позволяет предсказать его реактивность и способность образовывать соединения с другими веществами. Это особенно важно в химии, где степень окисления металла может влиять на его способность к каталитическим реакциям, электропроводности и другим свойствам.
Как можно определить степень окисления металла в соединении?
Для определения степени окисления металла в соединении необходимо использовать набор правил, основанных на фундаментальных принципах. Например, степень окисления вещества обычно определяется их электроотрицательностью - чем меньше электроотрицательность металла, тем выше его степень окисления. Также степень окисления металла может зависеть от типа связей, которые он образует в соединении.
