Металлы – особый класс химических элементов, имеющих высокую электропроводность и способность формировать положительные ионы. Изучение металлов является одним из важных аспектов химии и является неотъемлемой частью ЕГЭ по химии. Понимание основных понятий и свойств металлов позволит успешно справиться с заданиями экзамена и достичь высокого результат.
Основные свойства металлов включают их металлический блеск, электропроводность и теплопроводность, хорошую пластичность и деформируемость. Металлы обладают большой реакционной способностью и могут вступать в химические реакции с другими веществами. Изучение реакций металлов и их окисление и восстановление является важным компонентом подготовки к экзамену по химии.
Важными понятиями в теории металлов являются атомные и ионные радиусы, электроотрицательность и степень окисления. Знание этих понятий позволяет объяснить свойства и восстановительные способности металлов, а также их реакции с кислотами и основаниями. Анализ и классификация металлов по их свойствам позволяет установить закономерности в их химическом поведении и прогнозировать результаты химических реакций.
Все о металлах в химии на ЕГЭ: подготовка к экзамену

Металлы - это широкий класс химических элементов, которые обладают хорошей проводимостью электрического тока и тепла, а также отличаются типичными физическими и химическими свойствами. Изучение свойств металлов является важной частью программы ЕГЭ по химии. Понимание основных характеристик металлов поможет успешно справиться с экзаменом.
Металлы обладают множеством уникальных свойств. Одно из главных отличий металлов от других элементов - это их способность образовывать положительные ионы (катионы) и отдавать электроны. Именно поэтому металлы хорошие проводники электрического тока.
Кроме того, металлы обладают высокой теплопроводностью, что позволяет им эффективно распространять тепло. Как правило, металлы обладают блеском, который называется металлическим блеском, и способностью деформироваться безразрушительно - пластичностью. Эти свойства позволяют использовать металлы для создания различных конструкций и изделий.
В таблице химических элементов металлы расположены слева от ступеньки, которая выделяет металлы от неметаллов. Время от времени на ЕГЭ задают вопросы, связанные с размещением элементов в таблице Менделеева. Запомните, что автоматически записывать элементы слева от ступеньки в раздел «Металлы» легко и удобно!
Еще одним важным аспектом изучения металлов является их распространение в природе и способы добычи. Важно знать, что некоторые металлы встречаются в природе в чистом виде, такие металлы называются нативными. Отдельные металлы могут быть получены из руд - минералов, содержащих определенные соединения металлов. Руды делят на сульфидные, оксидные, гидроксидные и другие, и способ обогащения руд и извлечения металла зависит от их типа и свойств.
Таким образом, изучение свойств металлов является важным аспектом подготовки к экзамену по химии. Знание основных характеристик металлов, их расположение в таблице Менделеева, а также способы добычи металлов из руд поможет успешно справиться с экзаменом и получить высокий балл.
Определение металлов в химии

Металлы - это химические элементы, обладающие определенными свойствами. Они характеризуются высокой теплопроводностью и электропроводностью, а также способностью блескать, многие из них являются твердыми и имеют высокую плотность. В химии металлы обычно располагают слева в периодической системе элементов.
Для определения металлов в химии используются различные признаки. Одним из них является химическая реакция с водой: большинство металлов реагирует с водой, образуя гидроксиды и выделяя водород. Например, натрий реагирует с водой по следующему уравнению: 2Na + 2H₂O → 2NaOH + H₂.
Другим способом определения металлов является их способность образовывать ионы положительной заряды. В химии металлы обычно образуют катионы, отдавая электроны. Ионы металлов, как правило, обладают положительной зарядом и имеют стабильную электронную конфигурацию. Например, катион железа Fe²⁺.
Также металлы могут образовывать соли с кислотами. Образование соли сопровождается обменом ионов, при котором катионы металла замещают водородный ион в кислоте. Например, образование соли соляной кислоты: HCl + Na → NaCl + H₂.
Строение металлов и их свойства
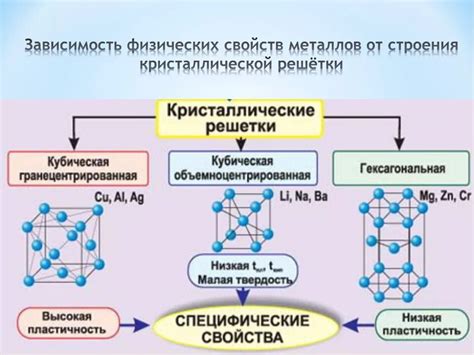
Строение металлов: Металлы имеют кристаллическую структуру, что означает, что их атомы упорядочены в решетке. Основными элементами кристаллической решетки металлов являются положительно заряженные ионы металла, которые окружены облаком электронов. Электроны в металлической решетке могут свободно двигаться, что обуславливает основные свойства металлов.
Свойства металлов: Металлы обладают несколькими характерными свойствами. Во-первых, металлы обладают высокой теплопроводностью и электропроводностью благодаря свободным электронам в их структуре. Это свойство делает металлы хорошими проводниками тепла и электричества. Во-вторых, металлы обладают высокой пластичностью и деформируемостью, что позволяет им легко поддаваться обработке и созданию различных форм. В-третьих, металлы обладают высокой прочностью и твердостью, что делает их подходящими для использования в конструкционных материалах.
Металлическая связь: Свободные электроны в металлической решетке образуют так называемую металлическую связь. Металлическая связь обуславливает высокую пластичность и деформируемость металлов, так как свободные электроны могут перемещаться в решетке, что позволяет металлам легко менять свою форму без разрыва связей. Также металлическая связь обуславливает высокую теплопроводность и электропроводность металлов, так как свободные электроны могут переносить энергию и электрический заряд.
Использование металлов: Металлы широко используются в различных отраслях промышленности и повседневной жизни. Они применяются в строительстве для создания каркасов зданий, в производстве машин и автотранспорта, в электронике для создания проводов и контактов, а также в производстве различных изделий, таких как посуда, оружие, украшения и т.д. Благодаря своим свойствам, металлы являются неотъемлемой частью современной жизни человека.
Химические реакции с металлами
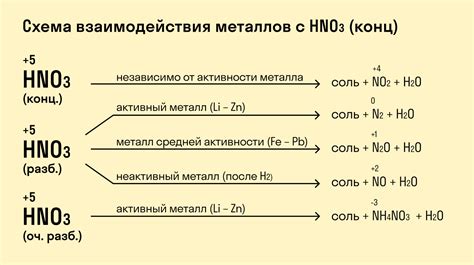
Металлы обладают способностью вступать в различные химические реакции, что делает их важными объектами изучения в химии. Химические реакции с металлами могут быть различными: окислительно-восстановительными, реакциями с кислотами или плавлениями.
В окислительно-восстановительных реакциях металлы могут выступать в качестве веществ, окисляющихся (восстанавливающихся). Например, металлы активной серии, такие как калий, натрий или магний, могут взаимодействовать с кислородом из воздуха, образуя оксиды металлов.
Металлы также могут реагировать с кислотами, образуя соли и выделяя водород. Например, реакция цинка с соляной кислотой приводит к получению хлорида цинка и выделению водорода.
Некоторые металлы имеют низкую температуру плавления и могут реагировать с нагреванием. Например, при нагревании меди и серебра они плавятся и реагируют с кислородом из воздуха, образуя соответствующие оксиды.
Химические реакции с металлами имеют важное практическое значение и находят применение в различных отраслях, таких как металлургия, электротехника, химическая промышленность и многие другие.
Коррозия металлов и способы защиты

Коррозия металлов является естественным процессом разрушения металлических материалов под воздействием окружающей среды. В условиях высокой влажности, наличия кислорода и других агрессивных веществ, металлы подвергаются окислению, что приводит к потере их механических и химических свойств.
Существует несколько способов защиты металлов от коррозии. Одним из них является использование покрытий, которые создают защитную преграду между металлом и окружающей средой. Например, цинковое покрытие может быть нанесено на стальной изделия методом гальванизации. Защитная пленка из цинка не только предотвращает контакт металла с агрессивными веществами, но и является самостоятельным анодом, что позволяет ему жертвовать собой в процессе коррозии и защищать основной металл.
Другим способом защиты от коррозии является использование антикоррозионных покрытий. Они создают тонкую прочную пленку на поверхности металла, которая предотвращает контакт с окружающей средой. Эти покрытия могут быть нанесены методом нанесения клеящих оснований, гальванического осаждения или покрытием на основе полимерных материалов.
Дополнительным способом защиты от коррозии являются методы электрохимической защиты. Они основаны на использовании разности потенциалов между металлами. Например, аноды из специальных металлов могут быть помещены рядом с металлическими конструкциями, такими как трубы или корпуса кораблей, и подключены к ним. Аноды будут жертвовать собой в процессе коррозии, тем самым предотвращая разрушение основных конструкций.
Металлы в экологии и промышленности

Металлы играют важную роль в современной экологии и промышленности. Они применяются в различных отраслях, таких как строительство, энергетика, автомобильная промышленность и другие.
Однако, использование металлов в процессе производства может оказывать негативное влияние на окружающую среду. Например, неконтролируемая выработка отходов, содержащих тяжелые металлы, может приводить к загрязнению водных ресурсов и почвы.
Кроме того, неправильное обращение с отходами предприятий может вызывать выбросы вредных веществ в атмосферу, что ведет к загрязнению воздуха и оказывает влияние на здоровье человека.
В связи с этим, для сохранения экологического равновесия требуется разработка и внедрение новых технологий и методов обработки металлов, способных минимизировать негативное влияние на окружающую среду.
Также стоит отметить, что металлы могут использоваться в экологических технологиях, например, в производстве солнечных батарей или электромобилей. Это позволяет уменьшить зависимость от ископаемых и перейти к более экологически чистым источникам энергии.
В целом, учет экологических аспектов при использовании металлов в промышленности является неотъемлемой частью современного устойчивого развития и требует постоянного внимания и разработки новых решений для устранения негативного воздействия на окружающую среду.
Упражнения и задания для подготовки к экзамену по металлам в химии

Подготовка к экзамену по металлам в химии включает выполнение различных упражнений и заданий, чтобы закрепить теоретические знания и развить навыки решения практических задач.
1. Идентификация металлов. Задания по идентификации металлов позволяют распознать различные металлы по их характерным свойствам. Выполняя данное задание, необходимо знать способы определения металлов, например, по реакции с кислотами или по цвету его солей.
2. Химические реакции металлов. Упражнения по решению химических реакций металлов помогут отработать умение описывать и балансировать уравнения химических реакций при взаимодействии металлов и растворов соляной кислоты и других соединений.
3. Окислительно-восстановительные реакции. Задания на определение окислителя и восстановителя в окислительно-восстановительных реакциях помогут разобраться в механизме этих реакций и научиться распознавать окислитель и восстановитель в химической реакции.
4. Применение металлов в промышленности. Задания на применение металлов в промышленности помогут узнать, какие металлы используются в различных отраслях промышленности, например, в производстве стальных изделий, технологии производства алюминия или лужение железа.
5. Расчеты по металлам. Упражнения и задания на расчеты по металлам позволят развить навыки решения задач, связанных с определением массы, объема или концентрации металлов в химическом соединении или растворе.
6. Тестовые задания. Тестовые задания на тему металлов помогут проверить уровень знаний и подготовленность к экзамену. Распределите время на выполнение заданий и старательно проверьте свои ответы.
Регулярное выполнение упражнений и заданий поможет вам успешно подготовиться к экзамену по металлам в химии и укрепить свои знания и навыки в данной области.
Вопрос-ответ

Какие основные понятия нужно знать о металлах в химии?
Основные понятия, которые необходимо знать о металлах в химии, включают следующие: атомный радиус, ионный радиус, металлическая связь, оксидация, восстановление, катионы, анионы, сплавы. Все эти понятия являются ключевыми для понимания свойств и реакций металлов.
Какие методы используются для определения металлической связи в химии?
В химии существует несколько методов для определения металлической связи. Некоторые из них включают рентгеноструктурный анализ, спектроскопию, магнитные методы. Рентгеноструктурный анализ позволяет определить расстояния между атомами в металлической структуре, а спектроскопия - изучать изменения в энергетических уровнях электронов и фотонов. Магнитные методы используются для изучения взаимодействия между электронами и магнитными полями в металлических соединениях.
