Металлы с переменной валентностью представляют собой группу химических элементов, которые способны образовывать соединения с различными степенями окисления. Это свойство позволяет им проявлять разнообразие химических свойств и функций в разных средах. Важно отметить, что переменная валентность характерна для нескольких элементов и является результатом наличия нескольких степеней окисления, которые зависят от условий окружающей среды и других факторов.
Наиболее известными металлами с переменной валентностью являются железо, медь, свинец, ванадий, марганец, молибден и титан. Каждый из этих металлов характеризуется наличием нескольких степеней окисления и образует различные оксидные формы, которые имеют разные физические и химические свойства. Например, железо может образовывать оксиды с валентностью +2 (FeO) и +3 (Fe2O3), а медь – с валентностью +1 (Cu2O) и +2 (CuO).
Таблица с перечнем металлов с переменной валентностью и их оксидными формами представлена ниже:
Металл | Основные оксидные формы
-------------------------
Железо | FeO, Fe2O3
Медь | Cu2O, CuO
Свинец | PbO, PbO2
Ванадий | VO, V2O5
Марганец | MnO2, MnO4
Молибден | MoO2, MoO3
Титан | TiO, TiO2
Металлы с переменной валентностью широко применяются в различных сферах, таких как металлургия, электроника, катализ и других. Их уникальные свойства позволяют использовать их в разных средах и процессах. Изучение металлов с переменной валентностью является важным аспектом в химической науке и позволяет лучше понять химические свойства и реактивность элементов.
Металлы с переменной валентностью
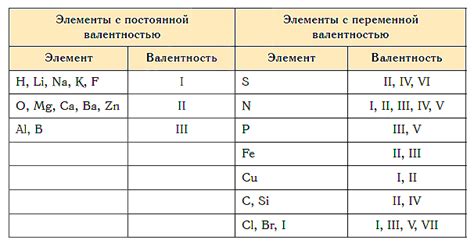
Металлы с переменной валентностью - это элементы, которые в химических соединениях могут принимать различные степени окисления. Это связано с наличием у этих элементов неполной заполненной внешней электронной оболочки.
Металлы с переменной валентностью широко представлены в периодической системе химических элементов. Некоторые из них имеют огромное количество оксидных форм, в то время как другие - только несколько.
Данные металлы обладают различными физическими и химическими свойствами, что позволяет им выполнять широкий спектр функций и применений в различных областях. Например, некоторые металлы с переменной валентностью используются в производстве катализаторов, электродов, магнитов и других устройств. Они также находят применение в медицине, энергетике, электронике и других отраслях.
Некоторые из наиболее известных металлов с переменной валентностью включают железо, медь, марганец, ванадий, уран и никель. Каждый из этих элементов имеет характеристические оксидные формы, которые широко используются в химической промышленности и науке.
Перечень химических элементов
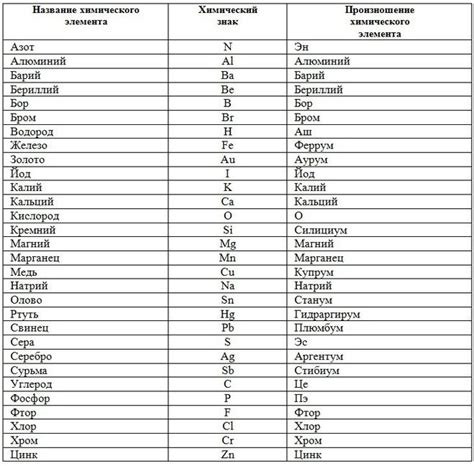
Металлы с переменной валентностью - это группа химических элементов, которые в химических соединениях могут формировать различные степени окисления. В таблице приведены некоторые химические элементы и их оксидные формы.
| Химический элемент | Оксидные формы |
|---|---|
| Железо | FeO, Fe2O3, Fe3O4 |
| Медь | Cu2O, CuO |
| Марганец | MnO, Mn2O3, MnO2 |
| Ванадий | VO, V2O3, V2O5 |
| Кобальт | CoO, Co2O3 |
Эти элементы проявляют различную валентность в своих оксидах, что обусловлено нестабильностью окисненных состояний. Это свойство позволяет им образовывать разнообразные соединения и принимать участие в различных химических реакциях.
Изучение металлов с переменной валентностью является важным направлением в химии и имеет большое применение в различных технологических процессах и промышленных производствах. Кроме того, эти элементы играют важную роль в биохимии и жизнедеятельности организмов.
Оксидные формы элементов

Металлы с переменной валентностью образуют различные оксидные формы, представляющие собой соединения элемента с кислородом. Оксидные формы металлов широко используются в различных отраслях промышленности, а также в научных исследованиях.
В таблице перечислены некоторые химические элементы и их оксидные формы:
| Химический элемент | Оксидные формы |
|---|---|
| Железо (Fe) | FeO, Fe2O3, Fe3O4 |
| Медь (Cu) | Cu2O, CuO |
| Марганец (Mn) | MnO, MnO2, Mn2O3 |
| Сурьма (Sb) | Sb2O3, Sb2O5 |
| Вольфрам (W) | WO2, WO3 |
Оксидные формы металлов обладают различными свойствами и находят широкое применение в различных областях. Например, оксид железа (Fe2O3), известный как красная руда, является основным источником железа в металлургии. Оксид меди (Cu2O) применяется в электронике и солнечных батареях.
Оксиды металлов играют важную роль в химических реакциях и являются важными компонентами многих материалов, таких как керамика, стекло и пигменты. Некоторые оксиды обладают также семикондукторными свойствами и используются в электронике и оптике.
Изучение оксидных форм элементов является важной областью химической науки и имеет практическое применение в различных технологических процессах и материалах.
Вопрос-ответ

Какие элементы из таблицы периодов имеют переменную валентность?
Многие элементы из таблицы периодов имеют переменную валентность. Некоторые из них: железо (Fe), марганец (Mn), хром (Cr), медь (Cu), серебро (Ag), олово (Sn), свинец (Pb) и другие.
Какие оксидные формы имеют элементы с переменной валентностью?
Элементы с переменной валентностью могут образовывать несколько оксидных форм с различной степенью окисления. Например, соединения железа могут быть представлены оксидами FeO, Fe2O3 и Fe3O4, марганец - оксидом MnO2, хром - оксидами CrO2 и Cr2O3, медь - оксидами CuO и Cu2O, и так далее.
Для чего используются металлы с переменной валентностью?
Металлы с переменной валентностью имеют широкий спектр применений в различных отраслях промышленности. Например, железо используется в производстве стали, марганец - в производстве батареек и сплавов, хром - в производстве нержавеющей стали и красок, медь - в электротехнической промышленности, серебро - в ювелирном производстве и пр. Благодаря своим свойствам переменной валентности, эти металлы находят широкое применение в различных технических и химических процессах.
Какие примеры металлов с переменной валентностью можно привести?
Примеры металлов с переменной валентностью включают такие элементы, как железо (Fe), марганец (Mn), хром (Cr), медь (Cu), серебро (Ag), олово (Sn), свинец (Pb) и другие. Они обладают способностью образовывать соединения с различной степенью окисления, что делает их полезными в разных областях науки и техники.
