Вода обычно является безопасным и нейтральным веществом, но есть некоторые металлы, которые могут реагировать с ней, вызывая различные эффекты и реакции. Возможность металлов реагировать с водой является результатом их химической активности и наличия свободных электронов в их структуре.
Один из наиболее известных металлов, реагирующих с водой, это натрий. При контакте с водой натрий начинает активно взаимодействовать с молекулами H2O, образуя гидроксид натрия и выделяя водород. Этот процесс сопровождается характерным шипящим звуком и образованием пузырьков газа.
Еще одним металлом, реагирующим с водой, является калий. При соприкосновении с водой калий выделяет водород и образует гидроксид калия. В результате реакции образуется щелочное растворение, который имеет высокую щелочность и может вызвать ощущение жжения на коже.
Алюминий - еще один металл, способный реагировать с водой. Однако, реакция алюминия с водой проходит медленно и требует наличия кислорода для активации. При контакте с водой алюминий образует оксид алюминия, который создает на поверхности металла защитную пленку, препятствующую дальнейшему взаимодействию с водой.
Таким образом, существуют различные металлы, которые могут реагировать с водой при комнатной температуре. Эти реакции вызывают образование газа, изменение pH раствора и другие химические эффекты. Изучение этих реакций помогает лучше понять химические свойства металлов и их взаимодействие с окружающей средой.
Металлы, реагирующие с водой

Некоторые металлы могут проявлять химическую реакцию с водой при комнатной температуре. Эта реакция обычно сопровождается выделением водорода и образованием осадка в виде гидроксида металла.
Одним из наиболее известных металлов, реагирующих с водой, является натрий. При контакте с водой натрий активно реагирует, выделяя водород и образуя гидроксид натрия. Эта реакция сопровождается появлением пламени и хлопком.
Другим металлом, реагирующим с водой, является калий. Калий также выделяет водород и образует гидроксид калия. Эта реакция проходит еще более интенсивно, чем у натрия, и также сопровождается появлением пламени.
Алюминий является еще одним металлом, реагирующим с водой. Однако, алюминий реагирует не напрямую с водой, а только с водными растворами щелочей, таких как гидроксид натрия или гидроксид калия. При этом выделяется водород, а алюминий окисляется до оксида алюминия.
- Натрий
- Калий
- Образуют гидроксиды
- Выделяют водород
Химическая реакция металлов с водой не только интересна, но и находит применение в различных областях. Эти металлы используются в процессе производства гидрогенового топлива, а также в химической промышленности для синтеза различных соединений.
Массивные металлы
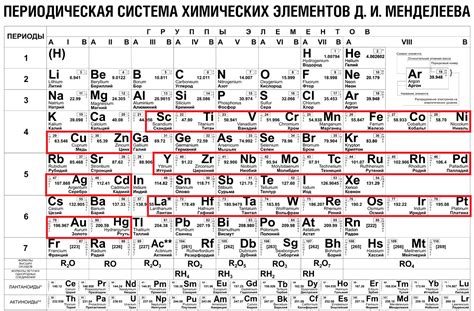
Массивные металлы – это металлы, которые обладают большой плотностью и являются одними из самых тяжелых веществ на земле. Они часто используются в различных отраслях промышленности благодаря своим уникальным свойствам.
Одним из таких металлов является олово. Оно обладает высокой плотностью и широко применяется в производстве сплавов, а также для создания легированных сталей. Олово также используется в продукции электроники, например, для изготовления контактов и паяльных припоев.
Еще одним массивным металлом является свинец. Он обладает высокой плотностью и является одним из наиболее распространенных металлов в мире. Свинец используется в производстве аккумуляторов, покрытий для кабелей, а также для создания сплавов с другими металлами.
Никель – еще один массивный металл, который имеет высокую плотность и применяется в различных отраслях промышленности. Он используется в производстве нержавеющей стали, а также в производстве монет и декоративных изделий.
Медь – один из самых известных массивных металлов, который обладает высокой электропроводностью и теплопроводностью. Она широко используется в электротехнике, а также в строительстве и производстве медных сплавов.
Самораспадающиеся металлы в воде

Некоторые металлы обладают особенностью самораспадаться при контакте с водой. Это происходит из-за химической реакции между металлом и молекулами воды, которая приводит к образованию газа или других продуктов.
Одним из самораспадающихся металлов является натрий. При взаимодействии с водой натрий активно реагирует, выделяя большое количество водорода. Эта реакция является очень быстрой и сопровождается высокими температурами и высоким давлением газа.
Еще одним самораспадающимся металлом является калий. Он также вступает в реакцию с водой, выделяя водород и образуя щелочное вещество - гидроксид калия. При этом выделяется большое количество тепла, что делает реакцию очень яркой и заметной.
Алюминий также считается самораспадающимся металлом в воде. В контакте с водой алюминий покрывается пленкой гидроксида алюминия, которая не пропускает воду и предотвращает дальнейшую реакцию.
Важно отметить, что реакция между самораспадающимися металлами и водой может быть опасной, поскольку выделение газа или тепла может вызвать взрывоопасную ситуацию. Поэтому такие металлы требуют особой осторожности при обращении с ними и должны использоваться только в специальных условиях и под контролем квалифицированных специалистов.
Металлы, реагирующие с образованием газа в воде
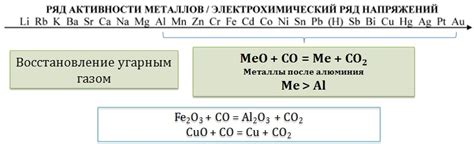
Ряд металлов проявляет свойство реагировать с водой при комнатной температуре с образованием газа. Это свойство обусловлено их активностью и химической реакцией с водой. При взаимодействии с водой эти металлы выделяют водородный газ и образуют соответствующие оксиды. Такие металлы считаются реактивными и могут быть опасными в использовании.
Одним из наиболее известных металлов, реагирующих с образованием газа в воде, является натрий (Na). При погружении натрия в воду происходит реакция, в результате которой образуется щелочной гидроксид и выделяется водородный газ. Подобная реакция натрия с водой является широкоизвестным демонстрационным опытом в химических лабораториях и образовательных учреждениях.
Кальций (Ca) также реагирует с водой с образованием газа. При контакте кальция с водой происходит резкая реакция, в результате которой образуется щелочной гидроксид и выделяется водородный газ. Однако реакция кальция с водой проходит менее интенсивно, чем реакция натрия, и может требовать более длительного времени для образования заметного количества газа.
Другим металлом, реагирующим с образованием газа в воде, является калий (K). Реакция калия с водой аналогична реакции натрия и кальция: образуется щелочной гидроксид и выделяется водородный газ. Однако в результате данной реакции могут наблюдаться более яркие вспышки и пламя, поэтому калий также требует осторожного обращения и особых условий использования.
Таким образом, металлы, реагирующие с образованием газа в воде, представляют определенный интерес и используются в образовательных целях. Их свойства и реакции с водой выполняют важную роль в понимании основ химии и существенно влияют на множество процессов в природе и промышленности.
Металлы, реагирующие с образованием гидроксидов в воде
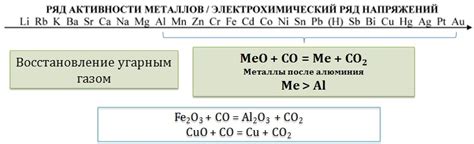
Некоторые металлы могут проявлять активность при контакте с водой при комнатной температуре. В результате такой реакции образуются гидроксиды металлов. Гидроксиды представляют собой соединения, состоящие из металлической катионной части и одного или нескольких гидроксильных ионов.
Один из наиболее известных примеров реакции металлов с образованием гидроксидов - это реакция натрия с водой. При контакте металлического натрия с водой происходит быстрая и интенсивная реакция, в результате которой образуется гидроксид натрия (NaOH) и выделяется водород (H₂). Реакция описывается следующим уравнением:
2Na + 2H₂O → 2NaOH + H₂
Также стоит упомянуть о реакции калия с водой. При реакции калия с водой образуется гидроксид калия (KOH) и выделяется водород (H₂). Уравнение реакции выглядит следующим образом:
2K + 2H₂O → 2KOH + H₂
Помимо натрия и калия, реактивность с водой также проявляют литий (Li), рубидий (Rb), цезий (Cs), а также кальций (Ca), стронций (Sr) и барий (Ba). Реакции этих металлов с водой приводят к образованию соответствующих гидроксидов.
Важно отметить, что реактивность металлов с водой может варьироваться в зависимости от условий, таких как температура и концентрация воды. Кроме того, некоторые металлы, такие как алюминий (Al) и цинк (Zn), образуют гидроксиды только при длительном контакте с водой или в присутствии определенных катализаторов.
Вопрос-ответ

Какие металлы реагируют с водой при комнатной температуре?
Некоторые металлы, такие как натрий (Na) и калий (K), реагируют с водой, образуя гидроксид металла и выделяя водород газ.
Почему металлы реагируют с водой?
Металлы реагируют с водой из-за их химических свойств. Когда металл вступает в контакт с водой, происходит окислительно-восстановительная реакция, при которой металл отдает электроны, образуя гидроксид и выделяя водород газ.
Может ли реакция металла с водой привести к опасным последствиям?
Да, реакция металла с водой может привести к опасным последствиям. В некоторых случаях, реакция может быть сильно экзотермической, то есть выделять большое количество тепла, что может вызвать возгорание вещества. Кроме того, выделение горючих газов, таких как водород, также может представлять опасность.
Какие применения могут иметь металлы, реагирующие с водой?
Металлы, которые реагируют с водой, могут иметь различные применения. Например, натрий и калий используются в химической промышленности для производства гидроксидов и других химических соединений. Они также могут использоваться в лабораториях в качестве агентов в реакциях. Кроме того, водород, образующийся при реакции, может использоваться в качестве источника энергии или в производстве аммиака и других химических соединений.













