Металлы составляют значительную часть элементов в периодической таблице химических элементов. Они обладают различными свойствами и играют важную роль в нашей жизни, используясь в различных областях, от строительства до производства электроники. Расположение металлов в периодической таблице объясняется их электронной конфигурацией и химическими свойствами.
Перед магнием, в периодической таблице находятся несколько металлов, которые определяются их порядковыми номерами и химическими свойствами. Прежде всего, это алкалинные металлы, такие как литий (Li), натрий (Na), калий (K) и рубидий (Rb). Эти металлы характеризуются низкой плотностью, низкой температурой плавления и реактивностью с водой.
Также перед магнием находятся металлы из группы переходных элементов, такие как скандий (Sc), титан (Ti) и ванадий (V). Они обладают высокой температурой плавления, прочностью и применяются в различных отраслях промышленности, включая производство сплавов и каталитических реакций.
Металлы, находящиеся перед магнием в периодической таблице, играют важную роль в химических реакциях и имеют широкий спектр применений. Они помогают нам понять свойства металлов и их взаимодействие с другими элементами. Понимание расположения металлов в периодической таблице важно для изучения химии и применения металлов в нашей повседневной жизни.
Металлы до магния в периодической таблице
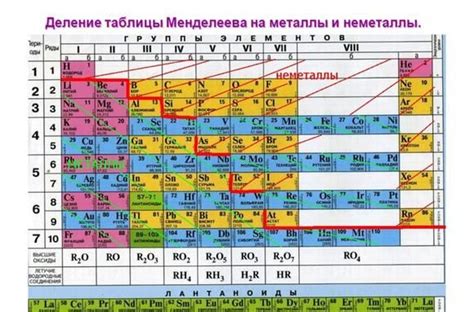
Магний (Mg) находится во втором периоде и второй группе периодической таблицы. Периодическая таблица химических элементов разделена на несколько блоков, каждый из которых содержит различные химические элементы. Металлы до магния находятся в первом периоде и первой группе.
Первым металлом до магния является литий (Li). Литий является легким металлом, который обладает низкой плотностью и хорошей проводимостью тепла и электричества. Он обычно используется в литий-ионных аккумуляторах, а также в различных химических процессах и синтезе органических соединений.
Вторым металлом до магния является натрий (Na). Натрий имеет мягкий серебристо-белый цвет и является очень реактивным элементом. Он широко используется в промышленности для производства щелочей, а также в пищевой промышленности для соления и консервирования продуктов.
Третьим металлом до магния является калий (K). Калий - мягкий серебристо-белый металл, который реагирует с водой и воздухом. Он является важным элементом для растительного роста, и его соединения используются как удобрения в сельском хозяйстве.
- Литий (Li)
- Натрий (Na)
- Калий (K)
Все эти металлы до магния обладают различными физическими и химическими свойствами и используются в различных отраслях промышленности и науки.
Щелочные металлы
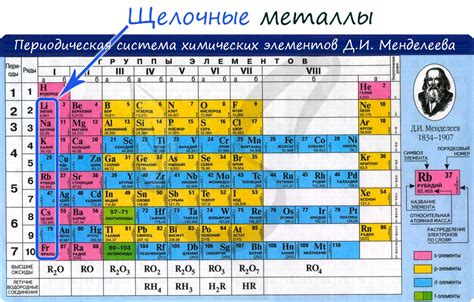
Щелочные металлы представляют собой группу элементов, находящихся в периодической таблице химических элементов до магния. Они включают в себя литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr). Все эти элементы являются химически активными и характеризуются низкой плотностью, низкой температурой плавления и высокой реактивностью.
Щелочные металлы обладают высокой электроотрицательностью и легко образуют ионы с положительным зарядом. Они активно реагируют с водой, образуя щелочные растворы с гидроксидами, например, гидроксидом натрия (NaOH) или гидроксидом калия (KOH).
Хотя щелочные металлы встречаются в природе в основном в виде соединений, их можно получить путем электролиза соответствующих солей или обработки минеральных руд. Самым распространенным щелочным металлом является натрий, который находится в большом количестве в морской воде и в основных минералах, таких как хлорид натрия (NaCl) или карбонат натрия (Na2CO3).
Щелочные металлы широко используются в различных отраслях промышленности и науки. Калий, например, используется в производстве удобрений, а рубидий применяется в лучевой терапии и в нефтяной промышленности. Литий широко используется в производстве аккумуляторов и лекарственных препаратов. Щелочные металлы также используются в различных химических реакциях и взаимодействиях, благодаря своей активности и способности образовывать неорганические соединения с различными элементами.
Таким образом, щелочные металлы представляют собой важную группу химических элементов в периодической таблице, которые играют значительную роль в промышленности, науке и технологии.
Щелочноземельные металлы
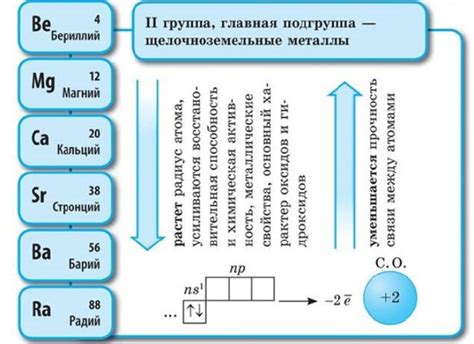
Щелочноземельные металлы — это группа химических элементов, которые находятся вторыми по активности после щелочных металлов в периодической таблице. Они расположены ниже магния и включают в себя следующие элементы: кальций, стронций, барий и радий.
Как и щелочные металлы, щелочноземельные металлы характеризуются высокой реактивностью и образованием ионов с положительным зарядом. Они обладают металлическим блеском, хорошей электропроводностью, высокой плотностью и температурой плавления. Они также образуют двухвалентные катионы, т.е. имеют степень окисления +2.
Щелочноземельные металлы часто встречаются в природе в виде соединений, таких как карбонаты, сульфаты и оксиды. Они играют важную роль в различных процессах в природной среде и имеют широкое промышленное использование.
Кальций, самый известный из щелочноземельных металлов, является важным компонентом костей и зубов человека, а также необходим для работы мышц и нервной системы. Стронций используется в производстве огнетушителей и ядерных реакторов, а барий - в производстве стекла, фарфора и в качестве бериллидной добавки к сплавам.
Наиболее редкий из щелочноземельных металлов - радий, обладает очень высокой радиоактивностью и в настоящее время не имеет практического применения в промышленности. Он был открыт в 1898 году и является одним из самых опасных известных химических элементов.
Переходные металлы

Переходные металлы - это элементы, которые находятся в середине периодической таблицы между аргоном и кальцием. Они включают в себя последовательность элементов от скандия до цинка, а также последовательность элементов от иттрия до рения. Эти элементы часто имеют характерные свойства переходных металлов и играют важную роль в различных областях науки и техники.
Основными характеристиками переходных металлов являются их изменяемость валентности и формирование комплексных соединений. Они обладают переменными зарядами и способностью образовывать стабильные соединения со многими другими элементами. Это делает их важными для катализа и синтеза различных соединений.
Переходные металлы обладают также характерной блоковой структурой, которая имеет влияние на их химические и физические свойства. Они обладают высокой плотностью, твердыми и прочными свойствами, а также высокими температурами плавления и кипения. Их способность к образованию различных оксидов и солей делает их важными в процессах экстракции металлов и производства материалов с определенными свойствами.
Примеры переходных металлов:
- Скандий (Sc)
- Титан (Ti)
- Ванадий (V)
- Хром (Cr)
- Марганец (Mn)
- Железо (Fe)
- Кобальт (Co)
- Никель (Ni)
- Медь (Cu)
- Цинк (Zn)
Переходные металлы играют важную роль в различных отраслях промышленности, включая металлургию, электротехнику, химию и многие другие. Их уникальные свойства и возможности делают их ценными компонентами в различных материалах и процессах производства, что позволяет создавать новые технологии и материалы с определенными свойствами и характеристиками.
Поиск места магния
Магний - металл, расположенный в периодической таблице элементов, между бериллием (Be) и алюминием (Al). Химический символ магния - Mg. Этот элемент является вторым по величине среди щелочноземельных металлов и обладает атомным номером 12.
Магний имеет характерные свойства металлов: он обладает серебристым блеском, хорошей теплопроводностью и прочностью. Кроме того, магний легко реагирует с кислородом и многими кислотами, что делает его важным элементом в различных промышленных и технических процессах.
Место магния в периодической таблице связано с его электронной конфигурацией. Магний содержит два электрона в своей внешней оболочке, что делает его аналогом щелочноземельных металлов. Однако, магний имеет некоторые характеристики, которые делают его уникальным и отличают его от других металлов.
Изучение расположения магния в периодической таблице позволяет получить представление о его свойствах и реактивности. Это помогает ученым и инженерам использовать магний в различных отраслях промышленности, а также разрабатывать новые материалы и технологии на его основе.
Расположение других металлов
В периодической таблице элементы расположены в порядке возрастания атомного номера. За магнием в таблице находятся еще несколько металлов, которые имеют свои особенности и свойства.
Следующим металлом после магния является алюминий. Он обладает высокой термической и электрической проводимостью, а также хорошими светоотражающими свойствами. Алюминий широко используется в различных отраслях промышленности, например, в производстве авиационных и космических конструкций, электротехнике и строительстве.
За алюминием идет кремний, который является основным элементом в составе кремниевых полупроводников. Кремний обладает положительными и отрицательными электрическими свойствами, что позволяет использовать его для создания различных электронных устройств, например, микрочипов и солнечных батарей.
Далее следует фосфор, который широко используется в производстве удобрений и в сельском хозяйстве. Фосфор является важным элементом для роста растений и применяется в виде фосфорных удобрений для обеспечения урожайности и питательности почв.
После фосфора в таблице находится сера. В природе сера встречается в виде серных соединений и широко применяется в различных отраслях, таких как химическая промышленность, производство горюче-смазочных материалов и фармацевтическая промышленность.
Таким образом, в периодической таблице после магния находятся металлы алюминий, кремний, фосфор и сера, каждый из которых имеет свои уникальные свойства и применение в различных областях науки и техники.
Вопрос-ответ

Какие элементы находятся до магния в периодической таблице?
Перед магнием в периодической таблице находятся элементы литий, бериллий и бор.
Почему магний находится во втором периоде таблицы?
Магний находится во втором периоде таблицы, потому что он имеет 12 электронов и его электронные орбитали заполняются в следующем порядке: 1s^2 2s^2 2p^6.
Какие свойства имеют металлы, находящиеся перед магнием в периодической таблице?
Металлы, находящиеся перед магнием в периодической таблице, обладают различными свойствами. Например, литий является мягким металлом, который легко реагирует с водой и обладает химической активностью. Бериллий обладает высокой плотностью, жаростойкостью и является нерастворимым в воде. Бор является полуметаллом и обладает семиметаллическими свойствами.
Какие элементы находятся перед магнием в группе 2 периодической таблицы?
Перед магнием в группе 2 периодической таблицы находятся элементы бериллий (Be) и бор (B). Они оба являются металлами и имеют различные характеристики и свойства.
